Dokumentation und Rückverfolgbarkeit in Pharma-Rohrleitungsprojekten sind keine nachträgliche Papierarbeit nach der Installation. Sie sind die Beweiskette, die belegt, dass das installierte System mit dem genehmigten Material, der Oberflächenbeschaffenheit, den Schweißnähten, der Inspektion und der hygienischen Designabsicht übereinstimmt. In GMP-Projekten kann eine Rohrleitungsschleife mechanisch fertiggestellt sein und dennoch nicht freigegeben werden, weil die Dokumentation nicht eindeutig belegt, was installiert wurde, wie es gefertigt wurde, welche Änderungen vor Ort vorgenommen wurden und ob die endgültige Montage noch den genehmigten Projektstandards entspricht.
Deshalb behandeln erfahrene Ingenieure Übergabedokumente nicht als administrative Übergabe. Sie betrachten sie von Anfang an als Teil der Projektsteuerung. Wenn Materialrückverfolgbarkeit, Schweißprotokolle, Oberflächenbeschaffenheitsaufzeichnungen, Inspektionsnachweise, Änderungsmarkierungen und Übergabedokumente nicht vor der Ausschreibung definiert werden, versucht das Projekt oft später, die Beweiskette mit höheren Kosten und geringerer Zuverlässigkeit nachzubilden. Dieser Leitfaden erklärt, was Dokumentation und Rückverfolgbarkeit in Pharma-Rohrleitungsprojekten wirklich bedeuten, welche Aufzeichnungen am wichtigsten sind, wo die Beweiskette typischerweise unterbrochen wird und wie GMP-Teams das richtige Dokumentationspaket vor Fertigungsbeginn definieren können.
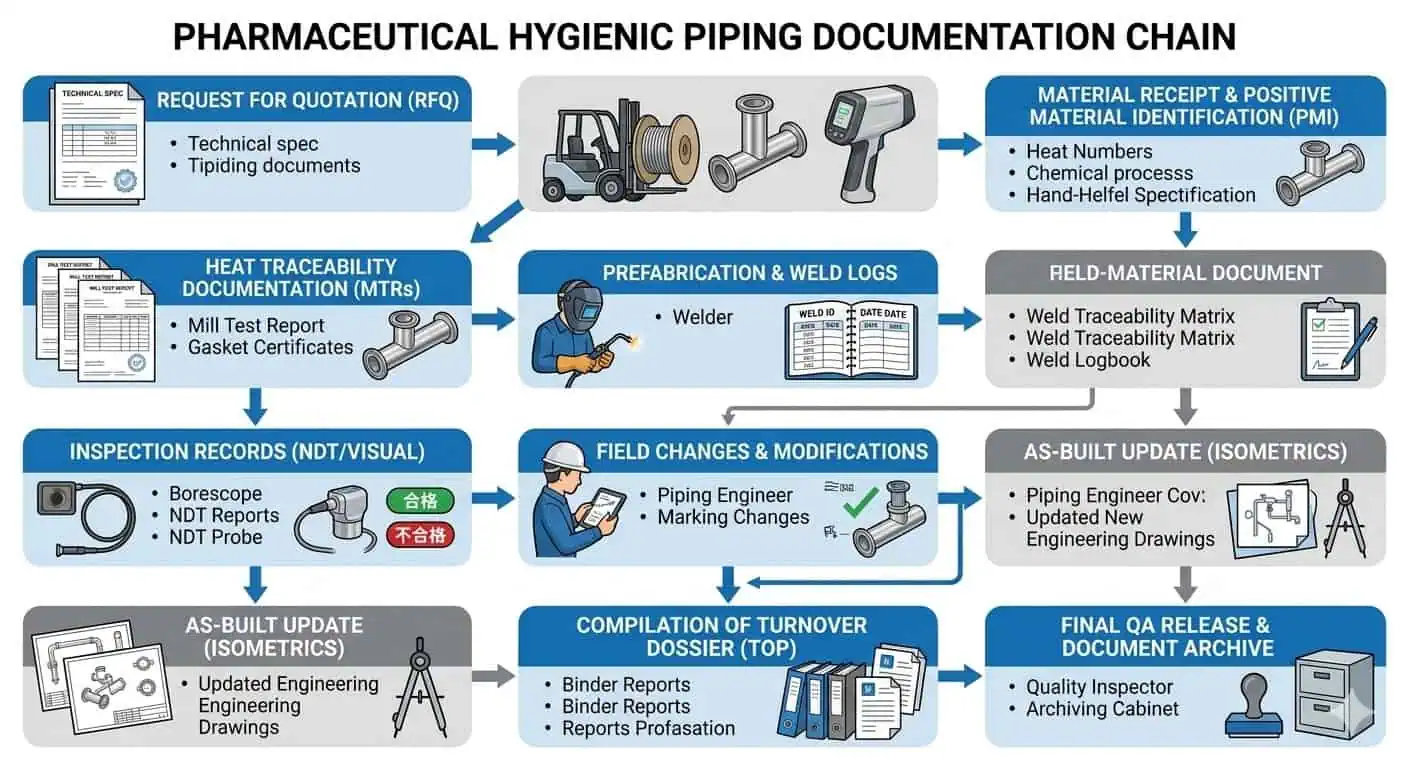
In der realen pharmazeutischen Praxis treten Dokumentationsprobleme selten als dramatische mechanische Ausfälle auf. Sie zeigen sich als langsamere QA-Abschlüsse, ungelöste Übergabekommentare, unklare Schweißhistorie, nicht übereinstimmende Rohrleitungsabschnittsgeschichten oder Unsicherheit darüber, ob die endgültig installierte Schleife noch die genehmigte hygienische Absicht widerspiegelt. Deshalb ist eine robuste Dokumentation keine Präferenz für Papierkram. Sie ist eine technische Kontrolle.
Warum Dokumentation und Rückverfolgbarkeit in Pharma-Rohrleitungsprojekten wichtig sind
Dies ist ein QA- und Freigabethema, nicht nur ein technisches Ablagethema
In Pharma-Rohrleitungen ist Dokumentation Teil der Freigabekontrolle, nicht nur der Projektadministration. EU GMP Kapitel 4 beschreibt Dokumentation nicht als Ablageerleichterung. Es beschreibt gute Dokumentation als einen wesentlichen Teil des Qualitätssicherungssystems und den Mechanismus, der verwendet wird, um Aktivitäten, die die Produktqualität beeinflussen, festzulegen, zu steuern, zu überwachen und aufzuzeichnen. Die FDA-Logik weist in dieselbe Richtung: Produktkontaktausrüstung muss gebrauchstauglich sein, und Reinigung, Wartung und Gerätehistorie müssen kontrolliert und aufgezeichnet werden. Mit anderen Worten, die installierte Schleife muss technisch korrekt und gleichzeitig nachweisbar korrekt sein.
Typischer Branchenfall: Eine Produktkontakt-Transferleitung ist vollständig installiert, druckgeprüft und visuell akzeptabel. Die Betriebsabteilung sieht ein fertiges Rohrleitungssystem. Die QA sieht eine unvollständige Beweiskette, weil das endgültige Dossier noch nicht eindeutig die genehmigte Materialidentität, Schweißhistorie und endgültige as-built-Konfiguration zusammenführen kann. Die Rohrleitung ist physisch vorhanden, aber die Freigabelogik ist noch ungelöst.
Expertenrat: Wenn das Projektteam die Dokumentation als etwas betrachtet, das bei der Übergabe beginnt, ist es bereits zu spät. In der GMP-Rohrleitungstechnik muss die Freigabegeschichte aufgebaut werden, während die Schleife entworfen, gefertigt, inspiziert und geändert wird – nicht nachdem die letzte Klemme angezogen ist.
Technische Anmerkung: In der GMP-Rohrleitungstechnik ist die installierte Schleife nur so freigabefähig wie die Beweiskette, die ihren endgültigen Benetzungszustand nachweist.
Warum Pharma-Rohrleitungsprojekte oft bei der Übergabe scheitern, nicht bei der Fertigung
Viele Pharma-Rohrleitungsprojekte scheitern nicht, weil die Schleife schlecht gebaut wurde. Sie scheitern, weil das Projekt nicht in freigabereifer Form nachweisen kann, dass die endgültig installierte Schleife noch mit der genehmigten hygienischen Absicht übereinstimmt. Das ist eine andere Art von Fehler, aber in der GMP-Arbeit ist er oft der gefährlichere, weil er spät auftritt, nachdem das System bereits mechanisch vollständig erscheint. EU GMP Kapitel 4 und die FDA-Aufzeichnungslogik unterstützen beide die gleiche praktische Schlussfolgerung: Wenn Reinigungsverlauf, Komponentenidentität, Schweißstatus und installierte Konfiguration nicht zuverlässig rekonstruiert werden können, wird das System bei der Freigabe und später im Betrieb schwerer zu verteidigen.
Typischer Branchenfall: Das Feldinstallationsteam beendet eine hygienische Schleife und geht davon aus, dass die schwierige Arbeit vorbei ist. Eine spätere Überprüfung zeigt, dass mehrere Rohrstränge vor Ort überarbeitet wurden, um die Verlegung und Neigung zu verbessern, aber die endgültige Schweißkarte, Material-Standort-Matrix und die as-built-Dokumentation wurden nie vollständig abgeglichen. Niemand behauptet, dass das Metall falsch ist. Das Problem ist, dass das Projekt nicht mehr sauber nachweisen kann, welche zertifizierten Materialien, Schweißaufzeichnungen und Inspektionsergebnisse zur endgültig installierten Anordnung gehören. An diesem Punkt kämpft die Schleife nicht gegen einen Fertigungsfehler. Sie kämpft gegen einen Freigabebeweisfehler.
Erfahrene Projektingenieure definieren daher die Dokumentationskette vor der Ausschreibung, nicht nach der mechanischen Fertigstellung. Sobald die Fertigung beginnt, wird jeder unkontrollierte Feldzuschnitt, Rohrstrangaustausch oder Abzweig-Umverlegung rückwirkend schwerer abzuschließen. Die technische Lehre ist einfach: In der GMP-Rohrleitungstechnik endet das Projekt, wenn man bis zur Übergabe wartet, um zu entscheiden, was rückverfolgbar sein muss, normalerweise damit, die Beweiskette mit höheren Kosten und geringerer Zuversicht neu aufzubauen.
Was der GMP- und regulatorische Rahmen tatsächlich erfordert
Die nützlichsten Vorschriften sind diejenigen, die ändern, was das Projektteam vor der Übergabe definiert und aufzeichnet. In diesem Thema umfasst der Kernrahmen in der Regel:
- ASME BPE, der Materialien, Konstruktion, Fertigung, Inspektionen, Prüfungen und Zertifizierungslogik für Bioprozess- und Pharmaanlagen abdeckt.
- FDA 21 CFR 211.65, die vorschreibt, dass produktberührende Oberflächen nicht reaktiv, nicht additiv und nicht absorbierend sein müssen.
- FDA 21 CFR 211.67, der die Reinigung und Wartung von Anlagen an schriftliche Verfahren und Aufzeichnungen bindet.
- FDA 21 CFR 211.182, der Reinigungs-, Wartungs- und Nutzungsprotokolle für Hauptanlagen behandelt.
- FDA 21 CFR 211.184, der Aufzeichnungen zu Komponenten, Behältern, Verschlüssen und Etiketten abdeckt.
- EU GMP Kapitel 4, der Dokumentation als wesentlichen Teil des Qualitätssicherungssystems definiert und erfordert, dass Aufzeichnungen kontrolliert, genau, rückverfolgbar und angemessen aufbewahrt werden.
Forschungserkenntnis: Diese Quellen behandeln Dokumentation nicht als Hintergrundunterstützung. Sie behandeln sie als kontrollierten Teil der GMP-Ausführung. Für Rohrleitungsteams bedeutet das, dass die Frage nie nur lautet: “Welche Aufzeichnungen haben wir?”, sondern: “Beweisen diese Aufzeichnungen das endgültige benetzte System noch klar genug für die QA-Freigabe?”.”
Was in einem GMP-Rohrleitungsprojekt rückverfolgbar sein muss
Rohre, Fittings, Ventile und andere benetzte Komponenten
Die Rückverfolgbarkeit sollte dem benetzten Pfad folgen, nicht nur den größten oder einfachsten Komponenten. Viele Teams verwalten Rohre gut, behandeln aber kleinere Fittings, Membranen, Probenventile, Ferrule, Dichtungen und Abzweigkomponenten zu nachlässig. In GMP-Projekten ist das ein Fehler. Die kleinsten benetzten Teile sind oft am einfachsten zu ersetzen, am schwierigsten später zu verfolgen und die ersten, die während der Übergabe QA-Fragen aufwerfen.
Typischer Branchenfall: Die Rückverfolgbarkeit von Rohren ist vollständig, aber das Übergabepaket wird bei lokalen Baugruppen schwach, weil Fittings, Dichtungen oder Probenventil-Innenteile außerhalb des Hauptkontroll-Workflows gehandhabt wurden. Die Leitung sieht bei der Begehung gut aus, doch die schwächste Rückverfolgbarkeitsverbindung sitzt genau dort, wo die hygienische Baugruppe am komplexesten ist.
Expertenrat: Wenn eine Komponente wichtig genug ist, um als Teil des hygienischen Designs spezifiziert zu werden, ist sie wichtig genug, um als Teil der Übergabelogik rückverfolgbar zu sein. In der Praxis erhalten Teams eine bessere QA-Abschluss, wenn sie die Rückverfolgbarkeit um den gesamten benetzten Pfad definieren, anstatt nur um Rohre allein.
Materialzertifikate, Chargennummern und Losidentität
Die Materialrückverfolgbarkeit ist nur nützlich, wenn der installierte Standort sauber auf den ursprünglichen Aufzeichnungssatz zurückgeführt werden kann. Materialprüfberichte, EN 10204 3.1-Zertifikate, Chargennummern und Eingangsaufzeichnungen sind alle wichtig, aber nur, wenn das Projekt die Verbindung zwischen Lieferantenidentität und installiertem Rohrstrang, Fitting oder Baugruppenstandort bewahrt. Ein Stapel Zertifikate ohne saubere Standortmatrix ist kein starkes Rückverfolgbarkeitspaket.
Typischer Branchenfall: Das Projekt verfügt über die korrekten Materialzertifikate, aber nach dem Schneiden vor Ort, dem Neuaufspulen und der lokalen Umleitung kann das Übergabeteam nicht schnell nachweisen, welche Chargennummern in welchen installierten Abzweigabschnitten gelandet sind. Das Problem ist nicht fehlendes Papier. Das Problem ist, dass das Papier nicht mehr klar auf die installierte Realität abgebildet werden kann.
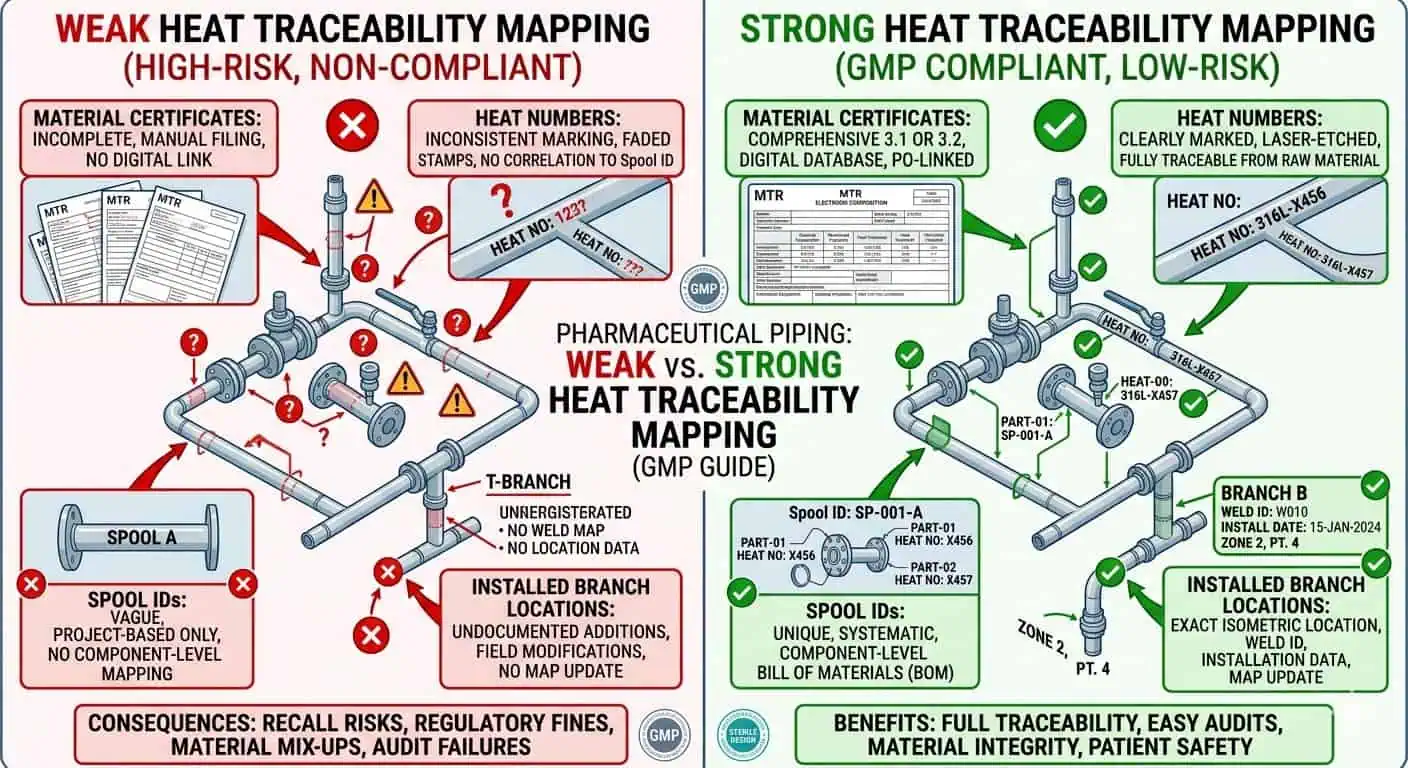
Expertenrat: In Hochrisiko-Produktkontaktsystemen sollte die Rückverfolgbarkeitsmatrix frühzeitig definiert werden, anstatt zu erlauben, dass Materialaufzeichnungen und Spool-Aufzeichnungen sich separat entwickeln. Sobald Feldmodifikationen beginnen, wird der Wiederaufbau dieser Verbindung langsamer und weniger zuverlässig.
Schweißpläne, Orbital-Schweißprotokolle und Prüfstatus
Schweißdokumentation ist oft der betrieblich wichtigste Teil der Rohrleitungsnachweiskette. In hygienischen Pharmasystemen sind Schweißnummern, Maschineneinstellungen, Bedieneridentität, Daten, Prüfstatus, Reparaturhistorie und Annahmestatus oft entscheidender als Teams erwarten. Das liegt daran, dass die Schweißnaht der Punkt ist, an dem Materialidentität, Fertigungsqualität, Prüfnachweise und endgültige hygienische Leistung zusammenlaufen. ASME BPE ist hier nützlich, nicht weil es Papierkram um seiner selbst willen erzeugt, sondern weil es Fertigung, Prüfung, Test und Zertifizierung als ein verbundenes Kontrollrahmenwerk behandelt. In Pharmaprojekten sind Schweißprotokolle daher nicht nur Werkstattaufzeichnungen. Sie sind Freigabeaufzeichnungen.
Typischer Ingenieursfall: Eine Schleife sieht bei der Begehung akzeptabel aus, aber die QA markiert sie dennoch, weil der Schweißplan und die endgültige Spool-Revision nach Feldänderungen nicht mehr übereinstimmen. Die installierten Schweißnähte mögen physisch akzeptabel sein, aber der Dokumentationssatz beweist nicht mehr, welche Aufzeichnungen zu welchen endgültigen Schweißpositionen gehören.
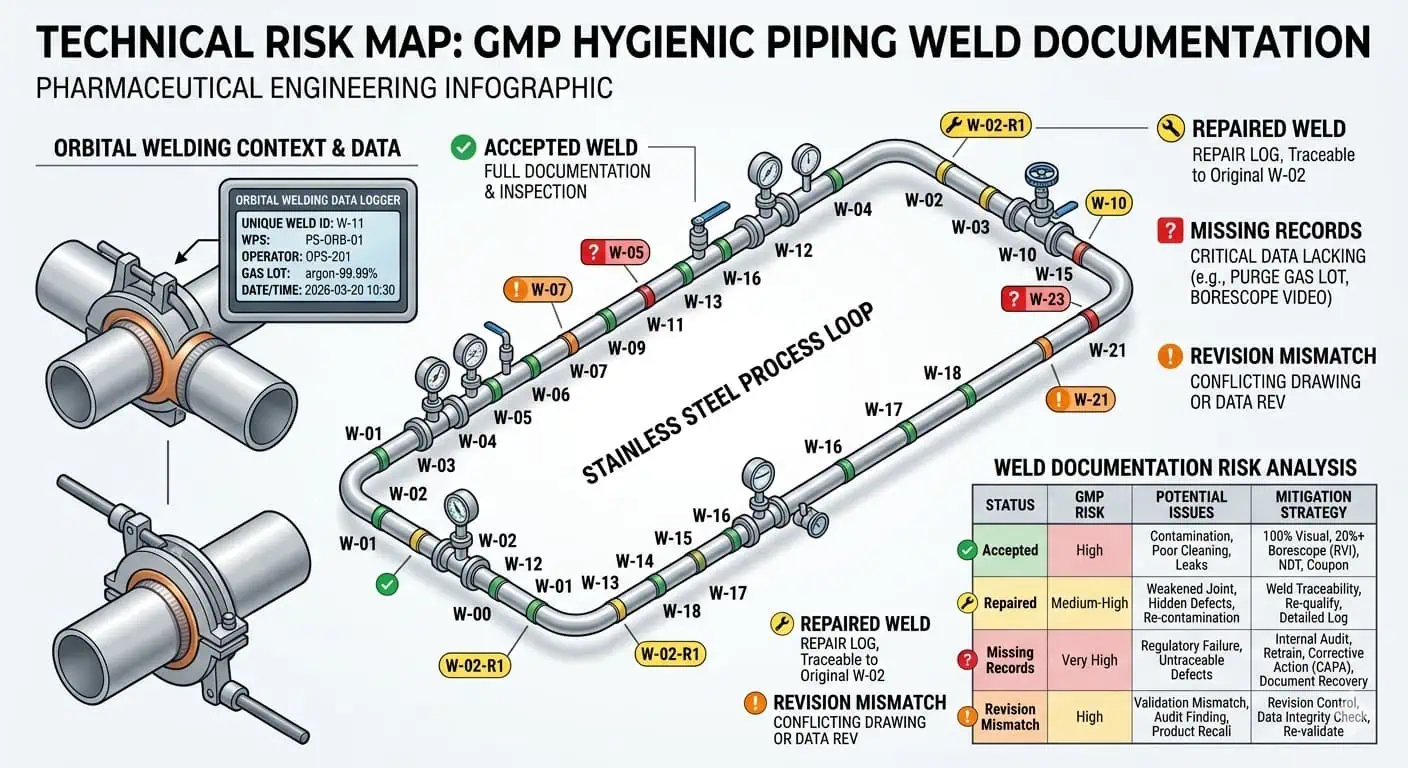
Expertenrat: Verwalten Sie Schweißaufzeichnungen nicht als reines Fertigungsdatenset. Verwalten Sie sie als Freigabedatenset, der auch nach Feldänderungen, Spool-Ersatz und endgültigem As-Built-Abschluss noch Sinn ergeben muss.
Oberflächenbeschaffenheit, Elektropolieren, Passivierung und zugehörige Aufzeichnungen
Anforderungen an die Beschaffenheit sind nur dann relevant, wenn das Projekt nachweisen kann, welche Beschaffenheit gefordert, welche geliefert und wie der endgültige benetzte Zustand erhalten wurde. In anspruchsvolleren GMP-Systemen ist die Entscheidung über die Beschaffenheit nicht von der Dokumentation getrennt. Wenn das Projekt zwischen Standard-316L und elektropoliertem 316L unterscheidet oder Passivierung und Nachbehandlungsnachweise erfordert, benötigen diese Anforderungen ihren eigenen Aufzeichnungspfad im Übergabedossier.
Typischer Branchenfall: Die Rohrqualität war akzeptabel, aber die Freigabediskussion verlagerte sich darauf, ob der endgültige Oberflächenzustand mehrerer produktberührender Rohrleitungsstücke nach der Fertigung und Nacharbeit noch den spezifizierten hygienischen Erwartungen entsprach. Die Legierung war nicht der Schwachpunkt. Die dokumentierte Beschaffenheit war es.
Expertenrat: Definieren Sie die beschaffenheitsbezogene Dokumentation vor Beginn der Fertigung. Wenn ein Projekt spät entscheidet, dass der Oberflächenzustand wichtiger ist als erwartet, sind die fehlenden Aufzeichnungen oft viel schwieriger nach der Fertigung wiederherzustellen als die Materialzertifikate.
Änderungsmarkierungen, As-Built-Zeichnungen und Feldänderungen
Feldänderungen sind der Punkt, an dem Rückverfolgbarkeitsketten am häufigsten unterbrochen werden. Ein Abzweig wird für den Zugang verlegt. Ein Rohrleitungsstück wird neu gefertigt, um der tatsächlichen Montage zu entsprechen. Ein Messpunkt wird überarbeitet. Eine Ventilausrichtung ändert sich. Keine dieser Aktionen ist automatisch fatal, aber jede birgt ein Dokumentationsrisiko, wenn der Prozess von Änderungsmarkierungen zu As-Built-Zeichnungen schwach ist. Eines der wichtigsten Dokumentationsprinzipien in der GMP-Praxis ist, dass Aufzeichnungen zum Zeitpunkt der Arbeit erstellt werden sollten. Das ist wichtig, weil rekonstruierte Aufzeichnungen fast immer schwächer sind als zeitgenössische.
Industriefall: Eine GMP-Skid-Anbindung wurde im Feld geändert, um die Verlegung und Wartungszugänglichkeit zu verbessern. Die Änderung selbst war vernünftig. Das Problem war, dass die aktualisierten Schweißreferenzen, Rohrleitungsreferenzen und As-Built-Zeichnungen hinter der Installation zurückblieben. Bei der Übergabe versuchte das Team, zwei technisch ähnliche, aber dokumentatorisch inkonsistente Versionen derselben Schleife in Einklang zu bringen.
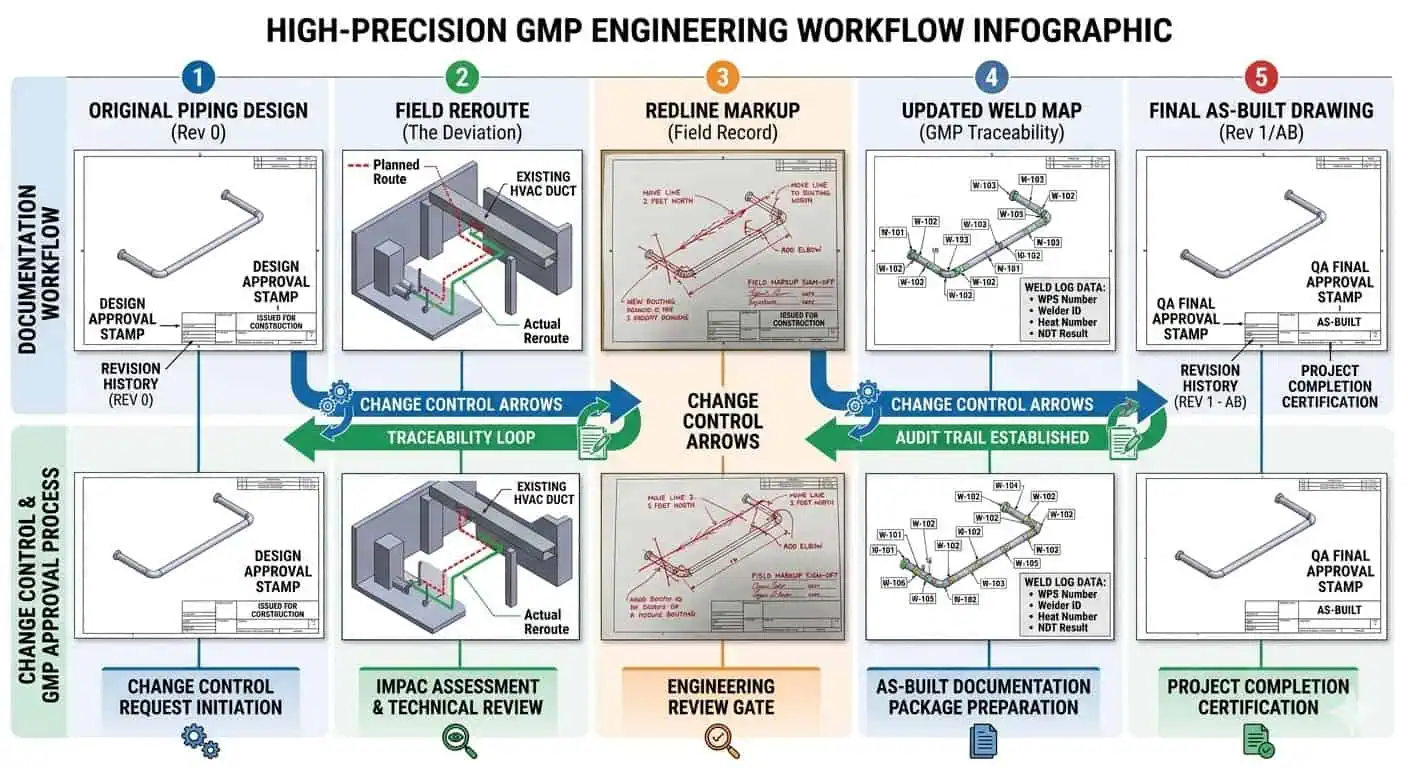
Expertenrat: Feldumleitungen sind nicht das eigentliche Problem. Unabgeschlossene Nachweise von Feldumleitungen sind das eigentliche Problem. Das Projekt sollte Rotstiftkorrekturen und as-built-Dokumente als aktive Steuerungsinstrumente behandeln, nicht als Endstufen-Zeichnungsaufgaben.
Das Kern-Dokumentationspaket, das GMP-Teams üblicherweise erwarten
Materialdokumentation
Materialdokumentation beweist, dass die genehmigten benetzten Materialien tatsächlich in das System eingebracht wurden. Mindestens bedeutet dies üblicherweise Materialzertifikate, Wärmenachverfolgbarkeit, Eingangskontrolle und eine Form der Standortkartierung, die installierte Komponenten mit dem genehmigten Materialdatensatz verknüpft. Je stärker die hygienischen oder produktkontaktbezogenen Konsequenzen sind, desto weniger akzeptabel wird es, diese Beziehung vage zu lassen.
Fertigungs- und Schweißdokumentation
Fertigungsdokumentation beweist, wie das System zu dem wurde, was es ist. Hier finden sich üblicherweise Schweißpläne, Orbital-Schweißprotokolle, Schweißprüfergebnisse, Reparaturverläufe, Boroskop-Aufzeichnungen, wo erforderlich, und Fertigungsstatusverfolgung. Der Sinn besteht nicht darin, einen dicken Dossier um seiner selbst willen zu erstellen. Der Sinn besteht darin, den installierten Kreislauf überprüfbar und technisch verteidigbar zu halten.
Oberflächen- und Behandlungsdokumentation
Oberflächenaufzeichnungen sind wichtig, wenn die Oberflächenbeschaffenheit oder Nachbehandlung Teil der hygienischen Anforderung ist. Wenn das Projekt Elektropolieren, Passivierung oder ein definiertes Oberflächenziel vorschreibt, sollte das Übergabepaket zeigen, wie diese Anforderung umgesetzt und wie die relevanten Teile identifiziert wurden. Andernfalls riskiert das Projekt, eine Oberflächenanforderung auf dem Papier zu haben, aber keine starken Beweise, dass die installierte Oberfläche noch damit übereinstimmt.
Prüfung und Übergabedokumentation
Prüf- und Übergabeaufzeichnungen verwandeln die Fertigungshistorie in Freigabebeweise. Druckprüfung, Leckprüfung, Inspektionsabschluss, Mängellistenabschluss und finale Dossierzusammenstellung sind die Punkte, an denen das Projekt demonstriert, dass die gefertigte Schleife nicht nur gebaut, sondern auch verifiziert und abgeschlossen wurde, um den GMP-Betrieb zu unterstützen.
Typischer Branchenfall: das Projekt hat alle einzelnen Aufzeichnungen irgendwo, aber die Übergabe stockt immer noch, weil das Paket nicht so strukturiert ist, wie die QA es zur Überprüfung und Freigabe der Schleife benötigt. Dies ist nicht nur ein Problem fehlender Dokumente. Es ist ein Dossier-Logik-Problem.

Expertenrat: wenn Übergabedokumente erst nach mechanischer Fertigstellung zum ersten Mal zusammengestellt werden, ist das Projekt aus dokumentenkontrollperspektive bereits verspätet.
Änderungskontrolle und Abweichungsaufzeichnungen
Änderungsdokumentation ist das, was die finale Beweiskette glaubwürdig hält. Das Projekt sollte in der Lage sein, anzuzeigen, was geändert wurde, wer es genehmigt hat, welche Inspektion oder Nacharbeit folgte und wie der endgültige Ist-Zustand diese Änderung aufgenommen hat. Ohne dies können selbst technisch sinnvolle Änderungen vor Ort unnötige QA-Zögern verursachen.
| Dokumentationssatz | Was es beweist | Wo es häufig versagt |
|---|---|---|
| Materialzertifikate und Rückverfolgbarkeitsmatrix | Die genehmigten benetzten Materialien wurden tatsächlich installiert | Die Standortzuordnung wird nach dem Schneiden oder der Neuverlegung vor Ort unklar |
| Schweißpläne und Schweißprotokolle | Die endgültigen Schweißnähte wurden unter Kontrolle abgeschlossen und inspiziert | Schweißnummern stimmen nicht mehr mit den endgültigen Rohrleitungssatz-Revisionen überein |
| Oberflächenbeschaffenheit / EP / Passivierungsprotokolle | Die spezifizierte Oberflächenbeschaffenheit wurde erreicht und erhalten | Nacharbeiten oder späte Fertigstellungsänderungen sind nicht vollständig dokumentiert |
| Rote Linien und As-Built-Zeichnungen | Die installierte Schleife entspricht der endgültig genehmigten Konfiguration | Feldänderungen erfolgen schneller als die Zeichnungsabschlüsse |
| Übergabedossier | Die vollständige Nachweiskette ist für die QA-Prüfung bereit | Protokolle existieren, aber nicht in einer freigabereifen Struktur |
Wo Dokumentationsketten typischerweise unterbrochen werden
Material war korrekt, aber die Rückverfolgbarkeitsmatrix war schwach
Eines der häufigsten Versäumnisse ist nicht fehlendes Material, sondern eine schwache Material-Standort-Zuordnung. Teams gehen manchmal davon aus, dass das Vorhandensein der Zertifikate ausreicht. Es reicht nicht aus, wenn das Projekt nicht schnell nachweisen kann, wo das zertifizierte Material nach dem Schneiden, der Fertigung, dem Spulen und der Änderung vor Ort gelandet ist.
Schweißnähte waren akzeptabel, aber der Schweißnachweis-Satz war unvollständig
Eine Schleife kann technisch einwandfrei sein und dennoch die Dokumentationsabschlussprüfung nicht bestehen, weil der Schweißnachweis-Satz unvollständig ist. Fehlender Schweißstatus, unklare Reparaturhistorie oder falsch ausgerichtete Schweißnummern verursachen meist mehr Verzögerung, als Teams erwarten. In GMP-Rohrleitungen ist der Schweißnachweis nicht nur ein Fertigungswerkzeug. Er ist Teil der Freigabebereitschaft.
Änderungen vor Ort erfolgten schneller als die Dokumentationsaktualisierung
Die Dokumentation hinkt dem Projekt oft genau in dem Moment hinterher, in dem das Projekt am dynamischsten wird. Änderungen der Leitungsführung in der Endphase, Überarbeitungen von Anschlüssen, Anpassungen der Montage vor Ort und hinzugefügte Abzweigungen erfolgen oft unter Termindruck. Wenn der Dokumentensatz nicht Schritt hält, wird das endgültige Übergabepaket zu einer Rekonstruktionsübung anstelle einer kontrollierten Übergabe.
Die kleinsten Komponenten verursachten das größte QA-Problem
Kleine benetzte Bauteile stellen ein unverhältnismäßiges Dokumentationsrisiko dar. Fittings, Probenkomponenten, Membranen, Dichtungen und instrumentbezogene benetzte Teile sind oft der Punkt, an dem die sauberste Nachweiskette zuerst bricht. Teams denken tendenziell in Rohrleitungsabschnitten, aber die Qualitätssicherung erlebt das Projekt oft in Form von ungelösten lokalen Baugruppen.
Erfahrung aus der Feldabschlussarbeit: Je lokaler und austauschbarer die Baugruppe ist, desto unsicherer ist die Annahme, dass ihre Aufzeichnungen sich von selbst erledigen.
Wie Ingenieure Dokumentationsanforderungen vor der Ausschreibung aufbauen sollten
Definieren, was rückverfolgbar sein muss
Vor der Ausschreibung definieren, welche benetzten Komponenten durch Installation und Übergabe rückverfolgbar bleiben müssen. Wenn nur Rohrleitungen kontrolliert werden und die kleineren benetzten Teile vage bleiben, ist die Nachweiskette normalerweise dort am schwächsten, wo die hygienische Baugruppe am komplexesten ist.
Definieren, was während der Fertigung aufgezeichnet werden muss
Projekte sollten definieren, was während der Arbeit aufgezeichnet werden muss, nicht nur was am Ende vorhanden sein muss. Schweißprotokolle, Inspektionspunkte, oberflächenbezogene Aufzeichnungen, Passivierungsnachweise, wo relevant, und Änderungsaktualisierungen vor Ort sollten Teil des definierten Projektablaufs sein.
Definieren Sie, was die QA bei der Übergabe erhalten muss
Das Übergabepaket sollte als Freigabedokument definiert werden, nicht als vage Sammlung von allem, was der Auftragnehmer später zusammenstellen kann. Wenn die QA eine spezifische Dossierstruktur, Rückverfolgbarkeitsmatrix oder Aufzeichnungsformat erwartet, sollte das Projekt dies definieren, solange noch Zeit besteht, diese Aufzeichnungen korrekt zu generieren.
Definieren Sie, was nach der Inbetriebnahme aufrechterhalten werden muss
Die Dokumentationskette sollte in den Betrieb übergehen, nicht bei der Übergabe enden. Geräteprotokolle, Wartungsaufzeichnungen, Rückverfolgbarkeit von Ersatzteilen und kontrollierte Aktualisierungen des installierten Systems sind alle Teil der Aufrechterhaltung der ursprünglichen Nachweiskette. Ein freigabefähiges System kann später viel schwerer zu verteidigen sein, wenn Lebenszyklusaufzeichnungen schwach sind.
Der beste Projektrat ist einfach: Definieren Sie die Nachweiskette vor der Beschaffung. Warten Sie nicht, bis die Fertigung im Gange ist, um zu entscheiden, ob Wärmerückverfolgbarkeit, Oberflächenaufzeichnungen, Schweißstatus oder Dokumentation von Änderungen vor Ort wichtig sind. Zu diesem Zeitpunkt sammelt das Projekt normalerweise Dokumente reaktiv, anstatt sie gezielt zu steuern. Dies ist eine der klarsten praktischen Lehren aus GMP-Übergabearbeiten: Projekte, die den Aufzeichnungssatz vor der Ausschreibung definieren, schließen normalerweise schneller und mit weniger QA-Überraschungen ab als Projekte, die ihn später rekonstruieren versuchen.
Wie dies mit Design, Material und Armaturenauswahl verbunden ist
Materialauswahl ohne Dokumentationskontrolle ist kein geschlossenes Risiko
Eine gute Materialentscheidung wird nur dann zu einer sicheren Projektentscheidung, wenn sie sauber dokumentiert ist. Für die umfassendere Materiallogik verknüpfen Sie diese Seite mit Pharmazeutische Hygienik-Rohrleitungsmaterialauswahl.
Oberflächenanforderungen sind nur dann relevant, wenn sie nachgewiesen sind
Elektropolieren, Oberflächenziele und Nachbehandlungserwartungen schließen das Risiko nicht, es sei denn, die Aufzeichnungen beweisen sie. Verknüpfen Sie dieses Thema mit Elektropolierter 316L vs. Standard 316L Edelstahl.
Fittings und Musterbaugruppen benötigen ihre eigene Nachweiskette
Je kleiner und lokaler die Baugruppe wird, desto wahrscheinlicher wird ihre Dokumentation zum schwächsten Teil des Übergabepakets. Verknüpfen Sie dieses Thema mit Auswahl von Hygienefittings für GMP-Anlagen.
Die As-Built-Dokumentation muss das tatsächliche Reinigungsrisiko widerspiegeln
Die Dokumentation sollte nicht nur beweisen, was installiert wurde. Sie sollte auch die endgültige lokale hygienische Realität des Systems widerspiegeln. Für diese Logik, verbinden Sie diese Seite mit CIP-Designüberlegungen für hygienische Rohrleitungen.
Häufige Fehler in der Dokumentation und Rückverfolgbarkeit für Pharma-Rohrleitungsprojekte
Dokumentation als Übergabeaktivität statt als Design-Input behandeln
Projekte, die das Dokumentationspaket spät definieren, enden oft damit, Aufzeichnungen unter Zeitdruck neu zu erstellen.
Rohrleitungen verfolgen, aber kleine benetzte Komponenten nicht verfolgen
Das schwächste Glied in der Rückverfolgbarkeit tritt oft bei Armaturen, Dichtungen, Membranen oder lokalen Probenbaugruppen auf.
Schweißdaten getrennt von der Freigabelogik auf Leitungsebene halten
Schweißaufzeichnungen sind viel weniger nützlich, wenn sie nicht klar auf die endgültig installierte Schleife und ihren Freigabestatus abgebildet werden.
Rote Linien von der installierten Realität abweichen lassen
Wenn Änderungen vor Ort schneller ablaufen als kontrollierte Aktualisierungen, wird das Übergabepaket schwerer zu vertrauen.
Annahme, dass die QA es später akzeptieren wird
In GMP-Rohrleitungen ist fehlende Nachweisführung selten einfacher am Ende des Projekts zu beheben als während der kontrollierten Ausführung.
Übermäßiges Sammeln von Dokumenten, aber unzureichende Definition dessen, was tatsächlich wichtig ist
Große Dokumentenmengen erzeugen nicht automatisch ein starkes Übergabepaket. Entscheidend ist, ob der Datensatz das installierte hygienische System klar genug für die Freigabe und spätere Lebenszykluskontrolle nachweist.
Praktische Checkliste: Was Sie fragen sollten, bevor Sie ein Pharma-Rohrleitungssystem freigeben
Vor Beginn der Fertigung
- Welche benetzten Komponenten müssen rückverfolgbar sein?
- Welche Aufzeichnungen müssen während der Fertigung erstellt werden?
- Welche Schweiß-, Oberflächen- und Prüfnachweise wird die QA später benötigen?
- Wie werden Änderungen vor Ort in kontrollierte Aufzeichnungen integriert?
Vor der mechanischen Fertigstellung
- Sind die Änderungsmarkierungen aktuell?
- Können installierte Komponenten eindeutig genehmigten Materialaufzeichnungen zugeordnet werden?
- Sind der Schweißstatus und die Reparaturhistorie abgeschlossen?
- Sind Abschluss- und Behandlungsaufzeichnungen dort vollständig, wo erforderlich?
Vor der QA-Freigabe
- Entspricht das Übergabepaket dem tatsächlich installierten Kreislauf?
- Sind lokale Baugruppen noch in Rückverfolgbarkeit oder Prüfaufzeichnungen ungeklärt?
- Kann das Projekt den endgültigen Ist-Zustand klar genug für die Freigabe nachweisen?
Nach Inbetriebnahme
- Wie werden Geräteprotokolle und Wartungsaufzeichnungen fortgeführt?
- Wie bleiben Ersatzteile rückverfolgbar?
- Wie werden zukünftige Änderungen mit der ursprünglichen Nachweiskette verknüpft?
| Projektphase | Schlüsseldokumentationsfrage | Wie gute Kontrolle aussieht |
|---|---|---|
| Vor der Angebotsanfrage | Was muss rückverfolgbar und lieferbar sein? | Der Aufzeichnungssatz ist definiert, nicht angenommen |
| Während der Fertigung | Werden Aufzeichnungen in Echtzeit erstellt? | Schweiß-, Material-, Oberflächen- und Änderungsaufzeichnungen bleiben aktuell |
| Vor der Übergabe | Entspricht das Dossier der installierten Realität? | As-built, Rückverfolgbarkeit und Inspektionsabschluss stimmen überein |
| Nach Inbetriebnahme | Wird die Beweiskette Lebenszyklusänderungen überstehen? | Wartungs- und Austauschaufzeichnungen bleiben unter Kontrolle |
Fazit: In Pharma-Rohrleitungen beweist die Dokumentation, dass das System, das Sie zu bauen glauben, das tatsächlich installierte System ist
Gute Dokumentation und Rückverfolgbarkeit schaffen nach dem Projekt keinen Mehrwert. Sie schützen das Projekt davor, genau in dem Moment, in dem es betriebsbereit sein sollte, nicht freigegeben werden zu können. In der Pharmarohrleitung ist das installierte System nur so akzeptabel wie die Nachweiskette, die belegt, dass sein Material, seine Herstellung, Oberflächenbeschaffenheit, Inspektion und Änderungen kontrolliert wurden.
Die stärksten Projekte versuchen nicht, diese Nachweiskette bei der Übergabe zu rekonstruieren. Sie definieren sie vor der Ausschreibung, pflegen sie während der Herstellung und schließen sie vor der Freigabe. Für das vollständige Pharma-Themencluster verbinden Sie diesen Artikel mit Pharmazeutische Hygienik-Rohrleitungsmaterialauswahl, Elektropolierter 316L vs. Standard 316L Edelstahl, Auswahl von Hygienefittings für GMP-Anlagenund CIP-Designüberlegungen für hygienische Rohrleitungen.
FAQ
Welche Dokumentation ist für Pharma-Rohrleitungsprojekte erforderlich?
Das genaue Paket hängt vom Projektumfang ab, aber sie umfasst in der Regel Materialzertifikate, Rückverfolgbarkeitsaufzeichnungen, Schweißdokumentation, Inspektionsprotokolle, Nachweise für Oberflächenbeschaffenheit oder Behandlung, wo erforderlich, Änderungszeichnungen, As-built-Dokumente und Übergabeprotokolle, die die QA-Freigabe unterstützen.
Welche Rückverfolgbarkeit ist in GMP-Rohrleitungen erforderlich?
Die Rückverfolgbarkeit sollte dem benetzten Pfad folgen. Das bedeutet oft, dass Rohre, Fittings, Ventile, lokale Baugruppen und andere kritische produktberührende Komponente bis zu genehmigten Aufzeichnungen rückverfolgbar sein müssen, die noch mit dem installierten Zustand übereinstimmen.
Warum scheitern Pharma-Rohrleitungsprojekte bei der Übergabe?
Sie scheitern oft, weil die Nachweiskette unvollständig ist. Die Installation kann physisch akzeptabel sein, aber fehlende oder schwache Material-, Schweiß-, Oberflächen- oder As-built-Aufzeichnungen können die QA-Freigabe dennoch verzögern.
Benötigen Armaturen und Dichtungen Rückverfolgbarkeit in GMP-Projekten?
In vielen kritischen hygienischen Anwendungen, ja. Kleinere benetzte Komponenten sind oft der schwächste Glied in der Dokumentation, daher sollten sie nicht als beiläufige Verbrauchsmaterialien behandelt werden, wenn sie die hygienische Leistung oder das Freigaberisiko beeinflussen.
Sind Schweißprotokolle für pharmazeutische Hygienikrohrleitungen erforderlich?
Projekte stützen sich häufig auf Schweißpläne und Schweißdokumentation, da sie zentral für den Nachweis des Herstellungs- und Inspektionsstatus sind. Das genaue Format variiert je nach Projekt, aber eine schwache Schweißdokumentation ist eines der häufigsten Übergabeprobleme.
Was ist der Unterschied zwischen As-Built-Dokumenten und Übergabedokumenten?
As-built-Aufzeichnungen zeigen die endgültige installierte Konfiguration. Übergabedokumente sind das umfassendere Nachweispaket, das zur Freigabe verwendet wird, einschließlich Rückverfolgbarkeit, Inspektion, Prüfung und zugehöriger Projektaufzeichnungen.



