
El diseño de tuberías de alta pureza para instalaciones biotecnológicas no es solo un ejercicio de trazado. Es una decisión de control de contaminación, limpieza, soldabilidad, drenabilidad y validación. En la fabricación biotecnológica, un sistema de tuberías hace más que mover fluido de un recipiente a otro. Debe proteger la integridad del proceso, soportar limpieza y esterilización repetibles, minimizar el riesgo microbiano y de residuos, permanecer inspeccionable después de la fabricación y resistir la carga de documentación y calificación de un entorno regulado.
Por eso, un buen diseño de tuberías de alta pureza comienza con la geometría, no con la apariencia. Un sistema puede parecer higiénico en un P&ID y aún fallar en operación si el diseño de ramales crea tramos muertos, la pendiente no drena como se instaló, la estrategia de soldadura es poco realista, o las válvulas locales y ensamblajes de muestreo son más difíciles de limpiar que la línea principal. En instalaciones biotecnológicas, el detalle higiénico más débil suele importar más que el tramo recto más limpio.
Esta guía explica cómo los ingenieros diseñan tuberías de alta pureza para instalaciones biotecnológicas, donde las decisiones sobre 316L y acabado superficial realmente importan, cómo el control de tramos muertos y la drenabilidad dan forma al diseño, por qué el diseño de soldadura no puede separarse del diseño de tuberías, y cómo las expectativas de mantenimiento y validación deben integrarse en el sistema antes de que comience la fabricación.
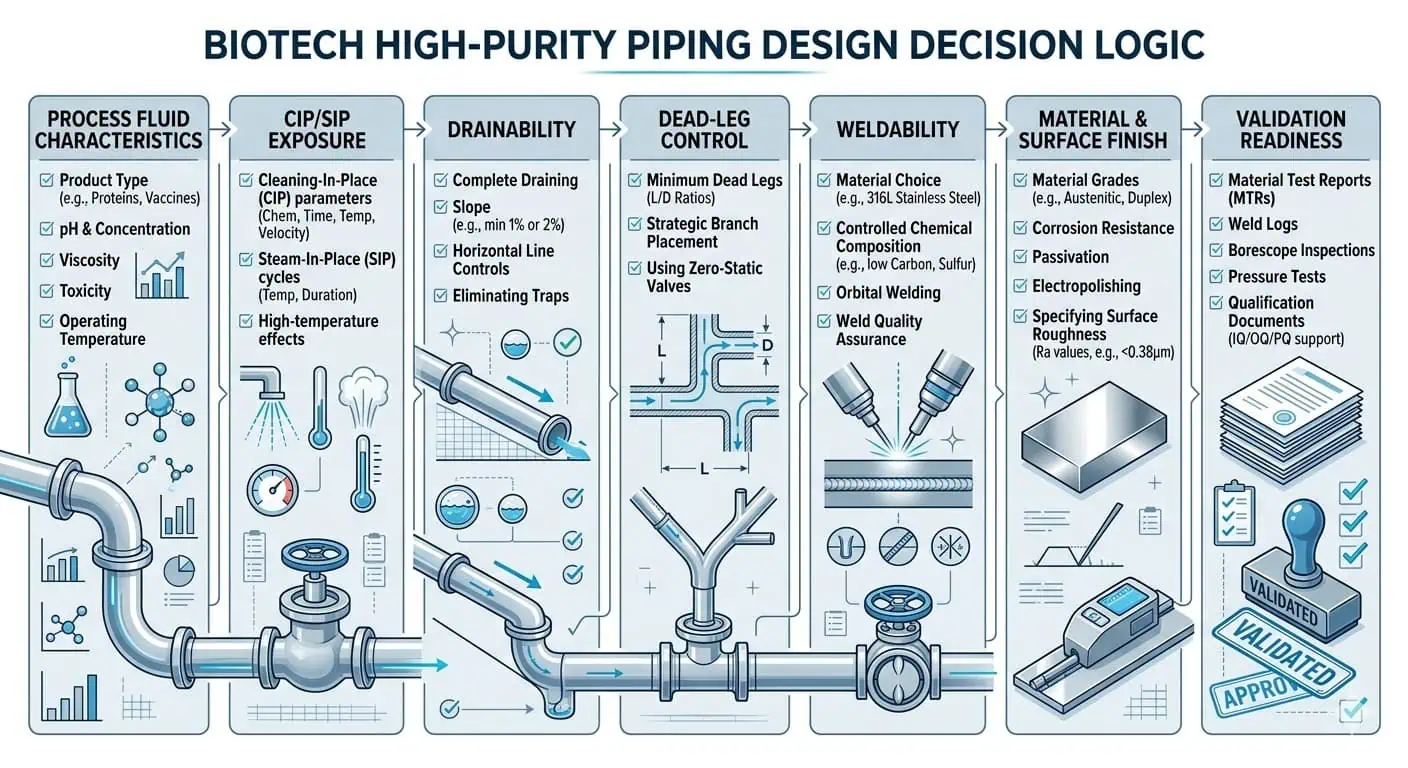
Lo que realmente significa el diseño de tuberías de alta pureza en instalaciones biotecnológicas
El diseño de alta pureza es una decisión de control de contaminación
En sistemas biotecnológicos, el diseño de tuberías es parte del control de contaminación. ASME BPE es útil aquí porque no trata los materiales, requisitos de superficie, diseño para limpieza y esterilidad, fabricación, examen, inspección, pruebas y certificación como temas aislados. Los trata como un marco de ingeniería higiénica conectado. Normas de equipos de la FDA apuntan en la misma dirección: el equipo debe estar diseñado apropiadamente, las superficies en contacto con el producto deben ser no reactivas, no aditivas y no absorbentes, y el equipo debe ser limpiable y mantenible bajo control documentado.
Realidad típica de la ingeniería: el bucle de tuberías que causa más problemas rara vez es la línea principal entre recipientes. Suele ser más a menudo la rama de muestreo, la T de instrumentación, el punto de distribución o el colector local que se trató como un detalle menor durante el diseño. En trabajos de biotecnología, la pregunta de diseño nunca es solo “¿Transferirá este fluido?” Es “¿Seguirá siendo este conjunto limpiable, drenable, inspeccionable y defendible después de la fabricación y validación?”
Consejo experto: si la revisión de diseño se centra solo en el caudal, la caída de presión y el trazado de líneas, sigue siendo incompleta para un sistema de biotecnología de alta pureza. El diseño debe revisarse a través del lente del fallo higiénico, no solo del flujo del proceso.
Por qué las instalaciones de biotecnología necesitan más que prácticas generales de tuberías de grado alimentario
Las instalaciones de biotecnología suelen imponer demandas más estrictas en las tuberías que el servicio higiénico general. La consecuencia de la retención de residuos, la contaminación microbiana, la mala respuesta del vapor limpio o el cambio de campo no documentado es mayor. En muchas instalaciones de biotecnología, el sistema de tuberías no se juzga solo por si opera de manera segura. Se juzga por si puede respaldar la calificación, la verificación de limpieza, el historial de mantenimiento, el control de cambios y la consistencia del proceso a largo plazo.
Caso típico de la industria: un concepto de diseño que funciona aceptablemente en una planta higiénica general aún puede ser rechazado en un proyecto de biotecnología porque la disposición de la rama local, la condición de la superficie o la carga de documentación es más difícil de defender en un entorno centrado en la validación. El problema no es que la biotecnología use una física completamente diferente. El problema es que la tolerancia al comportamiento higiénico ambiguo es mucho menor.
Un sistema de alta pureza debe funcionar higiénicamente, no solo parecer higiénico
El hardware de aspecto higiénico no crea automáticamente un sistema de alta pureza. Un tubo pulido, una férula higiénica o una tapa de soldadura de aspecto limpio no prueban que el sistema instalado drene correctamente, que la geometría de la rama sea aceptable o que el ensamblaje local más difícil se limpie de manera confiable en su lugar. El diseño de tuberías biotecnológicas tiene éxito cuando la geometría local y las prácticas de fabricación respaldan la intención higiénica de la especificación.
Esa es la razón por la que este artículo debe leerse junto con Selección de Conexiones de Grado Alimentario para Sistemas de Fermentación. El ensamblaje local incorrecto puede anular un diseño de sistema por lo demás sólido.
Comience con el Proceso Real: Fluido, Limpieza y Carga de Validación
Las Características del Fluido del Proceso Cambian el Diseño
Diferentes fluidos biotecnológicos crean diferentes cargas de diseño higiénico. Las soluciones tampón, medios, intermedios de producto, corrientes de cosecha, servicios relacionados con WFI, productos químicos CIP, vapor SIP y fluidos higiénicos relacionados con servicios públicos no se comportan de la misma manera en las tuberías. Algunos desafían el margen de corrosión. Algunos desafían la compatibilidad del sello. Algunos hacen que el diseño de puntos muertos y puntos de muestreo sea más sensible porque el comportamiento de los residuos o las consecuencias microbianas son mayores.
Conclusión técnica: Un buen diseño de tuberías comienza con el proceso real y los medios de limpieza, no con un estándar de tubería predeterminado. Si el equipo de diseño no puede describir claramente qué transportará la línea, qué temperaturas experimentará y cómo se limpiará o esterilizará, es demasiado pronto para finalizar los detalles de la tubería.
CIP, SIP y la Exposición Térmico-Química Son Entradas de Diseño
La limpieza y esterilización no son detalles operativos añadidos posteriormente. Son entradas de diseño. FDA 21 CFR 211.67 requiere que el equipo sea limpiado, mantenido y, cuando corresponda, higienizado y/o esterilizado bajo procedimientos controlados. En el diseño práctico de tuberías, eso significa que el sistema debe diseñarse para el régimen térmico y químico real al que estará expuesto. La exposición a vapor limpio, WFI caliente, cáustico, ácido, higienizante, enfriamiento y ciclos térmicos repetidos afectan qué materiales, sellos, soldaduras y accesorios locales sobrevivirán de manera confiable.
Caso típico de la industria: una línea fue dimensionada y enrutada correctamente para la transferencia del proceso, pero la exposición repetida a SIP reveló posteriormente debilidades en las interfaces de sellado local y orientaciones de válvulas difíciles de drenar. El problema no era que el flujo del proceso fuera incorrecto. El problema era que el entorno de limpieza y esterilización no había sido tratado como parte de la base de diseño original.
Consejo experto: si un ensamblaje local no sobreviviría a su exposición real a CIP/SIP sin precaución especial, entonces el problema está relacionado con el diseño incluso si la línea principal aún parece aceptable.
La Carga de Validación Cambia lo que Significa “Buen Diseño”
En instalaciones de biotecnología, el diseño se juzga en parte por qué tan bien el sistema puede validarse y mantenerse bajo control de cambios. Una línea que es operable pero difícil de inspeccionar, documentar o defender durante la calificación no es un diseño de alta pureza robusto. Por eso los ingenieros experimentados preguntan desde el principio: ¿dónde están los ensamblajes locales de mayor riesgo, cómo se inspeccionarán y qué evidencia se necesitará después de la fabricación y puesta en marcha?
Para el aspecto del ciclo de vida de esta lógica, conecte este artículo con Consideraciones de Mantenimiento y Validación para Tuberías de Grado Alimentario.
Los Principios de Diseño Centrales que Deciden si el Sistema Tendrá Éxito
Capacidad de drenaje
El drenaje verdadero es uno de los primeros requisitos de diseño en un sistema de tuberías de alta pureza. El líquido residual después de la limpieza o vaporización no es solo una molestia de mantenimiento. Cambia el comportamiento higiénico del siguiente ciclo, aumenta el riesgo de contaminación local, complica el secado y hace que la resolución de problemas sea menos confiable. Preguntas y respuestas sobre equipos de la FDA vincula el diseño del equipo, la limpieza, el mantenimiento y la idoneidad de las superficies en contacto con el producto, que es exactamente cómo debe juzgarse la capacidad de drenaje en un circuito de biotecnología.
Caso típico de la industria: el dibujo de diseño mostraba una línea de drenaje, pero después de ajustar los soportes en campo, un tramo instalado creó un punto bajo sutil que retenía líquido repetidamente después del CIP. El problema no apareció en el modelo de proceso principal. Apareció en la geometría instalada.
Consejo experto: nunca asuma la capacidad de drenaje solo por la intención del dibujo. Revise la pendiente, el espaciado de soportes, la orientación del cuerpo de la válvula, la ubicación del punto de drenaje y el comportamiento instalado final en conjunto.
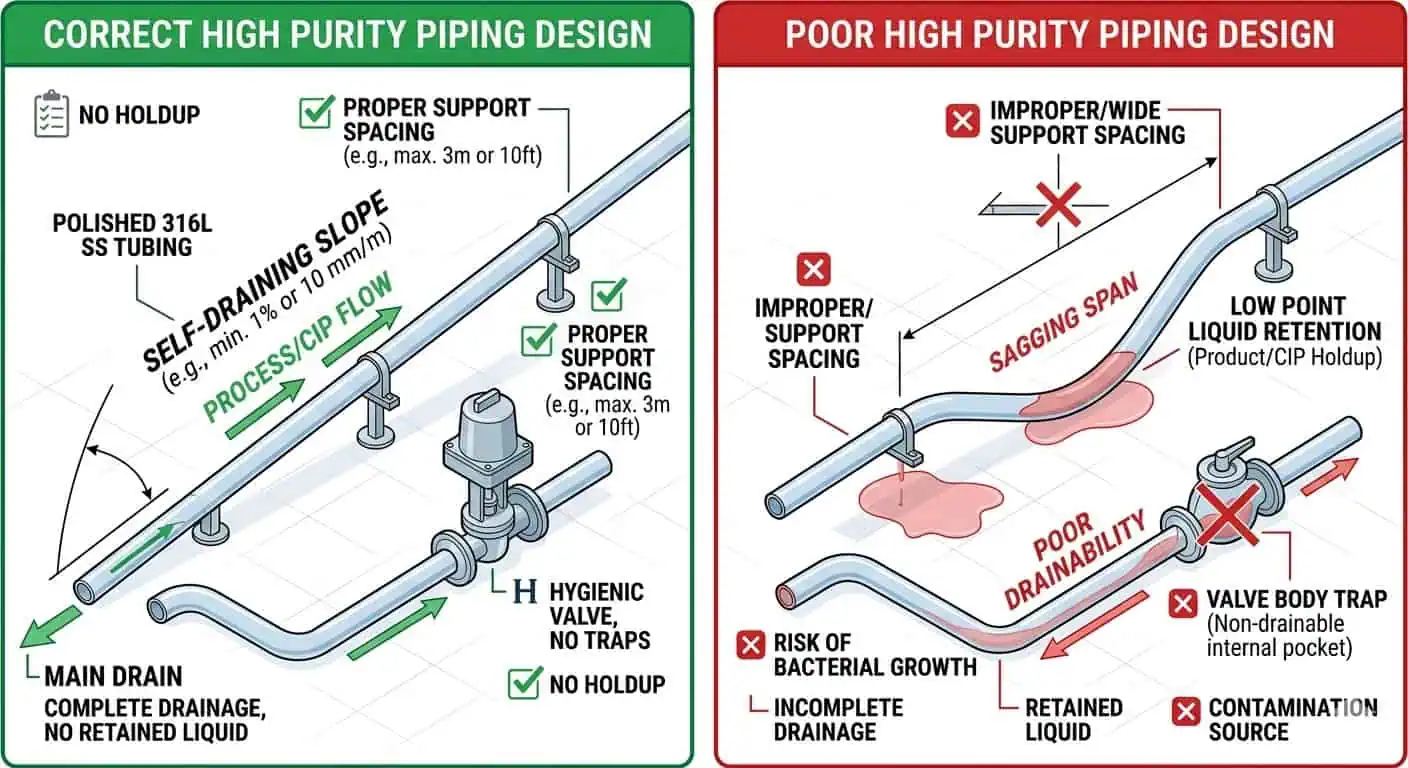
Control de Puntos Muertos
El control de puntos muertos sigue siendo una de las partes más importantes y más subestimadas del diseño de tuberías de alta pureza. Una línea puede estar hecha del material correcto, tener el acabado adecuado y aún así ser difícil de limpiar si el diseño de la rama crea zonas estancadas. Las tomas de muestra, las tes de instrumentos, los colectores locales y las ramas añadidas son donde este problema aparece con mayor frecuencia.
Caso típico de la industria: el circuito principal cumplió repetidamente los objetivos de operación y limpieza, pero una rama de muestra continuó generando preocupación higiénica. La causa raíz no fue la concentración de detergente o el tiempo del ciclo. Fue el débil intercambio de fluido local en una rama que nunca había sido revisada críticamente como parte del diseño CIP/SIP.
Consejo experto: evalúe la derivación local más difícil, no la sección recta más fácil. Si un conjunto local no puede intercambiar fluido y drenar de manera confiable, ese es el diseño que importa.
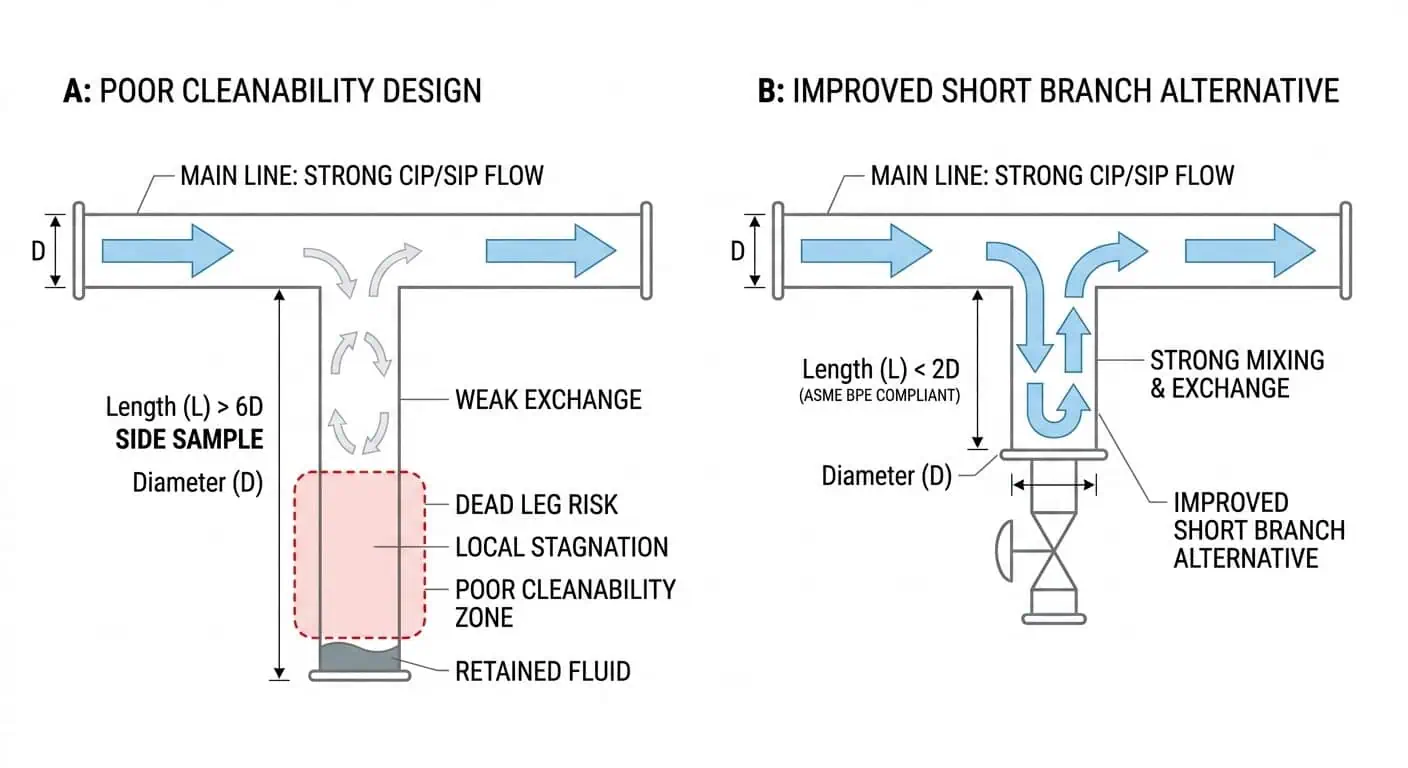
Trayectoria de Flujo Limpiable
Una línea que transfiere bien el producto no se limpia automáticamente bien. El flujo de producción y el flujo de limpieza están relacionados pero no son problemas de diseño idénticos. En sistemas de alta pureza, la ruta principal del proceso puede ser hidráulicamente aceptable mientras que un ensamblaje local aún se convierte en el punto débil porque su trayectoria interna, orientación o configuración de rama impide una acción de limpieza efectiva.
Lógica de diseño basada en investigación: Resumen del alcance de ASME BPE vincula directamente los requisitos de superficie, el diseño para limpiabilidad y esterilidad, la fabricación de componentes, la fabricación incluyendo la unión de materiales, tuberías, exámenes, inspecciones, pruebas y certificaciones. Eso importa porque refuerza una verdad de ingeniería práctica: la limpiabilidad no es solo una configuración química. Está diseñada en la trayectoria mojada.
Acceso de Inspección e Intervención Controlada
No todas las ubicaciones deben diseñarse para apertura rutinaria, y no todas las ubicaciones deben cerrarse permanentemente sin una buena razón. Los sistemas de alta pureza necesitan un equilibrio controlado entre minimizar interfaces y permitir acceso justificado donde los sellos, diafragmas o ensamblajes locales necesitarán atención durante su ciclo de vida. Este es uno de los compromisos de diseño más importantes en tuberías biotecnológicas, porque cada interfaz de desmontaje agregada puede mejorar el acceso mientras también aumenta el riesgo higiénico relacionado con sellos.
Materiales y Requisitos de Superficie en Tuberías Biotecnológicas de Alta Pureza
Por qué el 316L es comúnmente la línea base
El 316L se usa comúnmente en tuberías de biotecnología de alta pureza porque proporciona un equilibrio práctico de margen de corrosión, soldabilidad y aceptación de la industria para servicio higiénico crítico. Eso no lo convierte en la solución a cada problema de proceso, pero sí explica por qué muchos proyectos lo tratan como el material metálico de línea base para servicio crítico de contacto con productos y alta pureza. ASME BPE cubre los requisitos de materiales y superficie dentro del marco de diseño higiénico más amplio, que es exactamente cómo los ingenieros deben evaluar el 316L en la práctica.
Para la discusión completa del lado de materiales, conecte este artículo con Acero Inoxidable 316L en Aplicaciones de Bioprocesos.
El acabado superficial es una variable de rendimiento higiénico
El acabado superficial no es una elección cosmética en tuberías de biotecnología. Afecta la limpiabilidad local, la confianza en la inspección y el comportamiento práctico de las superficies de contacto con productos después de la fabricación. La pregunta clave de diseño no es si un acabado suena “más premium”. Es si el acabado elegido respalda el objetivo higiénico del proceso y las expectativas de inspección de la instalación.
Caso típico de la industria: la aleación era aceptable, pero el proyecto revisó posteriormente el requisito de acabado porque la expectativa de superficie original ya no coincidía con la limpiabilidad y la carga de inspección del área de proceso final. La lección no fue que la familia de metales estaba equivocada. La lección fue que el acabado no se había definido con suficiente disciplina específica del proceso.
Punto de hecho: ASTM A270 explicitly states that pharmaceutical quality may be requested as a supplementary requirement, which is a useful reminder that tubing decisions in higher-purity projects often go beyond generic sanitary tubing supply.
Las Partes Mojadas No Metálicas También Importan
El diseño de tuberías de alta pureza no se detiene en la pared del tubo de acero inoxidable. Las juntas, diafragmas, asientos de válvulas, mangueras y otras partes mojadas no metálicas a menudo se convierten en el primer punto débil en la limpieza, exposición al vapor o confiabilidad del ciclo de vida. En muchas desviaciones del proyecto, el acero inoxidable era aceptable, pero la estrategia local de elastómero o polímero no se controló lo suficientemente ajustada para el proceso real y el régimen de esterilización.
Consejo experto: si el equipo de diseño está debatiendo la elección de aleación pero no ha definido la compatibilidad del sello y la lógica de reemplazo, la revisión de diseño higiénico aún está incompleta.
Construcción Soldada, Soldadura Orbital y Realidad de Fabricación
El Diseño de Tuberías No Puede Separarse del Diseño de Soldadura
En un sistema de biotecnología de alta pureza, la soldabilidad es parte del diseño, no una idea posterior de fabricación. Cuanto más depende un sistema de la calidad controlada de la soldadura para el rendimiento higiénico, más irreal se vuelve finalizar el enrutamiento y la lógica de ramificación sin considerar cómo se harán, purgarán, inspeccionarán y documentarán realmente las soldaduras.
Caso típico de ingeniería: el material y la ruta eran aceptables en papel, pero un ensamblaje local se volvió difícil de defender porque el acceso a la soldadura, la calidad de purga y la practicidad de inspección no se habían considerado cuando se diseñó inicialmente la disposición de la ramificación. La debilidad no comenzó solo en la fabricación. Comenzó en el diseño.
¿Por qué Importa la Lógica de Soldadura Orbital?
La lógica de soldadura orbital importa en biotecnología no porque suene más avanzada, sino porque la repetibilidad, la controlabilidad y la documentación importan más en servicio de alta pureza. En la práctica, los ingenieros deben pensar si un diseño propuesto soporta una ejecución de soldadura confiable, condiciones de purga repetibles y acceso de inspección en las ubicaciones exactas que más importarán posteriormente a QA y mantenimiento.
Consejo experto: Durante la revisión de diseño, siempre pregunte si la línea es simplemente dibujable o realmente soldable bajo condiciones controladas de alta pureza.
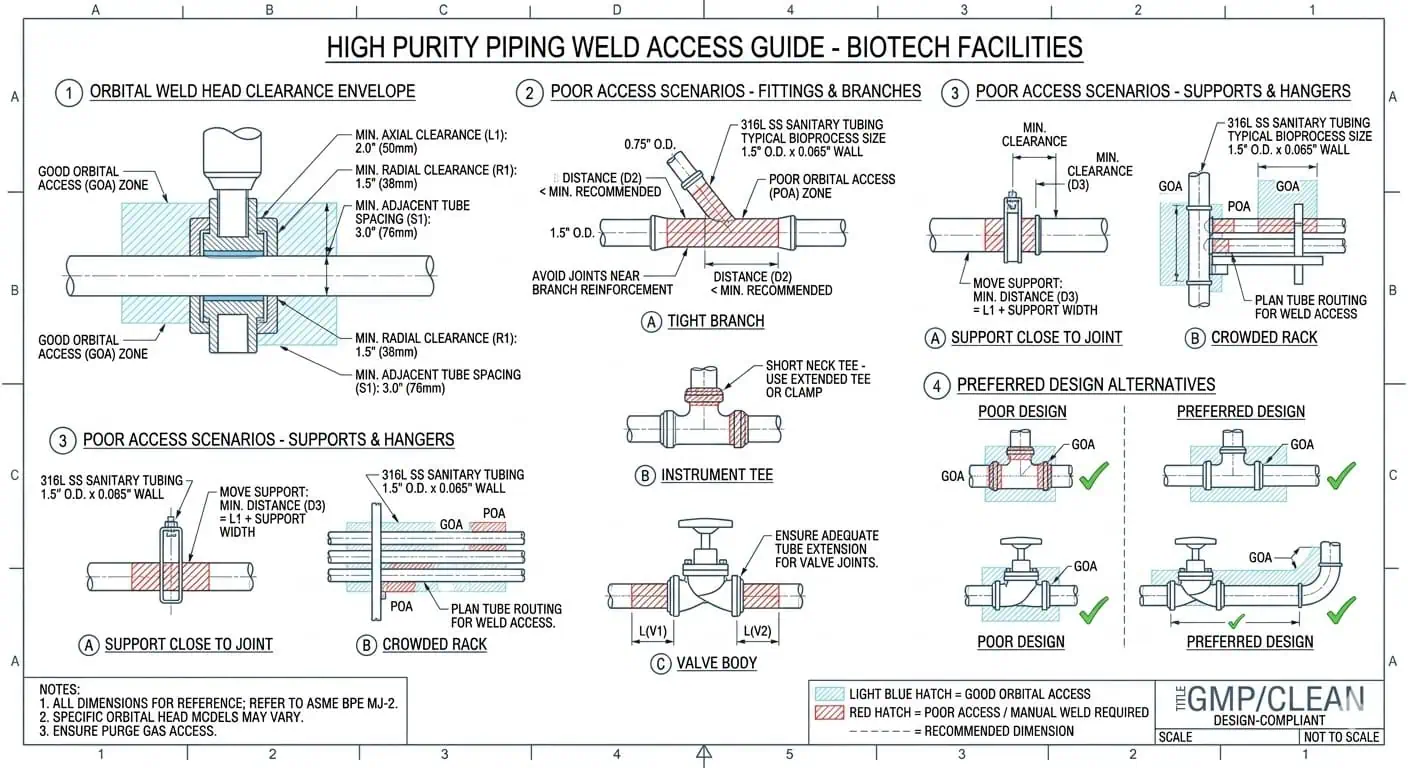
El Material Base Suele Ser Correcto, pero la Zona de Soldadura Se Convierte en el Punto Débil
Una de las fallas más realistas en tuberías de biotecnología es un sistema donde el material seleccionado era correcto, pero la condición adyacente a la soldadura se convirtió en el punto débil higiénico. Cuando eso sucede, los equipos a veces se enfocan excesivamente en la mejora de materiales cuando el problema real es la ejecución de la soldadura, el control de acabado local o la geometría original del ensamble. La lección de ingeniería es directa: una aleación correcta no puede rescatar una zona de soldadura higiénica inconsistente.
Válvulas, Ramales, Puntos de Muestreo y Ensambles Locales
Diseño de Puntos de Muestreo
Los puntos de muestreo son pequeños en tamaño pero de gran consecuencia. Combinan geometría de ramificación, interacción del operador, número de sellos, riesgo local de intercambio de fluidos y repetido escrutinio higiénico. Por eso, el diseño de puntos de muestreo merece más atención de ingeniería de lo que su huella sugiere. En muchas instalaciones de biotecnología, la pregunta higiénica más repetida no es sobre la línea principal de transferencia. Es sobre el conjunto local de muestreo.
Caso típico de la industria: un bucle principal funcionó aceptablemente, pero la misma ubicación de muestreo desencadenó repetidamente revisiones adicionales porque el conjunto atrapó fluido y nunca intercambió medios de limpieza tan efectivamente como el circuito principal.
Colectores de Válvulas y Áreas de Alta Densidad de Ramificaciones
Los grupos de válvulas y colectores de alta densidad de ramificaciones son donde los buenos diseños de alta pureza a menudo se vuelven frágiles. El problema no es que las válvulas sean malas. El problema es que las válvulas, ramificaciones, sellos e instrumentación multiplican la complejidad higiénica local. A medida que aumenta la complejidad local, el diseño necesita un control más fuerte sobre el drenaje, la densidad de soldaduras, las interfaces de sellado y la lógica de inspección.
Tees de Instrumentación y Conexiones de Sensores
Los tees de instrumentación y accesorios de sensores a menudo se subestiman porque son pequeños, pero pueden dominar el riesgo local de limpieza. Si el equipo de diseño no los trata como conjuntos locales críticos, a menudo se convierten en la ubicación donde la retención de residuos, el estancamiento local o la discrepancia en la documentación se hacen visibles por primera vez.
Consejo experto: diseñe el conjunto local que es más difícil de limpiar y más fácil de pasar por alto. Eso es generalmente donde reside el riesgo real del sistema.
Estrategia de Conexión: Soldada Versus Tipo Abrazadera Versus Acceso Controlado
Donde Se Prefieren Conexiones Soldadas Más Permanentes
Las conexiones soldadas más permanentes suelen ser la opción más segura donde la consecuencia higiénica es alta y no se necesita acceso rutinario. En áreas estables de contacto con producto, reducir el número de interfaces puede disminuir la variabilidad relacionada con sellos y eliminar una capa de riesgo de ensamblaje local. Esto no hace que la soldadura sea automáticamente mejor en todas partes. Significa que la unión permanente a menudo se vuelve preferible donde la ubicación no se beneficia lo suficiente de la apertura repetida para justificar la interfaz adicional.
Donde el Acceso Higiénico Tipo Abrazadera Todavía Tiene Sentido
Las conexiones de ajuste por abrazadera todavía tienen sentido donde el acceso controlado, el reemplazo de juntas o el cambio modular es un requisito real del ciclo de vida. El error no es usar conexiones de abrazadera en absoluto. El error es colocarlas en ubicaciones de alta consecuencia sin reconocer la carga adicional de control de sellos que crean.
Para la lógica local del lado del accesorio, conecte este artículo con Selección de Conexiones de Grado Alimentario para Sistemas de Fermentación.
La Mejor Pregunta No Es “¿Qué Conexión Es Mejor?”
La mejor pregunta es si la ubicación se beneficia más del acceso o de la reducción del número de interfaces. Ese es el verdadero compromiso de ingeniería. Un estilo de conexión que es excelente en un área puede convertirse en la respuesta incorrecta en otro lugar si introduce un control de sellado innecesario, una carga adicional de limpieza o una intervención de mantenimiento excesiva en una zona de alta pureza.
Diseñar para Mantenimiento y Validación desde el Primer Día
Un Buen Diseño es Más Fácil de Mantener
El sistema de tuberías de alta pureza más fácil de mantener es aquel cuyos riesgos higiénicos locales se redujeron durante el diseño en lugar de delegarse al mantenimiento posteriormente. Un drenaje deficiente, un acceso incómodo a los sellos, válvulas mal orientadas y ensamblajes locales difíciles de inspeccionar se convierten en cargas de mantenimiento después de la puesta en marcha. Son más fáciles de corregir en un dibujo que en una instalación biotecnológica en funcionamiento.
Para el lado del ciclo de vida, conecte este artículo con Consideraciones de Mantenimiento y Validación para Tuberías de Grado Alimentario.
La Validación Comienza en el Diseño
La validación no comienza después de la instalación. Comienza cuando el equipo de diseño decide lo que el sistema debe poder demostrar. Si la línea necesitará pruebas sólidas de limpieza, inspección o geometría local controlada, entonces esos requisitos ya deben ser visibles en el diseño. Los sistemas que son operables pero difíciles de validar suelen revelar que el equipo de diseño trató la lógica de calificación demasiado tarde en el proyecto.
Caso típico de la industria: un bucle de tuberías fue mecánicamente exitoso, pero la calificación tomó más tiempo de lo esperado porque los ensamblajes locales más difíciles de limpiar no se habían identificado claramente durante el diseño. La solución técnica fue menor. El impacto en el cronograma no lo fue.
Documentación y Trazabilidad Deben Ser Anticipadas en el Diseño
Un diseño de alta pureza también necesita una cadena de evidencia realista. La identidad del material, los registros de soldadura, las expectativas de acabado y los cambios en campo se vuelven mucho más difíciles de cerrar si el diseño nunca definió cómo se documentaría y liberaría el sistema final. Es por eso que el diseño de tuberías de alta pureza también debe conectarse con la lógica de entrega y trazabilidad del proyecto.
Errores Comunes de Diseño en Tuberías de Alta Pureza para Biotecnología
Diseñar para el Flujo del Producto pero No para el Flujo de Limpieza
Un circuito puede transferir el fluido del proceso bien y aún así tener un rendimiento inferior durante la limpieza si los ensamblajes locales nunca intercambian el medio de limpieza de manera suficientemente efectiva.
Aceptar Diseños de Apariencia Grado Alimentario Sin Verificar Puntos Muertos
La apariencia no reemplaza la revisión local de ramas. El comportamiento de puntos muertos a menudo se esconde en pequeños ensamblajes, no en la ruta principal.
Enfocarse Demasiado en el 316L Mientras se Ignoran las Soldaduras y la Geometría
Una aleación más fuerte no corrige una ejecución deficiente de soldadura, un drenaje deficiente o una geometría de rama difícil.
Utilizando una única lógica de diseño en todas las áreas de proceso
Las líneas de contacto con productos de alta consecuencia, ramales de muestreo, servicios higiénicos relacionados con servicios auxiliares y áreas de menor riesgo no deben diseñarse todas bajo un estándar indiferenciado.
Dejar las preguntas de validación y documentación hasta etapas tardías del proyecto
Si el sistema solo comienza a pensar en evidencia, trazabilidad y calificación después de la fabricación, el proyecto ya está operando con menos control del que debería.
Lista de verificación de diseño práctico para tuberías de alta pureza en instalaciones biotecnológicas
Antes de la congelación del P&ID
- Definir los medios reales de proceso y limpieza.
- Identificar los ensamblajes locales de mayor riesgo.
- Decidir dónde el sistema necesita acceso y dónde necesita menos interfaces.
- Definir la carga higiénica y de validación de cada área de proceso principal.
Antes del Enrutamiento Detallado
- Revisar la capacidad de drenaje, la lógica de pendiente y el riesgo de puntos bajos.
- Verificar la longitud de la rama, la dirección de salida y el potencial de tramos muertos locales.
- Revisar las orientaciones de válvulas y puntos de muestreo como conjuntos instalados, no solo como símbolos.
- Confirmar el acceso para soldadura y la practicidad de purga en ubicaciones críticas.
Antes de la Fabricación
- Definir juntos los requisitos de material, acabado y sellado.
- Alinear el enrutamiento con una estrategia de soldadura realista y lógica de inspección.
- Identificar los conjuntos que necesitarán una revisión higiénica más estricta después de la fabricación.
- Asegurarse de que la cadena de documentación sea compatible con la intención de diseño final.
Antes del Arranque y Calificación
- Confirmar que el circuito instalado aún drena según lo previsto.
- Revisar los ensambles locales más difíciles de limpiar, no solo la línea principal.
- Confirmar que los cambios en campo no introdujeron nuevos puntos débiles de grado alimentario.
- Verificar que el sistema final aún respalda el enfoque de validación y mantenimiento previsto.
| Tema de Diseño | Cómo se Ve un Buen Diseño | Lo que Suele Salir Mal |
|---|---|---|
| Capacidad de drenaje | La línea instalada drena de manera predecible en puntos locales de bajo y alto riesgo | El dibujo drena, pero la geometría de soporte instalada no lo hace |
| Control de tramo muerto | Las ramificaciones se revisan como ensambles higiénicos locales | Los puntos de muestreo y las tes de instrumentación se tratan como detalles menores |
| Estrategia de soldadura | El enrutamiento admite purga, acceso e inspección realistas | El diseño asume calidad de soldadura sin verificar la practicidad de fabricación |
| Lógica de conexión | El acceso y el recuento de interfaces se equilibran según la necesidad del proceso | Las opciones de abrazadera o soldadas se copian sin revisión específica de ubicación |
| Preparación para validación | Los conjuntos más difíciles son identificables y defendibles | La lógica de calificación comienza después de la fabricación en lugar de durante el diseño |
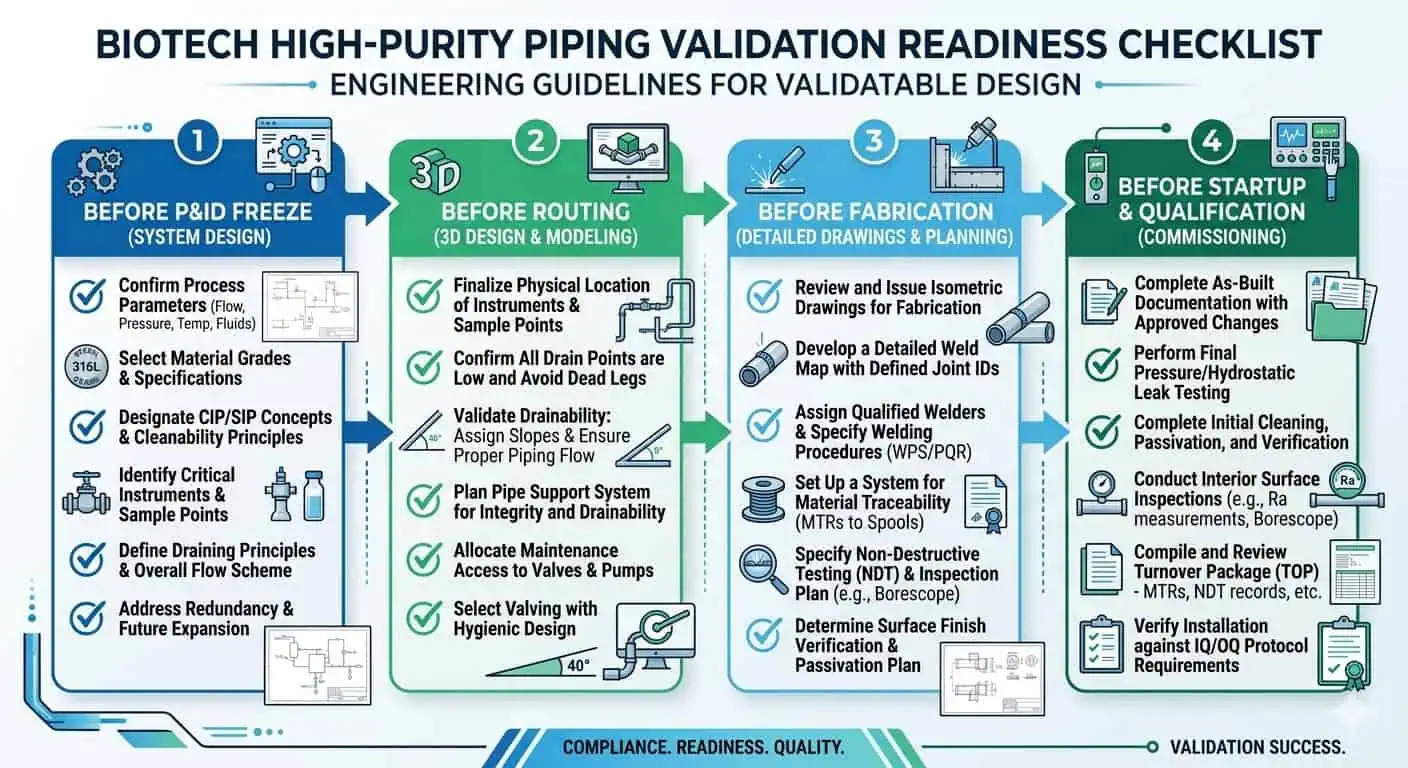
Conclusión: El diseño de tubería de alta pureza tiene éxito cuando la geometría, los materiales, la soldabilidad y la lógica de validación se tratan como un solo sistema.
El diseño de tubería de alta pureza para instalaciones biotecnológicas tiene éxito cuando la geometría, los materiales, la soldabilidad, la limpiabilidad, el drenaje y la lógica de validación se diseñan como un solo sistema. Los proyectos de tubería biotecnológica más sólidos no dependen únicamente del nombre de la aleación, la apariencia de la superficie o el estilo del componente del catálogo. Reducen el riesgo higiénico local en la rama, el punto de muestreo, el conjunto de válvulas y la zona de soldadura donde el proceso es menos tolerante a fallos.
Si desea un grupo de temas biotecnológicos más sólido, conecte este artículo con Acero Inoxidable 316L en Aplicaciones de Bioprocesos, Selección de Conexiones de Grado Alimentario para Sistemas de Fermentacióny Consideraciones de Mantenimiento y Validación para Tuberías de Grado Alimentario.
PREGUNTAS FRECUENTES
¿Cuál es el factor de diseño más importante en tuberías de biotecnología de alta pureza?
El factor más importante suele ser la geometría limpiable y drenable. Si el sistema no drena bien o crea comportamiento de tramo muerto en conjuntos locales, materiales más fuertes y acabados de mejor apariencia no resolverán el problema higiénico central.
¿Se requiere siempre 316L en tuberías higiénicas de grado alimentario para biotecnología?
No automáticamente. El 316L es una línea base común para servicio crítico de alta pureza, pero la decisión final aún depende de la química del proceso, la exposición a limpieza y esterilización, el requisito de acabado y el perfil de riesgo del conjunto local.
¿Por qué las ramas muertas son un problema tan grande en los sistemas de alta pureza?
Porque los tramos muertos debilitan el intercambio de fluido local, la efectividad de la limpieza y el drenaje. Son una de las razones más comunes por las que una rama local o un punto de muestreo sigue generando preocupación higiénica incluso cuando el bucle principal parece aceptable.
¿Cuándo se deben usar conexiones de ajuste por abrazadera en tuberías de biotecnología?
Úselos donde se necesite realmente acceso controlado, reemplazo de sellos o intervención modular. Pueden ser la elección correcta, pero cada interfaz añadida también aumenta el riesgo higiénico relacionado con los sellos, por lo que no deben usarse por defecto en cada ubicación de alta pureza.
¿Resuelve el electropulido problemas de soldadura deficiente o de geometría deficiente?
No. Un acabado más ajustado puede respaldar un objetivo higiénico más alto, pero no soluciona un drenaje deficiente, una geometría de ramal deficiente o una zona de soldadura deficiente.
¿Cómo afecta la validación a las decisiones de diseño de tuberías?
La validación cambia lo que el sistema debe poder demostrar, no solo cómo debe funcionar. Un diseño de tuberías que sea operable pero difícil de inspeccionar, documentar o defender aún puede ser un diseño débil en biotecnología.




