Documentação e rastreabilidade em projetos de tubulação farmacêutica não são papelada adicionada após a instalação. Eles são a cadeia de evidências que comprova que o sistema instalado corresponde ao material aprovado, acabamento, solda, inspeção e intenção de design higiênico. Em projetos GMP, um circuito de tubulação pode estar mecanicamente completo e ainda permanecer não liberável porque a documentação não comprova claramente o que foi instalado, como foi fabricado, o que mudou no campo e se a montagem final ainda atende ao padrão aprovado do projeto.
É por isso que engenheiros experientes não tratam os documentos de entrega como uma transferência administrativa. Eles os tratam como parte do controle de design do projeto desde o início. Se a rastreabilidade do material, registros de solda, registros de acabamento, evidências de inspeção, redlines e entregáveis de entrega não forem definidos antes do RFQ, o projeto frequentemente tenta reconstruir a cadeia de evidências posteriormente a um custo muito maior e com menor confiança. Este guia explica o que documentação e rastreabilidade realmente significam em projetos de tubulação farmacêutica, quais registros são mais importantes, onde a cadeia de evidências geralmente quebra e como as equipes GMP podem definir o pacote de documentação correto antes do início da fabricação.
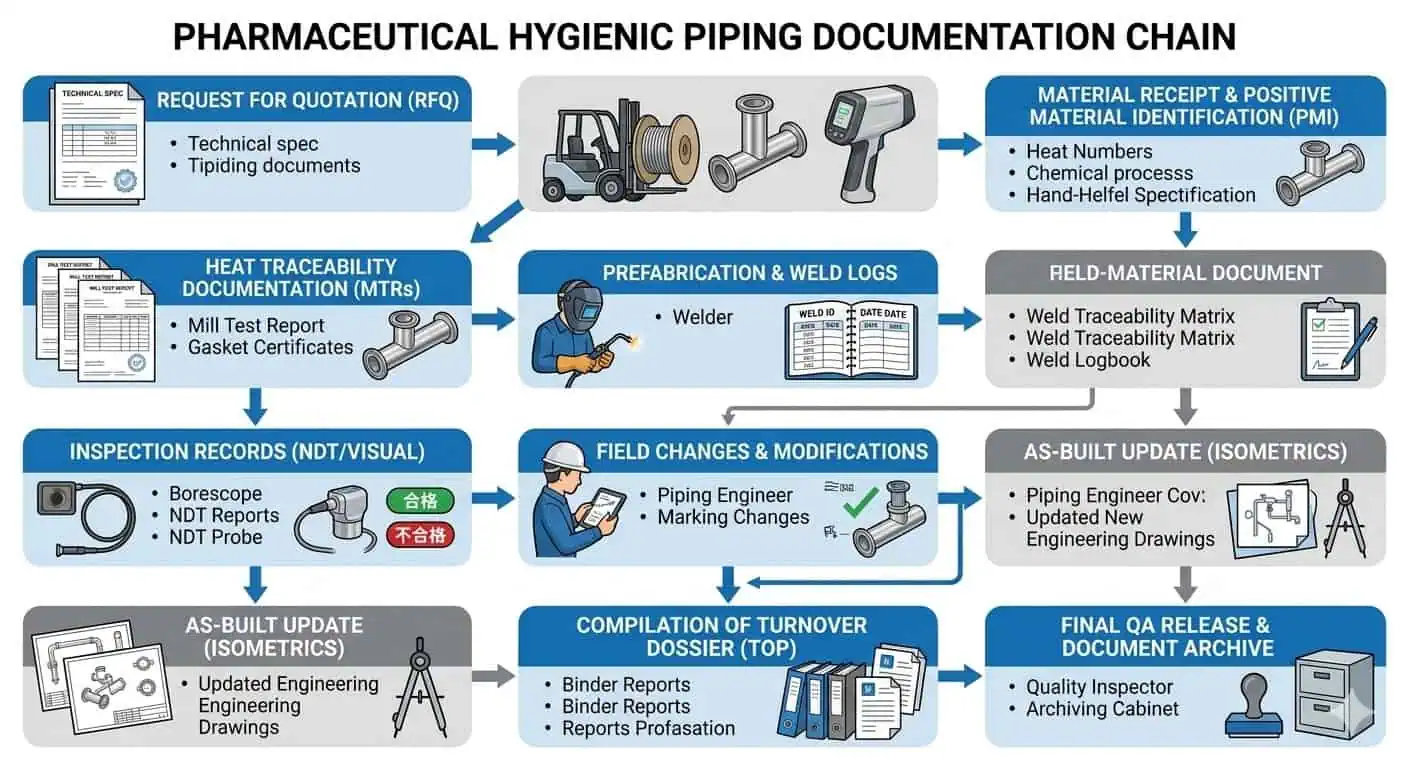
No trabalho farmacêutico real, os problemas de documentação raramente aparecem como falhas mecânicas dramáticas. Eles aparecem como fechamento QA mais lento, comentários de entrega não resolvidos, linhagem de solda pouco clara, históricos de spool incompatíveis ou incerteza sobre se o circuito instalado final ainda reflete a intenção higiênica aprovada. É por isso que uma documentação forte não é uma preferência de papelada. É um controle de engenharia.
Por que Documentação e Rastreabilidade Importam em Projetos de Tubulação Farmacêutica
Este é um Tópico de QA e Liberação, Não Apenas um Tópico de Arquivamento de Engenharia
Na tubulação farmacêutica, a documentação é parte do controle de liberação, não apenas da administração do projeto. O Capítulo 4 do EU GMP não descreve a documentação como uma conveniência de arquivamento. Ele descreve uma boa documentação como uma parte essencial do sistema de garantia de qualidade e o mecanismo usado para estabelecer, controlar, monitorar e registrar atividades que afetam a qualidade do produto. A lógica da FDA aponta na mesma direção: equipamentos em contato com o produto devem ser adequados para uso, e limpeza, manutenção e histórico do equipamento devem ser controlados e registrados. Em outras palavras, o circuito instalado tem que estar tecnicamente correto e comprovadamente correto ao mesmo tempo.
Caso típico da indústria: um circuito de transferência em contato com o produto está totalmente instalado, testado à pressão e visualmente aceitável. Operações vê um sistema de tubulação finalizado. QA vê uma cadeia de evidências incompleta porque o dossiê final ainda não pode vincular claramente a identidade do material aprovado, o histórico de solda e a configuração final as-built. A tubulação está fisicamente lá, mas a lógica de liberação ainda não está resolvida.
Conselho de especialista: Se a equipe do projeto trata a documentação como algo que começa na entrega, já é tarde demais. Em tubulação GMP, a história de liberação precisa ser construída enquanto o circuito está sendo projetado, fabricado, inspecionado e alterado—não depois que o último grampo é apertado.
Nota de engenharia: em tubulação GMP, o circuito instalado só é tão liberável quanto a cadeia de evidências que comprova sua condição final molhada.
Por que Projetos de Tubulação Farmacêutica Frequentemente Falham na Entrega, Não na Fabricação
Muitos projetos de tubulação farmacêutica não falham porque o circuito foi mal construído. Eles falham porque o projeto não consegue provar, em formato pronto para liberação, que o circuito instalado final ainda corresponde à intenção higiênica aprovada. Esse é um tipo diferente de falha, mas no trabalho GMP, muitas vezes é o mais perigoso porque aparece tarde, depois que o sistema já parece mecanicamente completo. A lógica de registro do Capítulo 4 do GMP da UE e da FDA apoia a mesma conclusão prática: se o histórico de limpeza, identidade do componente, status da solda e configuração instalada não puderem ser reconstruídos de forma confiável, o sistema se torna mais difícil de defender na liberação e posteriormente durante a operação.
Caso típico da indústria: A equipe de instalação de campo termina um circuito de grau alimentício e assume que o trabalho difícil acabou. Uma revisão posterior mostra que várias peças de tubulação foram revisadas em campo para melhorar o roteamento e a inclinação, mas o mapa final de soldas, matriz de localização de materiais e pacote como-construído nunca foram totalmente reconciliados. Ninguém está afirmando que o metal está errado. O problema é que o projeto não consegue mais provar claramente quais materiais certificados, registros de solda e resultados de inspeção pertencem ao arranjo instalado final. Nesse ponto, o circuito não está lutando contra um defeito de fabricação. Está lutando contra um defeito de evidência de liberação.
Engenheiros de projeto experientes, portanto, definem a cadeia de documentação antes do RFQ, não após a conclusão mecânica. Uma vez que a fabricação começa, cada corte de campo não controlado, troca de tubulação ou redirecionamento de ramal se torna mais difícil de fechar retroativamente. A lição de engenharia é simples: em tubulação GMP, se você esperar até a entrega para decidir o que deve ser rastreável, o projeto geralmente acaba reconstruindo a cadeia de evidências com custo mais alto e menor confiança.
O que o Quadro GMP e Regulatório Realmente Exige
Os regulamentos mais úteis são aqueles que mudam o que a equipe do projeto define e registra antes da entrega. Neste tópico, a estrutura central geralmente inclui:
- ASME BPE, que abrange materiais, projeto, fabricação, inspeções, testes e lógica de certificação para equipamentos de bioprocessamento e farmacêuticos.
- FDA 21 CFR 211.65, o que exige que as superfícies em contato com o produto sejam não reativas, não aditivas e não absorventes.
- FDA 21 CFR 211.67, que vincula a limpeza e manutenção de equipamentos a procedimentos escritos e registros.
- FDA 21 CFR 211.182, que aborda registros de limpeza, manutenção e uso de equipamentos principais.
- FDA 21 CFR 211.184, que abrange registros de componentes, recipientes, fechamentos e rotulagem.
- EU GMP Capítulo 4, que define a documentação como uma parte essencial do sistema de garantia de qualidade e exige que os registros sejam controlados, precisos, rastreáveis e retidos adequadamente.
Conclusão da pesquisa: essas fontes não tratam a documentação como suporte de fundo. Elas a tratam como uma parte controlada da execução de GMP. Para equipes de tubulação, isso significa que a pergunta nunca é apenas “que registros temos?” mas sim “esses registros ainda comprovam o sistema úmido final de forma suficientemente clara para a liberação de QA?”
O que Deve Ser Rastreável em um Projeto de Tubulação GMP
Tubos, Conexões, Válvulas e Outros Componentes Úmidos
O rastreamento deve seguir o caminho úmido, não apenas os componentes maiores ou mais fáceis. Muitas equipes gerenciam bem os tubos, mas tratam conexões menores, diafragmas, válvulas de amostragem, férulas, juntas e componentes de ramificação de forma muito casual. Em projetos GMP, isso é um erro. As menores partes úmidas são frequentemente as mais fáceis de substituir, as mais difíceis de rastrear posteriormente e as primeiras a criar questões de QA durante a entrega.
Caso típico da indústria: o rastreamento de tubos está completo, mas o pacote de entrega fica fraco em montagens locais porque conexões, juntas ou internos de válvulas de amostragem foram tratados fora do fluxo de trabalho principal de controle. A linha parece boa na inspeção, mas o elo de rastreamento mais fraco está exatamente onde a montagem higiênica é mais complexa.
Conselho de especialista: se um componente é importante o suficiente para ser especificado como parte do projeto higiênico, é importante o suficiente para ser rastreável como parte da lógica de entrega. Na prática, as equipes obtêm melhor fechamento de QA quando definem o rastreamento em torno do caminho úmido completo, em vez de apenas em torno dos tubos.
Certificados de Material, Números de Forno e Identidade de Lote
O rastreamento de material só é útil quando a localização instalada pode ser vinculada de forma limpa ao conjunto original de registros. Relatórios de teste de material, certificados EN 10204 3.1, números de forno e registros de recebimento são importantes, mas apenas se o projeto preservar o vínculo entre a identidade do fornecedor e a localização instalada do trecho, conexão ou montagem. Uma pilha de certificados sem uma matriz de localização limpa não é um pacote de rastreamento forte.
Caso típico da indústria: o projeto possui os certificados de material corretos em mãos, mas após corte em campo, re-enrolamento e reroteamento local, a equipe de entrega não consegue provar rapidamente quais números de lote acabaram em quais seções de ramal instaladas. O problema não é a falta de papel. O problema é que o papel não mapeia mais claramente a realidade instalada.
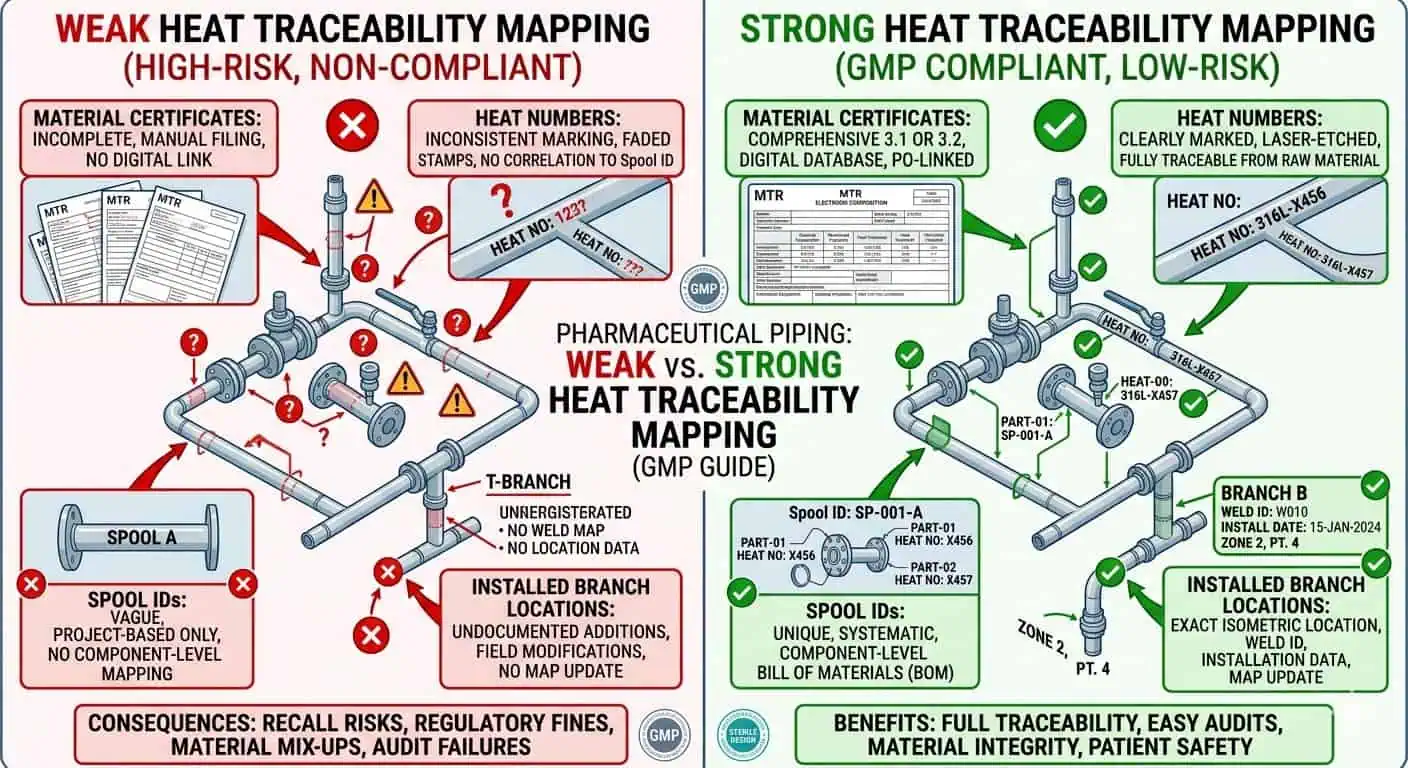
Conselho de especialista: em sistemas de contato com produto de alta consequência, defina a matriz de rastreabilidade antecipadamente, em vez de permitir que registros de material e registros de enrolamento evoluam separadamente. Uma vez que as modificações em campo começam, reconstruir esse vínculo se torna mais lento e menos confiável.
Mapas de Solda, Registros de Solda Orbital e Status de Inspeção
A documentação de solda é frequentemente a parte operacionalmente mais importante da cadeia de evidências de tubulação. Em sistemas farmacêuticos sanitários, números de solda, configurações da máquina, identidade do operador, datas, status de inspeção, histórico de reparos e status de aceitação são frequentemente mais decisivos do que as equipes esperam. Isso porque a solda é onde a identidade do material, a qualidade da fabricação, a evidência de inspeção e o desempenho sanitário final convergem. A ASME BPE é útil aqui não porque cria papelada por si só, mas porque trata fabricação, exame, teste e certificação como um quadro de controle conectado. Em projetos farmacêuticos, os registros de solda, portanto, não são apenas registros de oficina. Eles são registros de liberação.
Caso típico de engenharia: um circuito parece aceitável na inspeção visual, mas o QA ainda o sinaliza porque o mapa de solda e a revisão final do enrolamento não estão mais alinhados após alterações em campo. As soldas instaladas podem ser fisicamente aceitáveis, mas o conjunto de documentação não prova mais quais registros pertencem a quais locais de solda finais.
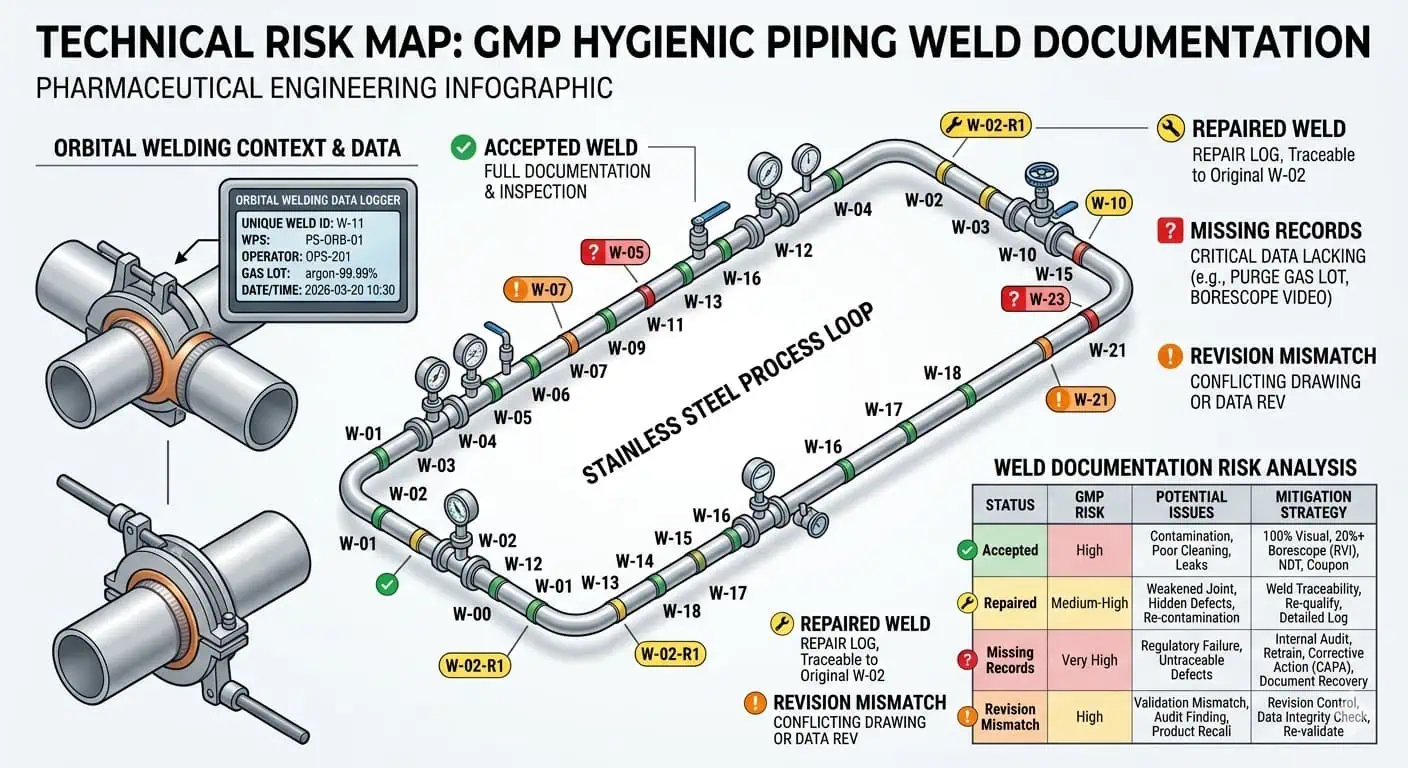
Conselho de especialista: não gerencie registros de solda como um conjunto de dados apenas de fabricação. Gerencie-os como um conjunto de dados de liberação que ainda deve fazer sentido após alterações em campo, substituição de enrolamento e fechamento final como construído.
Acabamento de Superfície, Eletropolimento, Passivação e Registros Relacionados
Os requisitos de acabamento importam apenas quando o projeto pode comprovar qual acabamento foi exigido, o que foi fornecido e como a condição final molhada foi preservada. Em sistemas GMP mais exigentes, a decisão sobre o acabamento não é separada da documentação. Se o projeto diferencia entre aço 316L padrão e 316L eletropolido, ou exige evidências de passivação e tratamento pós-fabricação, esses requisitos precisam de seu próprio caminho de registro no dossiê de entrega.
Caso típico da indústria: o grau do tubo era aceitável, mas a discussão de liberação mudou para se a condição final da superfície de várias peças de trecho em contato com o produto ainda correspondia à expectativa higiênica especificada após a fabricação e retrabalho. A liga não era o ponto fraco. A condição de acabamento documentada era.
Conselho de especialista: defina a documentação relacionada ao acabamento antes do início da fabricação. Se um projeto decide tardiamente que a condição da superfície importa mais do que o esperado, os registros ausentes geralmente são muito mais difíceis de reconstruir após a fabricação do que os certificados de material.
Linhas Vermelhas, Conforme Construído e Alterações de Campo
As alterações de campo são onde as cadeias de rastreabilidade mais frequentemente se quebram. Um ramal é movido para acesso. Um trecho é refeito para se adequar ao encaixe real. Um ponto de instrumento é revisado. A orientação de uma válvula muda. Nenhuma dessas ações é automaticamente fatal, mas cada uma cria risco de documentação se o processo de linha vermelha para conforme construído for fraco. Um dos princípios de documentação mais importantes na prática GMP é que os registros devem ser criados no momento em que o trabalho acontece. Isso importa porque registros reconstruídos são quase sempre mais fracos do que os contemporâneos.
Caso da indústria: uma conexão de skid GMP foi alterada no campo para melhorar o roteamento e o acesso à manutenção. A mudança em si era razoável. O problema foi que as referências de solda atualizadas, as referências de trecho e os desenhos conforme construído ficaram atrás da instalação. Na entrega, a equipe estava tentando reconciliar duas versões tecnicamente semelhantes, mas documentalmente inconsistentes, do mesmo circuito.
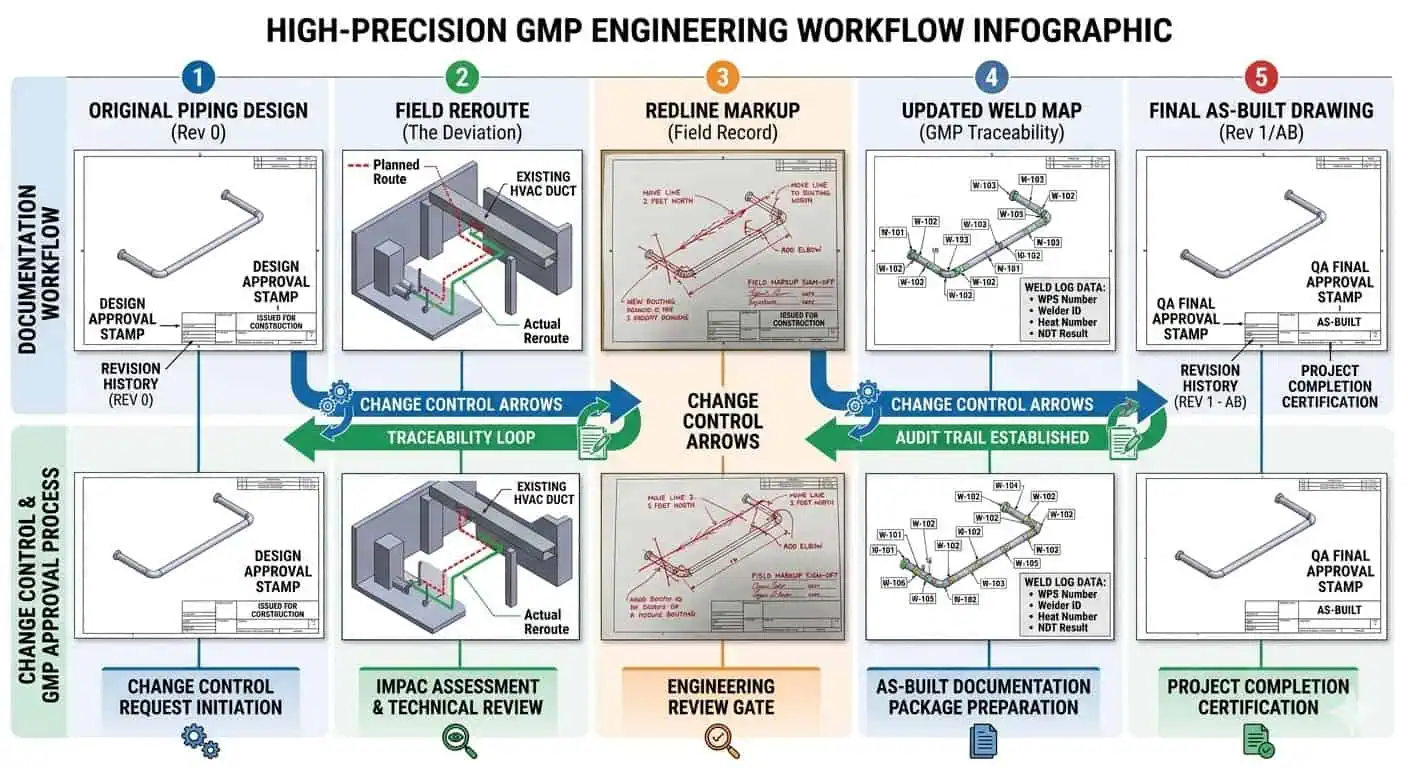
Conselho de especialista: Os redirecionamentos de campo não são o problema real. As evidências não fechadas dos redirecionamentos de campo são o problema real. O projeto deve tratar as linhas vermelhas e os as-builts como ferramentas de controle ativas, não como tarefas de desenho em estágio final.
O Pacote de Documentação Central que as Equipes de GMP Geralmente Esperam
Documentação de Materiais
A documentação de materiais comprova que os materiais molhados aprovados realmente entraram no sistema. No mínimo, isso geralmente significa certificados de material, rastreabilidade de calor, controle de recebimento e alguma forma de mapeamento de localização que vincula os componentes instalados ao conjunto de registros de material aprovado. Quanto mais forte for a consequência de grau alimentício ou contato com o produto, menos aceitável se torna deixar essa relação vaga.
Documentação de Fabricação e Solda
A documentação de fabricação comprova como o sistema se tornou o que é. É aqui que geralmente ficam os mapas de solda, registros de solda orbital, resultados de inspeção de solda, históricos de reparo, registros de boroscopia quando exigidos e o rastreamento do status de fabricação. O objetivo não é criar um dossiê espesso por si só. O objetivo é manter o circuito instalado auditável e tecnicamente defensável.
Documentação de Superfície e Tratamento
Os registros de superfície são importantes sempre que o acabamento ou tratamento pós-fabricação faz parte do requisito de grau alimentício. Se o projeto especifica eletropolimento, passivação ou um alvo de acabamento definido, o pacote de entrega deve mostrar como esse requisito foi aplicado e como as partes relevantes foram identificadas. Caso contrário, o projeto corre o risco de ter um requisito de acabamento no papel, mas sem evidências sólidas de que a superfície instalada ainda corresponde a ele.
Testes e Documentação de Entrega
Os registros de testes e entrega transformam o histórico de fabricação em evidência de liberação. Testes de pressão, testes de vazamento, fechamento de inspeção, encerramento da lista de pendências e montagem do dossiê final são onde o projeto demonstra que o circuito fabricado não apenas foi construído, mas também verificado e fechado de forma que suporte a operação GMP.
Caso típico da indústria: o projeto tem todos os registros individuais em algum lugar, mas a entrega ainda fica paralisada porque o pacote não está estruturado da forma que o Controle de Qualidade precisa para revisar e aprovar o circuito. Isso não é apenas um problema de documento ausente. É um problema de lógica do dossiê.

Conselho de especialista: se os documentos de entrega estão sendo montados pela primeira vez apenas após a conclusão mecânica, o projeto já está atrasado do ponto de vista do controle de documentação.
Controle de Mudanças e Registros de Desvios
A documentação de mudanças é o que mantém a cadeia final de evidências crível. O projeto deve ser capaz de mostrar o que foi alterado, quem aprovou, qual inspeção ou retrabalho seguiu e como a condição final como-construído absorveu essa alteração. Sem isso, mesmo alterações de campo tecnicamente razoáveis podem criar hesitação desnecessária de QA.
| Conjunto de Documentação | O que Comprova | Onde Falha Comumente |
|---|---|---|
| Certificados de material e matriz de rastreabilidade | Os materiais molhados aprovados foram realmente instalados | O mapeamento de localização torna-se confuso após corte ou reroteamento de campo |
| Mapas de solda e registros de solda | As soldas finais foram concluídas e inspecionadas sob controle | Os números de solda param de corresponder às revisões finais de spool |
| Acabamento / EP / registros de passivação | A condição de superfície especificada foi alcançada e preservada | Retrabalho ou alterações tardias de acabamento não estão totalmente documentados |
| Redlines e as-builts | O loop instalado corresponde à configuração final aprovada | Alterações de campo ocorrem mais rápido que o fechamento de desenhos |
| Dossiê de entrega | A cadeia completa de evidências está pronta para revisão de QA | Registros existem, mas não em uma estrutura pronta para liberação |
Onde as Cadeias de Documentação Geralmente Quebram
Material Correto, mas a Matriz de Rastreabilidade Era Fraca
Uma das falhas mais comuns não é a falta de material, mas o mapeamento fraco entre material e localização. As equipes às vezes assumem que ter os certificados é suficiente. Não é suficiente se o projeto não puder provar rapidamente onde o material certificado acabou após corte, fabricação, enrolamento e alteração de campo.
Soldas Aceitáveis, mas o Conjunto de Registros de Solda Estava Incompleto
Um circuito pode ser tecnicamente sólido e ainda falhar no fechamento da documentação porque o conjunto de registros de solda está incompleto. Status de solda ausente, histórico de reparo não claro ou numeração de solda desalinhada geralmente cria mais atraso do que as equipes esperam. Em tubulação GMP, a evidência de solda não é apenas uma ferramenta de fabricação. É parte da prontidão para liberação.
Alterações de Campo Ocorreram Mais Rápido do que a Atualização da Documentação
A documentação frequentemente fica atrás do projeto exatamente no momento em que o projeto se torna mais dinâmico. Alterações de roteamento em estágio tardio, revisões de conexão, ajustes de montagem de campo e ramificações adicionadas frequentemente ocorrem sob pressão de cronograma. Se o conjunto de documentos não acompanhar, o pacote final de entrega se torna um exercício de reconstrução em vez de uma transferência controlada.
Os Componentes Menores Criaram o Maior Problema de QA
Pequenas partes molhadas criam um risco desproporcional de documentação. Conexões, componentes de amostra, diafragmas, juntas e partes molhadas relacionadas a instrumentos são frequentemente onde a cadeia de evidências mais limpa se quebra primeiro. As equipes tendem a pensar em termos de trechos de tubulação, mas o Controle de Qualidade muitas vezes vivencia o projeto em termos de montagens locais não resolvidas.
Lições de especialistas do trabalho de fechamento em campo: quanto mais local e substituível for a montagem, menos seguro é supor que seus registros serão tratados por si mesmos.
Como os Engenheiros Devem Construir Requisitos de Documentação Antes da RFQ
Definir o que Deve Ser Rastreável
Antes da RFQ, defina quais componentes molhados devem permanecer rastreáveis durante a instalação e a entrega. Se apenas a tubulação for controlada e as partes molhadas menores forem deixadas vagas, a cadeia de evidências geralmente será mais fraca onde a montagem higiênica é mais complexa.
Definir o que Deve Ser Registrado Durante a Fabricação
Os projetos devem definir o que deve ser registrado enquanto o trabalho está acontecendo, não apenas o que deve existir no final. Registros de solda, pontos de inspeção, registros relacionados ao acabamento, evidência de passivação quando relevante e atualizações de alterações em campo devem fazer parte do fluxo de projeto definido.
Definir o que o Controle de Qualidade (CQ) deve receber na entrega
O pacote de entrega deve ser definido como um entregável de liberação, não uma coleção vaga de qualquer coisa que o contratante possa montar posteriormente. Se o CQ espera uma estrutura específica de dossiê, matriz de rastreabilidade ou formato de registro, o projeto deve definir isso enquanto ainda há tempo para gerar esses registros corretamente.
Definir o que deve ser mantido após a partida
A cadeia de documentação deve sobreviver na operação, não parar na entrega. Registros de equipamentos, registros de manutenção, rastreabilidade de peças de reposição e atualizações controladas do sistema instalado são todos parte de manter a cadeia de evidências original viva. Um sistema pronto para liberação pode se tornar muito mais difícil de defender posteriormente se os registros do ciclo de vida forem fracos.
O conselho de projeto mais forte é simples: defina a cadeia de evidências antes da aquisição. Não espere até que a fabricação esteja em andamento para decidir se a rastreabilidade térmica, registros de acabamento, status de solda ou documentação de alterações em campo serão importantes. Nesse ponto, o projeto geralmente acaba coletando documentos de forma reativa em vez de controlá-los deliberadamente. Esta é uma das lições práticas mais claras do trabalho de entrega em Boas Práticas de Fabricação (GMP): projetos que definem o conjunto de registros antes da Solicitação de Cotação (RFQ) geralmente fecham mais rápido e com menos surpresas de CQ do que projetos que tentam reconstruí-lo posteriormente.
Como isso se conecta à seleção de projeto, material e conexões
Seleção de Material Sem Controle de Documentação Não É Risco Fechado
Uma boa decisão de material só se torna uma decisão segura de projeto quando é documentada de forma clara. Para a lógica mais ampla do lado do material, conecte esta página com Seleção de Materiais para Tubulação de Grau Alimentício Farmacêutica.
Requisitos de Acabamento Só Importam Se Forem Comprovados
Eletropolimento, metas de acabamento e expectativas de pós-tratamento não fecham o risco, a menos que os registros os comprovem. Vincule este tópico com Aço Inoxidável 316L Eletropolidado vs 316L Padrão.
Conexões e Montagens de Amostra Precisam de Sua Própria Cadeia de Evidências
Quanto menor e mais local a montagem se torna, mais provável que sua documentação se torne a parte mais fraca do pacote de entrega. Vincule este tópico com Seleção de Conexões de Grau Alimentício para Instalações GMP.
A Documentação Como Construída Deve Refletir o Risco Real de Limpeza
A documentação não deve apenas provar o que foi instalado. Ela também deve refletir a realidade higiênica local final do sistema. Para essa lógica, conecte esta página com Considerações de Projeto CIP para Tubulação Higiênica.
Erros Comuns na Documentação e Rastreabilidade para Projetos de Tubulação Farmacêutica
Tratar a Documentação como uma Atividade de Entrega em vez de uma Entrada de Projeto
Projetos que definem o pacote de documentação tardiamente geralmente acabam reconstruindo registros sob pressão de cronograma.
Rastrear Tubulação mas Não Rastrear Pequenos Componentes Molhados
O elo mais fraco da rastreabilidade geralmente aparece em conexões, vedações, diafragmas ou montagens locais de amostra.
Manter Dados de Solda Separados da Lógica de Liberação em Nível de Linha
Registros de solda são muito menos úteis se não mapearem claramente para o circuito instalado final e seu status de liberação.
Permitir que Alterações de Campo se Afastem da Realidade Instalada
Quando mudanças de campo avançam mais rápido que atualizações controladas, o pacote de entrega se torna mais difícil de confiar.
Supondo que o Controle de Qualidade Aceitará Posteriormente
Em tubulações de Boas Práticas de Fabricação (GMP), a falta de evidências raramente é mais fácil de corrigir no final do projeto do que durante a execução controlada.
Coletar Documentos em Excesso, mas Definir Insuficientemente o que Realmente Importa
Grandes volumes de documentos não criam automaticamente um pacote de entrega robusto. O que importa é se o conjunto de registros comprova o sistema sanitário instalado de forma suficientemente clara para liberação e controle posterior do ciclo de vida.
Lista de Verificação Prática: O que Perguntar Antes de Liberar um Sistema de Tubulação Farmacêutica
Antes do Início da Fabricação
- Quais componentes molhados devem ser rastreáveis?
- Quais registros devem ser criados durante a fabricação?
- Quais evidências de solda, acabamento e inspeção o Controle de Qualidade exigirá posteriormente?
- Como as alterações de campo serão incorporadas aos registros controlados?
Antes da Conclusão Mecânica
- As marcações vermelhas estão atualizadas?
- Os componentes instalados mapeiam claramente os registros de materiais aprovados?
- O status de solda e o histórico de reparos estão encerrados?
- Os registros de acabamento e tratamento estão completos onde exigidos?
Antes da Liberação de QA
- O pacote de entrega corresponde ao circuito instalado real?
- Existem montagens locais ainda não resolvidas em registros de rastreabilidade ou inspeção?
- O projeto pode comprovar a condição final como-construído claramente o suficiente para liberação?
Após a Partida
- Como os registros de equipamentos e manutenção continuarão?
- Como as peças de reposição permanecerão rastreáveis?
- Como as futuras alterações serão vinculadas à cadeia de evidências original?
| Estágio do Projeto | Pergunta-Chave de Documentação | Como é um Bom Controle |
|---|---|---|
| Antes da RFQ | O que deve ser rastreável e entregável? | O conjunto de registros é definido, não presumido |
| Durante a fabricação | Os registros estão sendo criados em tempo real? | Registros de solda, material, acabamento e alterações permanecem atualizados |
| Antes da entrega | O dossiê corresponde à realidade instalada? | Conformidade de as-built, rastreabilidade e encerramento de inspeção |
| Após a partida | A cadeia de evidências sobreviverá a mudanças no ciclo de vida? | Registros de manutenção e substituição continuam sob controle |
Conclusão: Em Tubulação Farmacêutica, a Documentação Comprova que o Sistema que Você Pensa ter Construído é o Sistema Realmente Instalado
Boa documentação e rastreabilidade não agregam valor após o projeto. Elas protegem o projeto de se tornar irrealizável no exato momento em que deveria estar pronto para operar. Na tubulação farmacêutica, o sistema instalado só é aceitável quanto a cadeia de evidências que comprova que seu material, fabricação, acabamento, inspeção e alterações foram controlados.
Os projetos mais robustos não tentam reconstruir essa cadeia de evidências na entrega. Eles a definem antes da RFQ, mantêm-na durante a fabricação e a encerram antes da liberação. Para o cluster completo de tópicos farmacêuticos, conecte este artigo com Seleção de Materiais para Tubulação de Grau Alimentício Farmacêutica, Aço Inoxidável 316L Eletropolidado vs 316L Padrão, Seleção de Conexões de Grau Alimentício para Instalações GMPe Considerações de Projeto CIP para Tubulação Higiênica.
PERGUNTAS FREQUENTES
Qual documentação é necessária para projetos de tubulação farmacêutica?
O pacote exato depende do escopo do projeto, mas geralmente inclui certificados de material, registros de rastreabilidade, documentação de solda, registros de inspeção, evidências de acabamento ou tratamento quando exigidas, redlines, as-builts e registros de entrega que suportam a liberação de QA.
Qual rastreabilidade é exigida em tubulação de GMP?
A rastreabilidade deve seguir o caminho molhado. Isso frequentemente significa que tubos, conexões, válvulas, conjuntos locais e outros componentes críticos em contato com o produto devem ser rastreáveis até registros aprovados de forma que ainda correspondam à condição instalada.
Por que os projetos de tubulação farmacêutica falham na entrega?
Eles frequentemente falham porque a cadeia de evidências está incompleta. A instalação pode ser fisicamente aceitável, mas registros ausentes ou fracos de material, solda, acabamento ou as-builts ainda podem atrasar a liberação de QA.
As conexões e juntas precisam de rastreabilidade em projetos de GMP?
Em muitas aplicações higiênicas críticas, sim. Componentes molhados menores são frequentemente onde o elo de documentação mais fraco aparece, então eles não devem ser tratados como consumíveis casuais se influenciarem o desempenho higiênico ou o risco de liberação.
São necessários registros de solda para tubulação higiênica de grau alimentício farmacêutico?
Os projetos comumente dependem de mapas de solda e documentação de solda porque são centrais para comprovar o status de fabricação e inspeção. O formato exato varia conforme o projeto, mas a documentação de solda deficiente é um dos problemas mais comuns na entrega.
Qual é a diferença entre registros as-built e documentos de entrega?
Os registros as-built mostram a configuração final instalada. Os documentos de entrega são o pacote de evidências mais amplo usado para apoiar a liberação, incluindo rastreabilidade, inspeção, testes e registros relacionados ao projeto.




