Документация и прослеживаемость в проектах фармацевтических трубопроводов - это не бумажная работа, добавляемая после монтажа. Это цепочка доказательств, подтверждающая, что установленная система соответствует утвержденным материалам, отделке, сварке, инспекции и гигиеническому замыслу проекта. В проектах GMP трубопроводный контур может быть механически завершен, но оставаться недопустимым к эксплуатации, потому что документация не может четко доказать, что было установлено, как оно было изготовлено, что изменилось на месте и соответствует ли окончательная сборка утвержденному стандарту проекта.
Вот почему опытные инженеры не рассматривают передаточные документы как административную передачу. Они рассматривают их как часть контроля проектирования с самого начала. Если прослеживаемость материалов, записи о сварке, записи о отделке, доказательства инспекции, красные линии и передаваемые результаты не определены до запроса предложений, проект часто пытается восстановить цепочку доказательств позже с гораздо более высокими затратами и меньшей уверенностью. Это руководство объясняет, что на самом деле означают документация и прослеживаемость в проектах фармацевтических трубопроводов, какие записи наиболее важны, где цепочка доказательств обычно нарушается и как команды GMP могут определить правильный пакет документации до начала изготовления.
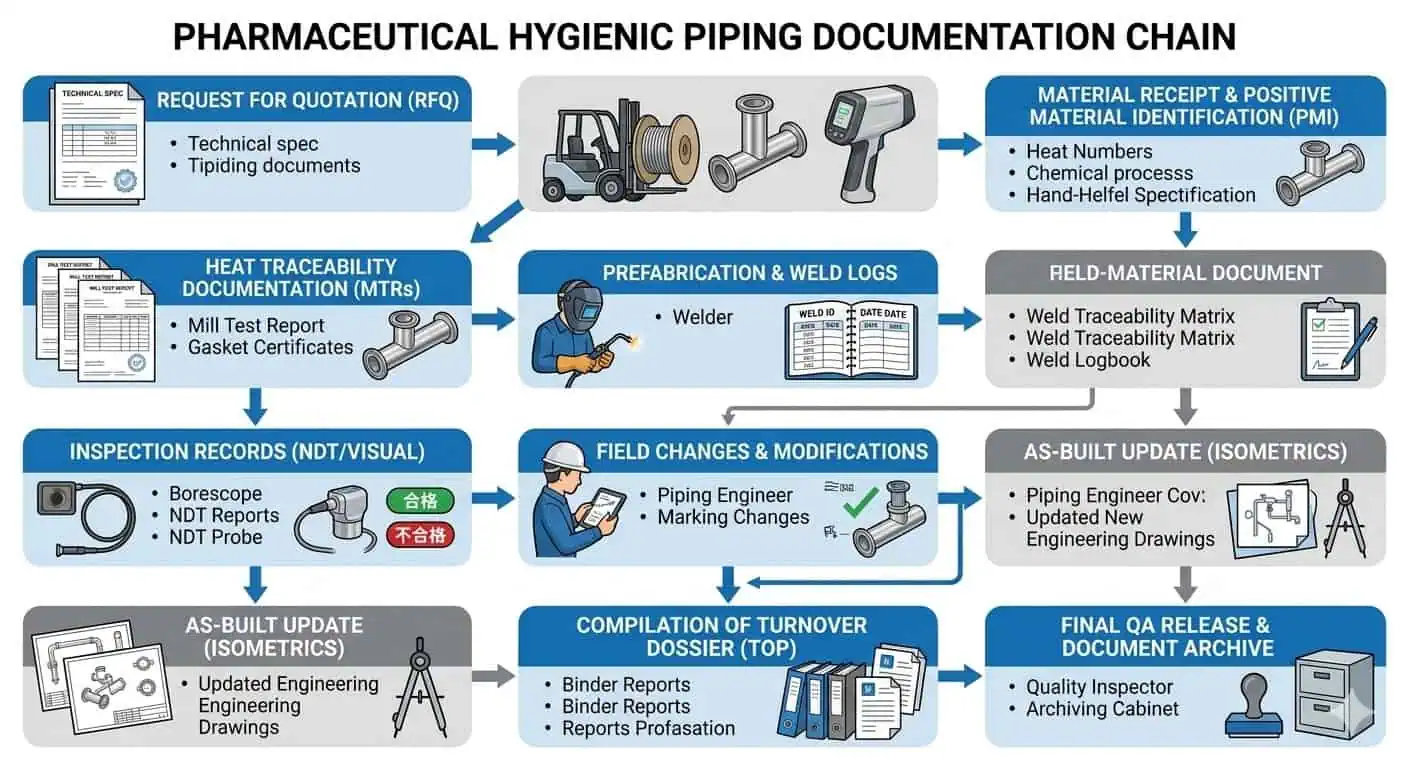
В реальной фармацевтической работе проблемы с документацией редко проявляются как драматические механические сбои. Они проявляются как более медленное закрытие QA, нерешенные замечания при передаче, неясная история сварки, несоответствующие истории секций или неопределенность относительно того, отражает ли окончательный установленный контур утвержденный гигиенический замысел. Вот почему надежная документация - это не предпочтение в бумажной работе. Это инженерный контроль.
Почему документация и прослеживаемость важны в проектах фармацевтических трубопроводов
Это тема QA и выпуска, а не просто тема инженерного делопроизводства
В фармацевтических трубопроводах документация является частью контроля выпуска, а не просто администрацией проекта. Глава 4 EU GMP не описывает документацию как удобство делопроизводства. Она описывает хорошую документацию как неотъемлемую часть системы обеспечения качества и механизм, используемый для установления, контроля, мониторинга и записи действий, влияющих на качество продукции. Логика FDA указывает в том же направлении: оборудование, контактирующее с продуктом, должно быть пригодно для использования, а очистка, техническое обслуживание и история оборудования должны контролироваться и регистрироваться. Другими словами, установленный контур должен быть технически правильным и доказуемо правильным одновременно.
Типичный отраслевой случай: Контур передачи, контактирующий с продуктом, полностью установлен, испытан под давлением и визуально приемлем. Операции видят готовую трубопроводную систему. QA видит неполную цепочку доказательств, потому что окончательное досье все еще не может четко связать утвержденную идентичность материала, историю сварки и окончательную конфигурацию по факту выполнения. Трубопровод физически присутствует, но логика выпуска все еще не решена.
Экспертный совет: Если проектная команда рассматривает документацию как нечто, что начинается при сдаче объекта, уже слишком поздно. В трубопроводах GMP история выпуска должна создаваться во время проектирования, изготовления, контроля и изменения контура — а не после затяжки последнего хомута.
Техническое примечание: в трубопроводах GMP установленный контур может быть выпущен только в той мере, в какой цепочка доказательств подтверждает его окончательное состояние в контакте с продуктом.
Почему проекты фармацевтических трубопроводов часто терпят неудачу при сдаче, а не при изготовлении
Многие проекты фармацевтических трубопроводов терпят неудачу не из-за плохого изготовления контура. Они терпят неудачу, потому что проект не может доказать в форме, готовой к выпуску, что окончательный установленный контур по-прежнему соответствует утвержденному гигиеническому замыслу. Это другой вид неудачи, но в работе по GMP он часто более опасен, потому что проявляется поздно, после того как система уже выглядит механически завершенной. Логика ведения записей в EU GMP Chapter 4 и FDA поддерживает один и тот же практический вывод: если историю очистки, идентификацию компонентов, состояние сварных швов и установленную конфигурацию нельзя надежно восстановить, систему становится труднее защищать при выпуске и позже во время эксплуатации.
Типичный отраслевой случай: Полевая монтажная команда завершает гигиенический контур и предполагает, что сложная работа окончена. Последующий обзор показывает, что несколько секций трубопровода были изменены в полевых условиях для улучшения трассировки и уклона, но окончательная карта сварных швов, матрица материалов-местоположений и исполнительный пакет так и не были полностью согласованы. Никто не утверждает, что металл неправильный. Проблема в том, что проект больше не может четко доказать, какие сертифицированные материалы, записи о сварке и результаты контроля относятся к окончательной установленной конфигурации. На этом этапе контур борется не с дефектом изготовления. Он борется с дефектом доказательств выпуска.
Поэтому опытные инженеры проекта определяют цепочку документации до запроса предложений, а не после механического завершения. Как только начинается изготовление, каждое неконтролируемое полевое разрезание, замена секции трубопровода или перенаправление ответвления становится труднее закрыть задним числом. Технический урок прост: в трубопроводах GMP, если ждать до сдачи объекта, чтобы решить, что должно быть прослеживаемым, проект обычно заканчивается перестройкой цепочки доказательств с более высокими затратами и меньшей уверенностью.
Что на самом деле требуют GMP и нормативная база
Наиболее полезные нормативные акты — это те, которые меняют то, что проектная команда определяет и записывает до сдачи объекта. В этой теме основная структура обычно включает:
- ASME BPE, которая охватывает материалы, проектирование, изготовление, инспекции, тестирование и логику сертификации для оборудования для биопроцессинга и фармацевтики.
- FDA 21 CFR 211.65, что требует, чтобы поверхности, контактирующие с продуктом, были нереактивными, неаддитивными и неабсорбирующими.
- FDA 21 CFR 211.67, которая связывает очистку и техническое обслуживание оборудования с письменными процедурами и записями.
- FDA 21 CFR 211.182, которая касается журналов очистки, технического обслуживания и использования основного оборудования.
- FDA 21 CFR 211.184, которая охватывает записи о компонентах, контейнерах, крышках и маркировке.
- EU GMP Глава 4, которая определяет документацию как важную часть системы обеспечения качества и требует, чтобы записи контролировались, были точными, прослеживаемыми и надлежащим образом хранились.
Вывод исследования: Эти источники не рассматривают документацию как фоновую поддержку. Они рассматривают её как контролируемую часть выполнения GMP. Для трубопроводных команд это означает, что вопрос никогда не сводится к “какие записи у нас есть?”, а к “доказывают ли эти записи окончательную смоченную систему достаточно чётко для выпуска QA?”
Что должно быть отслеживаемым в проекте трубопроводов GMP
Трубки, фитинги, клапаны и другие смоченные компоненты
Отслеживаемость должна следовать по смоченному пути, а не только по самым крупным или простым компонентам. Многие команды хорошо управляют трубками, но относятся к меньшим фитингам, диафрагмам, пробоотборным клапанам, обжимным кольцам, прокладкам и ответвлениям слишком небрежно. В проектах GMP это ошибка. Самые маленькие смощенные детали часто легче всего заменить, сложнее отследить позже и они первыми вызывают вопросы QA при сдаче.
Типичный отраслевой случай: отслеживаемость трубок завершена, но пакет сдачи становится слабым на локальных сборках, потому что фитинги, прокладки или внутренние части пробоотборных клапанов обрабатывались вне основного рабочего процесса контроля. Линия выглядит хорошо при обходе, но самое слабое звено отслеживаемости находится именно там, где гигиеническая сборка наиболее сложна.
Экспертный совет: если компонент достаточно важен, чтобы быть указанным как часть гигиенического дизайна, он достаточно важен, чтобы быть отслеживаемым как часть логики сдачи. На практике команды получают лучшую закрытость QA, когда они определяют отслеживаемость вокруг полного смоченного пути, а не только вокруг трубок.
Сертификаты материалов, номера плавок и идентификаторы партий
Отслеживаемость материалов полезна только тогда, когда установленное местоположение может быть чётко привязано к исходному набору записей. Отчёты об испытаниях материалов, сертификаты EN 10204 3.1, номера плавок и записи о приёмке — всё это важно, но только если проект сохраняет связь между идентификатором поставщика и установленным местоположением секции трубопровода, фитинга или сборки. Куча сертификатов без чёткой матрицы местоположений не является сильным пакетом отслеживаемости.
Типичный отраслевой случай: Проект имеет на руках правильные сертификаты материалов, но после полевой резки, повторной намотки и локальной перемаршрутизации команда сдачи не может быстро доказать, какие номера плавок оказались в каких установленных ответвлениях. Проблема не в отсутствии бумаг. Проблема в том, что бумаги больше не соответствуют установленной реальности.
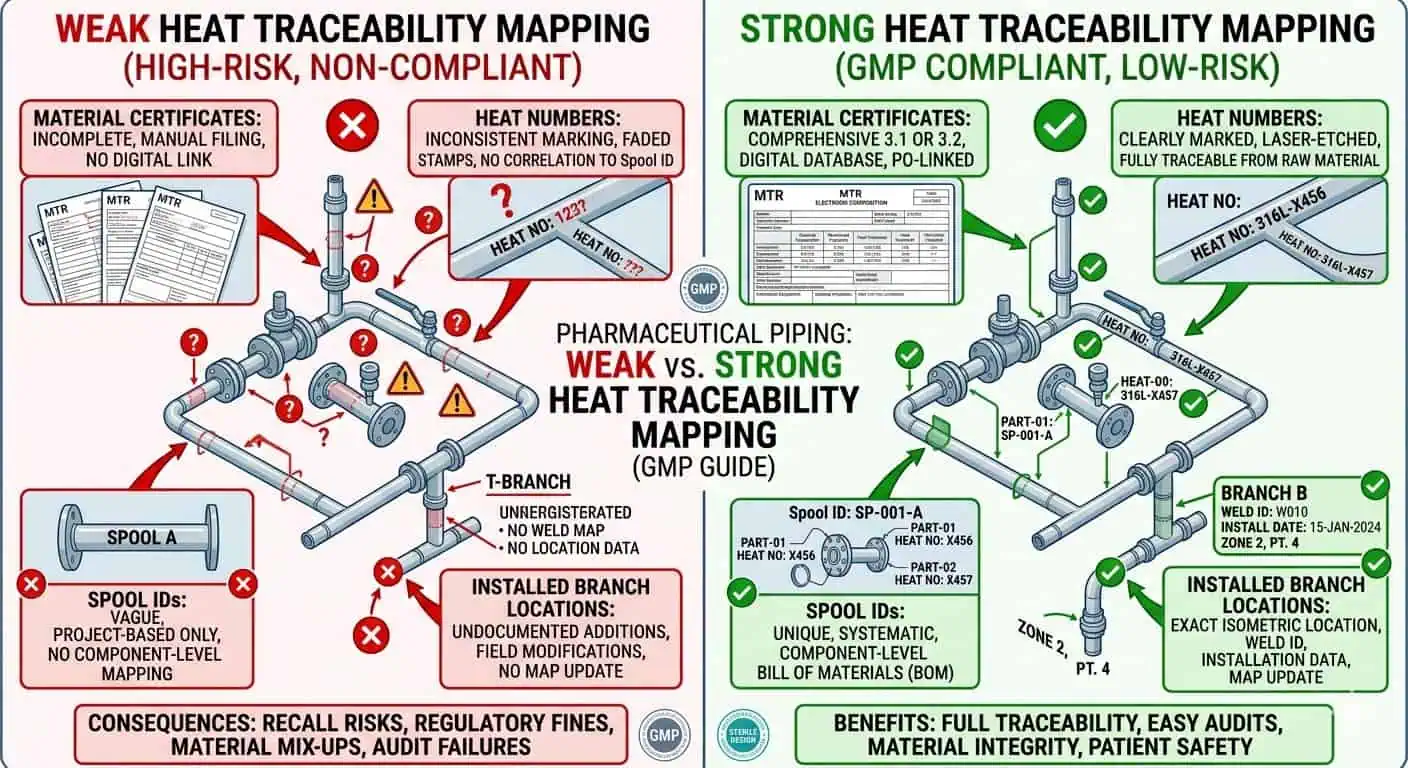
Экспертный совет: В системах с высокими последствиями контакта с продуктом определите матрицу прослеживаемости заранее, вместо того чтобы позволять записям материалов и трубопроводов развиваться отдельно. Как только начинаются полевые модификации, восстановление этой связи становится медленнее и менее надежным.
Карты сварки, журналы орбитальной сварки и статус инспекции
Документация по сварке часто является наиболее оперативно важной частью цепочки доказательств для трубопроводов. В гигиенических фармацевтических системах номера сварных швов, настройки оборудования, личность оператора, даты, статус инспекции, история ремонта и статус приемки часто оказываются более решающими, чем ожидают команды. Это потому, что сварной шов — это место, где сходятся идентичность материала, качество изготовления, доказательства инспекции и конечная гигиеническая производительность. ASME BPE полезен здесь не потому, что он создает бумажную работу ради самой себя, а потому, что он рассматривает изготовление, осмотр, испытания и сертификацию как одну связанную систему контроля. В фармацевтических проектах журналы сварки, следовательно, не просто записи цеха. Это записи сдачи.
Типичный инженерный случай: Контур выглядит приемлемым при обходе, но QA все равно отмечает его, потому что карта сварки и окончательная ревизия трубопровода больше не совпадают после полевых изменений. Установленные сварные швы могут быть физически приемлемыми, но набор документации больше не доказывает, какие записи принадлежат каким конечным местам сварки.
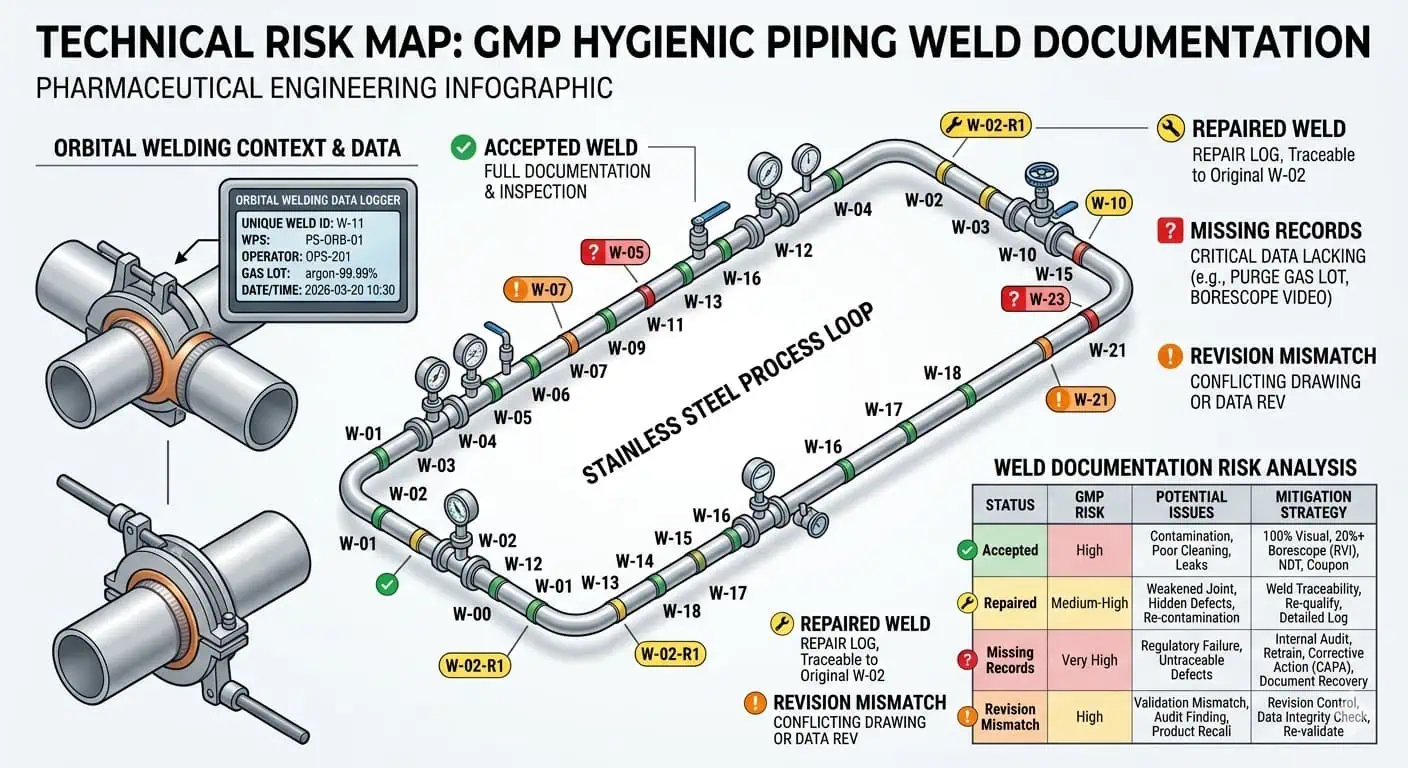
Экспертный совет: Не управляйте записями сварки как набором данных только для изготовления. Управляйте ими как набором данных для сдачи, который все еще должен иметь смысл после полевых изменений, замены трубопроводов и окончательного закрытия по факту установки.
Отделка поверхности, электрохимическая полировка, пассивация и связанные записи
Требования к отделке имеют значение только тогда, когда проект может доказать, какая отделка требовалась, что было поставлено и как было сохранено конечное смоченное состояние. В более требовательных системах GMP решение о отделке неотделимо от документации. Если проект различает стандартную 316L и электрохимически полированную 316L или требует пассивации и доказательств пост-производственной обработки, эти требования нуждаются в собственном пути записи в досье сдачи.
Типичный отраслевой случай: Сорт трубки был приемлемым, но обсуждение выпуска сместилось на то, соответствует ли конечное состояние поверхности нескольких штуцеров, контактирующих с продуктом, указанным гигиеническим ожиданиям после изготовления и переделки. Сплав не был слабым звеном. Документированное состояние отделки было.
Экспертный совет: Определите документацию, связанную с отделкой, до начала изготовления. Если проект поздно решает, что состояние поверхности важнее, чем ожидалось, отсутствующие записи часто гораздо сложнее восстановить после изготовления, чем сертификаты на материал.
Красные линии, как построено и полевые изменения
Полевые изменения — это где цепочки прослеживаемости чаще всего разрываются. Ветвь перемещена для доступа. Штуцер переделан для соответствия фактической сборке. Точка прибора пересмотрена. Ориентация клапана изменена. Ни одно из этих действий не является автоматически фатальным, но каждое создает риск документации, если процесс от красных линий к как построено слаб. Один из самых важных принципов документации в практике GMP заключается в том, что записи должны создаваться во время выполнения работ. Это важно, потому что восстановленные записи почти всегда слабее, чем современные.
Промышленный случай: Соединение GMP-стойки было изменено в поле для улучшения маршрутизации и доступа для обслуживания. Само изменение было разумным. Проблема заключалась в том, что обновленные ссылки на сварные швы, ссылки на штуцеры и чертежи как построено отставали от установки. К сдаче команда пыталась согласовать две технически похожие, но документально несовместимые версии одного и того же контура.
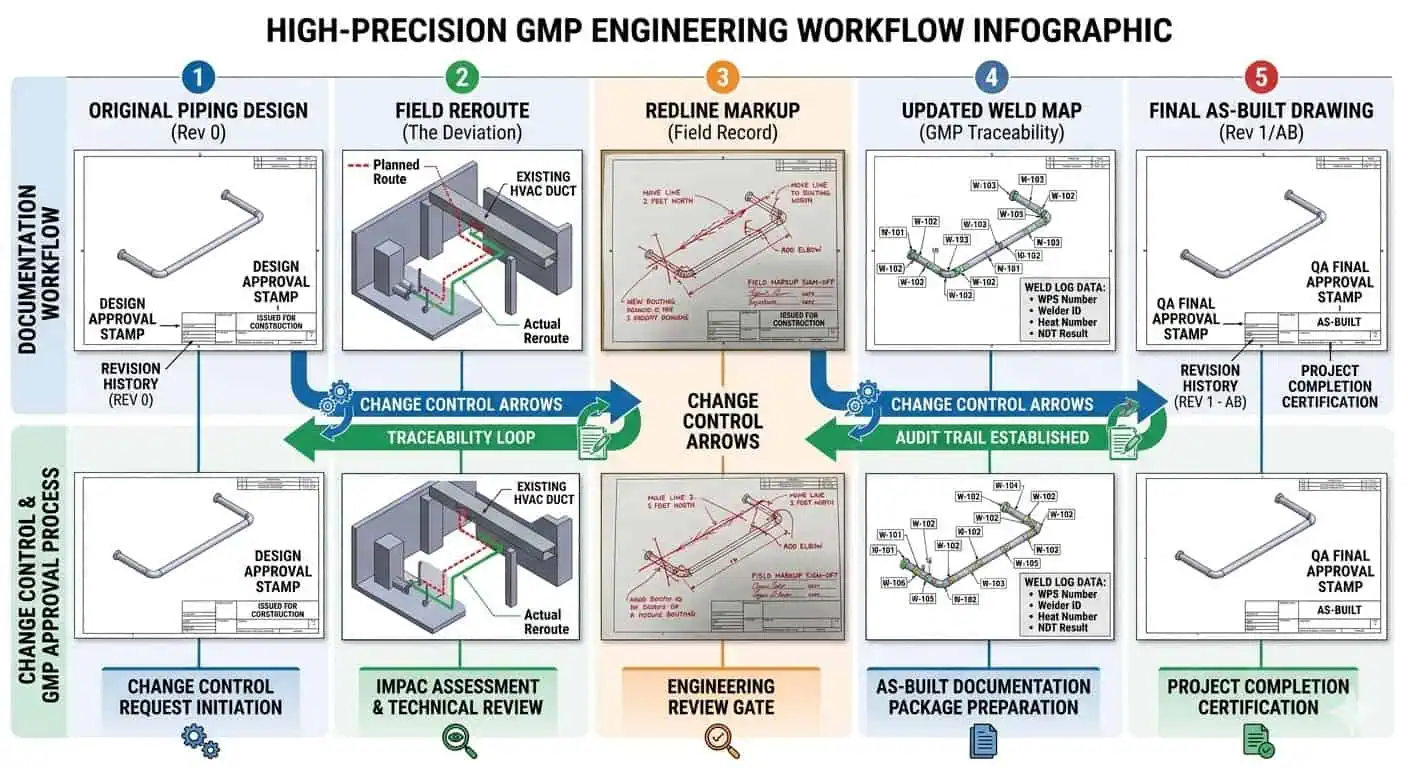
Экспертный совет: Перемаршрутизация на объекте - не настоящая проблема. Незакрытые свидетельства от перемаршрутизации на объекте - настоящая проблема. Проект должен рассматривать красные линии и документы по факту выполнения как активные инструменты контроля, а не как задачи черчения на конечном этапе.
Основной пакет документации, который обычно ожидают команды GMP
Документация по материалам
Документация по материалам доказывает, что одобренные контактирующие с продуктом материалы действительно вошли в систему. Как минимум, это обычно означает сертификаты материалов, прослеживаемость плавки, контроль приёмки и некоторую форму картографирования местоположения, которая связывает установленные компоненты с одобренным набором записей материалов. Чем серьёзнее последствия для гигиены или контакта с продуктом, тем менее приемлемо оставлять эту связь неопределённой.
Документация по изготовлению и сварке
Документация по изготовлению доказывает, как система стала тем, чем она является. Здесь обычно находятся карты сварных швов, журналы орбитальной сварки, результаты проверки сварки, истории ремонта, записи бороскопии, где требуется, и отслеживание статуса изготовления. Цель не в создании толстого досье ради самого себя. Цель в том, чтобы сохранить установленный контур проверяемым и технически защищаемым.
Документация по поверхности и обработке
Поверхностные записи имеют значение, когда обработка поверхности или пост-производственная обработка являются частью гигиенических требований. Если проект предусматривает электрополировку, пассивацию или определенную цель обработки поверхности, пакет сдачи должен показывать, как это требование было применено и как были идентифицированы соответствующие детали. В противном случае проект рискует иметь требование к обработке поверхности только на бумаге, без убедительных доказательств того, что установленная поверхность все еще соответствует ему.
Тестирование и документация по сдаче
Записи тестирования и сдачи превращают историю изготовления в доказательства выпуска. Испытания под давлением, испытания на герметичность, закрытие инспекции, завершение списка замечаний и сбор окончательного досье — это этапы, на которых проект демонстрирует, что изготовленный контур не только построен, но и проверен и закрыт таким образом, чтобы поддерживать работу в соответствии с GMP.
Типичный отраслевой случай: проект имеет все отдельные записи где-то, но сдача все еще задерживается, потому что пакет не структурирован так, как это необходимо отделу контроля качества для проверки и утверждения контура. Это не только проблема отсутствия документов. Это проблема логики досье.

Экспертный совет: если документы по сдаче собираются впервые только после механического завершения, проект уже опаздывает с точки зрения контроля документации.
Контроль изменений и записи об отклонениях
Документация по изменениям — это то, что делает окончательную цепочку доказательств убедительной. Проект должен показывать, что изменилось, кто утвердил изменения, какие проверки или доработки последовали, и как окончательное состояние после строительства учло эти изменения. Без этого даже технически обоснованные изменения на месте могут вызвать ненужные сомнения в контроле качества.
| Комплект документации | Что это доказывает | Где обычно возникают проблемы |
|---|---|---|
| Сертификаты на материалы и матрица прослеживаемости | Утверждённые контактирующие с рабочей средой материалы действительно были установлены | Карта расположения становится неясной после резки или перенаправления трубопровода на месте |
| Карты сварных швов и журналы сварки | Окончательные сварные швы были выполнены и проверены под контролем | Номера сварных швов перестают соответствовать окончательным ревизиям узлов |
| Отделка / ЭП / пассивационные записи | Указанное состояние поверхности достигнуто и сохранено | Доработки или поздние изменения отделки не полностью задокументированы |
| Красные линии и исполнительные схемы | Установленный контур соответствует окончательно утвержденной конфигурации | Изменения на месте происходят быстрее, чем закрытие чертежей |
| Досье сдачи | Полная цепочка доказательств готова для проверки ОК | Записи существуют, но не в структуре, готовой к выпуску |
Где обычно разрываются цепочки документации
Материал был правильным, но матрица прослеживаемости была слабой
Одной из самых распространенных проблем является не отсутствие материала, а слабое сопоставление материала с местом установки. Команды иногда полагают, что наличие сертификатов достаточно. Этого недостаточно, если проект не может быстро доказать, где оказался сертифицированный материал после резки, изготовления, сборки в секции и изменений на месте.
Сварные швы были приемлемыми, но комплект записей о сварке был неполным
Контур может быть технически исправным и все же не пройти документальное закрытие из-за неполного комплекта записей о сварке. Отсутствие статуса сварки, неясная история ремонта или несоответствие нумерации сварных швов обычно создают больше задержек, чем команды ожидают. В трубопроводах GMP, свидетельства о сварке — это не просто инструмент изготовления. Это часть готовности к сдаче.
Изменения на месте происходили быстрее, чем обновление документации
Документация часто отстает от проекта именно в тот момент, когда проект становится наиболее динамичным. Изменения маршрутизации на поздних стадиях, пересмотры врезок, корректировки подгонки на месте и добавленные ответвления часто происходят под давлением графика. Если комплект документов не успевает, итоговый пакет сдачи превращается в упражнение по восстановлению вместо контролируемой передачи.
Самые маленькие компоненты создали самую большую проблему с контролем качества
Малые контактирующие с продуктом детали создают непропорциональный риск для документации. Фасонные части, пробоотборные компоненты, диафрагмы, прокладки и контактирующие с продуктом детали приборов часто являются первым звеном, где нарушается цепочка доказательств чистоты. Команды обычно мыслят в терминах трубопроводных трасс, но отдел контроля качества часто сталкивается с проектом в виде неразрешенных локальных узлов.
Экспертный урок из работ по закрытию объекта: чем более локальным и заменяемым является узел, тем менее безопасно предполагать, что его записи позаботятся о себе сами.
Как инженеры должны формировать требования к документации до запроса предложений
Определите, что должно быть прослеживаемым
До запроса предложений определите, какие контактирующие с продуктом компоненты должны оставаться прослеживаемыми на протяжении монтажа и сдачи в эксплуатацию. Если контролируется только трубопровод, а более мелкие контактирующие с продуктом детали остаются неопределенными, цепочка доказательств обычно будет наиболее слабой там, где гигиенический узел наиболее сложен.
Определите, что должно регистрироваться во время изготовления
Проекты должны определять, что должно регистрироваться в процессе выполнения работ, а не только что должно существовать в конце. Журналы сварки, точки контроля, записи, связанные с отделкой, доказательства пассивации, где это уместно, и обновления изменений на месте должны быть частью определенного рабочего процесса проекта.
Определите, что отдел контроля качества должен получить при сдаче
Пакет сдачи должен быть определен как готовый к выпуску результат, а не как расплывчатая коллекция всего, что подрядчик сможет собрать позже. Если отдел контроля качества ожидает определенной структуры досье, матрицы прослеживаемости или формата записей, проект должен определить это, пока еще есть время для правильного создания этих записей.
Определите, что должно поддерживаться после запуска
Цепочка документации должна сохраняться в процессе эксплуатации, а не останавливаться на передаче. Журналы оборудования, записи технического обслуживания, прослеживаемость запасных частей и контролируемые обновления установленной системы — все это часть поддержания исходной цепочки доказательств. Система, готовая к выпуску, может стать гораздо сложнее для защиты позже, если записи жизненного цикла слабы.
Самый сильный совет по проекту прост: определите цепочку доказательств до закупок. Не ждите, пока начнется изготовление, чтобы решить, будет ли иметь значение прослеживаемость нагрева, записи отделки, статус сварки или документация по изменениям на месте. К этому моменту проект обычно собирает документы реактивно, а не контролирует их целенаправленно. Это один из самых ясных практических уроков из работ по сдаче в соответствии с GMP: проекты, которые определяют набор записей до запроса предложений, обычно закрываются быстрее и с меньшим количеством сюрпризов для отдела контроля качества, чем проекты, которые пытаются восстановить его позже.
Как это связано с проектированием, материалами и выбором фитингов
Выбор материала без контроля документации не является закрытым риском
Хорошее решение по материалам становится безопасным проектным решением только тогда, когда оно четко задокументировано. Для более широкой логики по материалам свяжите эту страницу с Выбор материалов для фармацевтических гигиенических трубопроводов.
Требования к отделке имеют значение только при их подтверждении
Электрополировка, целевые показатели отделки и ожидания после обработки не закрывают риск, если записи не подтверждают их. Свяжите эту тему с Электрополированная сталь 316L против стандартной стали 316L.
Фитинги и образцы сборок требуют собственной цепочки доказательств
Чем меньше и локальнее становится сборка, тем более вероятно, что ее документация станет самой слабой частью пакета сдачи. Свяжите эту тему с Выбор пищевых фитингов для объектов GMP.
Исполнительная документация должна отражать реальный риск очищаемости
Документация должна не только подтверждать, что было установлено. Она также должна отражать окончательную локальную гигиеническую реальность системы. Для этой логики свяжите эту страницу с Конструктивные особенности для систем промывки на месте (CIP) в пищевых трубопроводах.
Распространенные ошибки в документации и прослеживаемости для проектов фармацевтических трубопроводов
Рассмотрение документации как деятельности по сдаче вместо входных данных проектирования
Проекты, которые определяют пакет документации поздно, обычно заканчиваются перестройкой записей под давлением графика.
Отслеживание трубопроводов, но не отслеживание мелких смачиваемых компонентов
Самый слабый элемент прослеживаемости часто проявляется в фитингах, уплотнениях, диафрагмах или локальных сборках проб.
Хранение данных о сварке отдельно от логики выпуска на уровне линии
Записи о сварке гораздо менее полезны, если они не отображаются четко на окончательно установленный контур и его статус выпуска.
Позволяя красным линиям отклоняться от установленной реальности
Когда полевые изменения происходят быстрее, чем контролируемые обновления, пакет сдачи становится труднее доверять.
Предполагая, что отдел контроля качества примет это позже
В трубопроводах GMP отсутствие доказательств редко легче исправить в конце проекта, чем во время контролируемого выполнения.
Избыточный сбор документов, но недостаточное определение того, что действительно важно
Большие объемы документов не создают автоматически надежный пакет сдачи. Важно, достаточно ли четко набор записей доказывает установленную гигиеническую систему для выпуска и последующего контроля жизненного цикла.
Практический контрольный список: что спросить перед выпуском фармацевтической трубопроводной системы
До начала изготовления
- Какие контактирующие с продуктом компоненты должны быть прослеживаемыми?
- Какие записи должны создаваться во время изготовления?
- Какие доказательства сварки, отделки и инспекции потребуются отделу контроля качества позже?
- Как изменения на месте будут включены в контролируемые записи?
Перед механическим завершением
- Актуальны ли красные линии?
- Соответствуют ли установленные компоненты утвержденным записям материалов?
- Закрыты ли статусы сварки и история ремонтов?
- Завершены ли записи по отделке и обработке там, где это требуется?
Перед выпуском ОКК
- Соответствует ли пакет сдачи фактически установленному контуру?
- Остаются ли какие-либо локальные сборки неразрешенными в отношении прослеживаемости или записей инспекции?
- Может ли проект доказать окончательное состояние по факту установки достаточно четко для выпуска?
После запуска
- Как будут вестись журналы оборудования и записи о техническом обслуживании?
- Как будет обеспечиваться прослеживаемость запасных частей?
- Как будущие изменения будут связаны с исходной цепочкой доказательств?
| Этап проекта | Ключевой вопрос по документации | Как выглядит хороший контроль |
|---|---|---|
| До запроса предложений (RFQ) | Что должно быть прослеживаемым и поставляемым? | Набор записей определен, а не предполагается |
| В процессе изготовления | Создаются ли записи в режиме реального времени? | Записи о сварке, материалах, отделке и изменениях остаются актуальными |
| Перед сдачей | Соответствует ли досье фактической установке? | Исполнительная документация, прослеживаемость и закрытие инспекций согласованы |
| После запуска | Сохранится ли цепочка доказательств при изменениях в жизненном цикле? | Записи о техническом обслуживании и замене продолжают находиться под контролем |
Вывод: В фармацевтических трубопроводах документация доказывает, что система, которую вы думаете, что построили, является системой, которую вы фактически установили
Хорошая документация и прослеживаемость не добавляют ценности после проекта. Они защищают проект от невозможности выпуска в тот самый момент, когда он должен быть готов к запуску. В фармацевтических трубопроводах установленная система считается приемлемой только в той мере, в какой цепочка доказательств подтверждает, что её материал, изготовление, отделка, инспекция и изменения контролировались.
Самые успешные проекты не пытаются воссоздать эту цепочку доказательств при сдаче. Они определяют её до запроса предложений, поддерживают во время изготовления и завершают перед выпуском. Для полного кластера тем по фармацевтике свяжите эту статью с Выбор материалов для фармацевтических гигиенических трубопроводов, Электрополированная сталь 316L против стандартной стали 316L, Выбор пищевых фитингов для объектов GMP, и Конструктивные особенности для систем промывки на месте (CIP) в пищевых трубопроводах.
Часто задаваемые вопросы
Какая документация требуется для проектов фармацевтических трубопроводов?
Точный пакет документации зависит от объема проекта, но обычно она включает сертификаты на материалы, записи прослеживаемости, документацию по сварке, протоколы инспекции, доказательства отделки или обработки, где требуется, красные линии, исполнительные чертежи и записи сдачи, которые поддерживают выпуск ОК.
Какая прослеживаемость требуется в трубопроводах GMP?
Прослеживаемость должна следовать по смоченному пути. Это часто означает, что трубки, фитинги, клапаны, локальные сборки и другие критические компоненты, контактирующие с продуктом, должны быть прослеживаемы до утверждённых записей таким образом, чтобы они всё ещё соответствовали установленному состоянию.
Почему проекты фармацевтических трубопроводов терпят неудачу при сдаче?
Они часто терпят неудачу из-за неполной цепочки доказательств. Установка может быть физически приемлемой, но отсутствующие или слабые записи по материалам, сварке, отделке или исполнительным чертежам всё ещё могут задержать выпуск ОК.
Требуется ли прослеживаемость фитингов и прокладок в проектах GMP?
Во многих критических гигиенических применениях — да. Меньшие смоченные компоненты часто являются самым слабым звеном в документации, поэтому их не следует рассматривать как обычные расходные материалы, если они влияют на гигиенические характеристики или риск выпуска.
Требуются ли журналы сварки для пищевых трубопроводов в фармацевтике?
Проекты обычно полагаются на карты сварки и документацию по сварке, потому что они центральны для доказательства статуса изготовления и инспекции. Точный формат варьируется в зависимости от проекта, но слабая документация по сварке является одной из наиболее распространенных проблем при сдаче.
В чем разница между исполнительной документацией и документами на сдачу-приемку?
Исполнительная документация показывает окончательную установленную конфигурацию. Документы сдачи представляют собой более широкий пакет доказательств, используемый для поддержки выпуска, включая прослеживаемость, инспекцию, испытания и связанные проектные записи.




