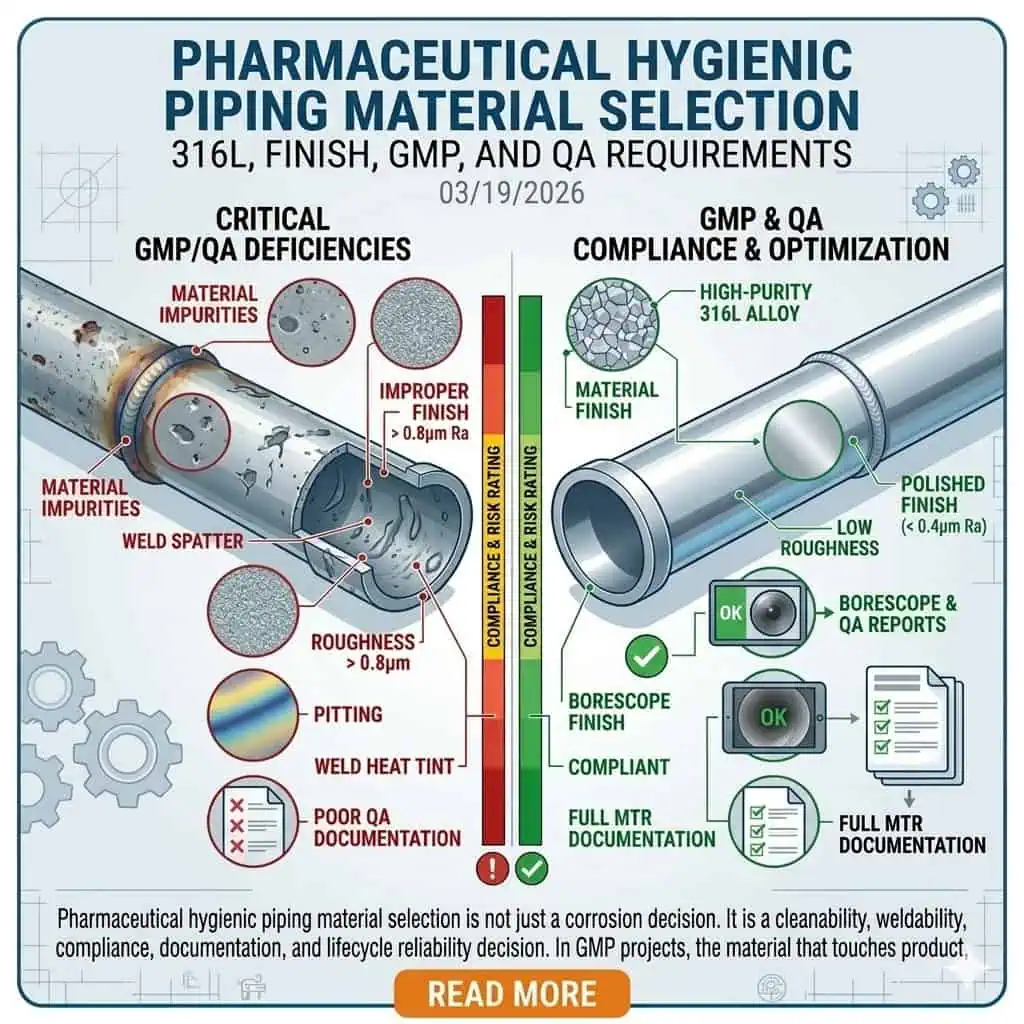
A seleção de materiais para tubulação higiênica farmacêutica não é apenas uma decisão sobre corrosão. É uma decisão sobre limpeza, soldabilidade, conformidade, documentação e confiabilidade do ciclo de vida. Em projetos de GMP, o material que entra em contato com o produto, fluidos do processo, água de alta pureza ou meios de limpeza deve fazer mais do que “resistir à ferrugem”. Deve permanecer não reativo, não aditivo, não absorvente, limpo, inspecionável e suportar fabricação repetível e liberação de QA. É por isso que engenheiros experientes não selecionam tubos e conexões apenas pelo nome da liga.
Na maioria dos sistemas de tubulação higiênica farmacêutica, o aço inoxidável 316L é a linha de base prática para serviço crítico de contato com produto metálico porque equilibra margem de corrosão, soldabilidade, aceitação da indústria e compatibilidade com práticas de fabricação de alta pureza. Isso não significa que cada linha, cada conexão ou cada montagem deva ser tratada da mesma forma. A decisão correta depende da química real do processo, regime de CIP/SIP, requisito de acabamento superficial, densidade de solda, sensibilidade à contaminação e do pacote de documentação necessário para entrega e validação.
Este guia explica como os engenheiros selecionam materiais para tubulação higiênica farmacêutica, onde o 316L faz sentido claro, onde o 316L padrão pode não ser suficiente sem o acabamento e qualidade de solda adequados, e onde a documentação e rastreabilidade se tornam tão importantes quanto o próprio metal. Em revisões reais de projetos, a decisão final de material raramente é alterada por uma grande falha. Geralmente é alterada por um padrão de problemas menores: uma solda mais difícil de inspecionar do que o esperado, um registro de acabamento que não fecha limpo com QA, um ramo de amostra que sofre ciclos de SIP mais severos do que o resto do loop, ou uma montagem local que se comporta como uma zona de maior risco do que o P&ID sugeria.
O que a Seleção de Materiais para Tubulação Higiênica Farmacêutica Realmente Significa
A Escolha do Material é uma Decisão de GMP e Controle de Contaminação
Em sistemas farmacêuticos, a seleção de materiais é parte do controle de contaminação. Um tubo, corpo de válvula, anel de compressão ou conexão não é aceito porque parece sanitário. É aceito porque a superfície de contato com o produto pode suportar o processo pretendido sem alterar segurança, identidade, força, qualidade ou pureza. Esse princípio está alinhado com FDA 21 CFR 211.65, o que exige que as superfícies em contato com o produto sejam não reativas, não aditivas e não absorventes.
Na prática, isso significa que os engenheiros revisam a escolha do material juntamente com o acabamento da superfície, a condição da solda, a drenabilidade, a passivação, a química de limpeza e a acessibilidade para inspeção. Uma liga correta com purga de solda deficiente, condição de superfície não controlada ou documentação fraca ainda pode se tornar um problema de GMP. Uma lição comum de campo é que um pacote de tubulação pode parecer tecnicamente aceitável na liberação de fabricação e ainda se tornar difícil durante a qualificação porque a decisão do material foi tratada como um item de compra, em vez de uma decisão de controle de contaminação.
Nota de engenharia: em trabalhos de GMP, a pergunta não é apenas “Essa liga sobreviverá?” mas também “Essa superfície finalizada, soldada e documentada se comportará de forma previsível na inspeção, limpeza e liberação de QA?”
Por que a Seleção de Tubulação Farmacêutica é Diferente do Serviço Sanitário Geral
A tubulação higiênica farmacêutica geralmente é mantida em um padrão mais rigoroso do que o serviço sanitário geral de alimentos ou utilidades. O motivo não é apenas o valor do produto. É a consequência da contaminação, retenção de resíduos, substituições não documentadas, fabricação inconsistente e liberação atrasada de QA em ambientes validados. O mesmo grau de aço inoxidável pode ser aceitável em uma aplicação sanitária geral, mas ainda ficar aquém em um sistema GMP se a consistência do acabamento, registros de solda ou rastreabilidade não forem controlados no nível que o projeto exige.
É por isso que a revisão de materiais em projetos farmacêuticos deve estar ao lado da seleção de conexões, controle de trechos mortos, aceitação de solda e planejamento de entrega de QA. Uma liga correta na montagem errada ainda é o resultado de engenharia errado.
Quais Padrões Realmente Impulsionam a Decisão
Os padrões mais úteis são aqueles que mudam o que você especifica, inspeciona e aceita. Em tubulação higiênica farmacêutica, as referências mais relevantes geralmente incluem:
- ASME BPE para materiais, projeto, fabricação, inspeção, teste e lógica de certificação em equipamentos de bioprocessamento e farmacêuticos.
- FDA 21 CFR 211.65 para construção de equipamentos e adequação da superfície de contato com o produto.
- FDA 21 CFR 211.67 para expectativas de limpeza e manutenção.
- ASTM A270/A270M para tubulação de grau alimentício, incluindo a opção de especificar qualidade farmacêutica como um requisito suplementar.
- EU GMP Anexo 1 para controle de contaminação, gerenciamento de risco de qualidade e expectativas de fabricação estéril.
O trabalho do engenheiro é transformar esses requisitos em decisões reais de material, acabamento, solda e documentação que possam sobreviver à aquisição, fabricação, inspeção, partida e revisão de QA. Em projetos sólidos, os padrões não são citados no final para justificar uma escolha finalizada. Eles são traduzidos no início em linguagem de RFQ, critérios de inspeção, requisitos de entrega e limites de controle de mudanças.
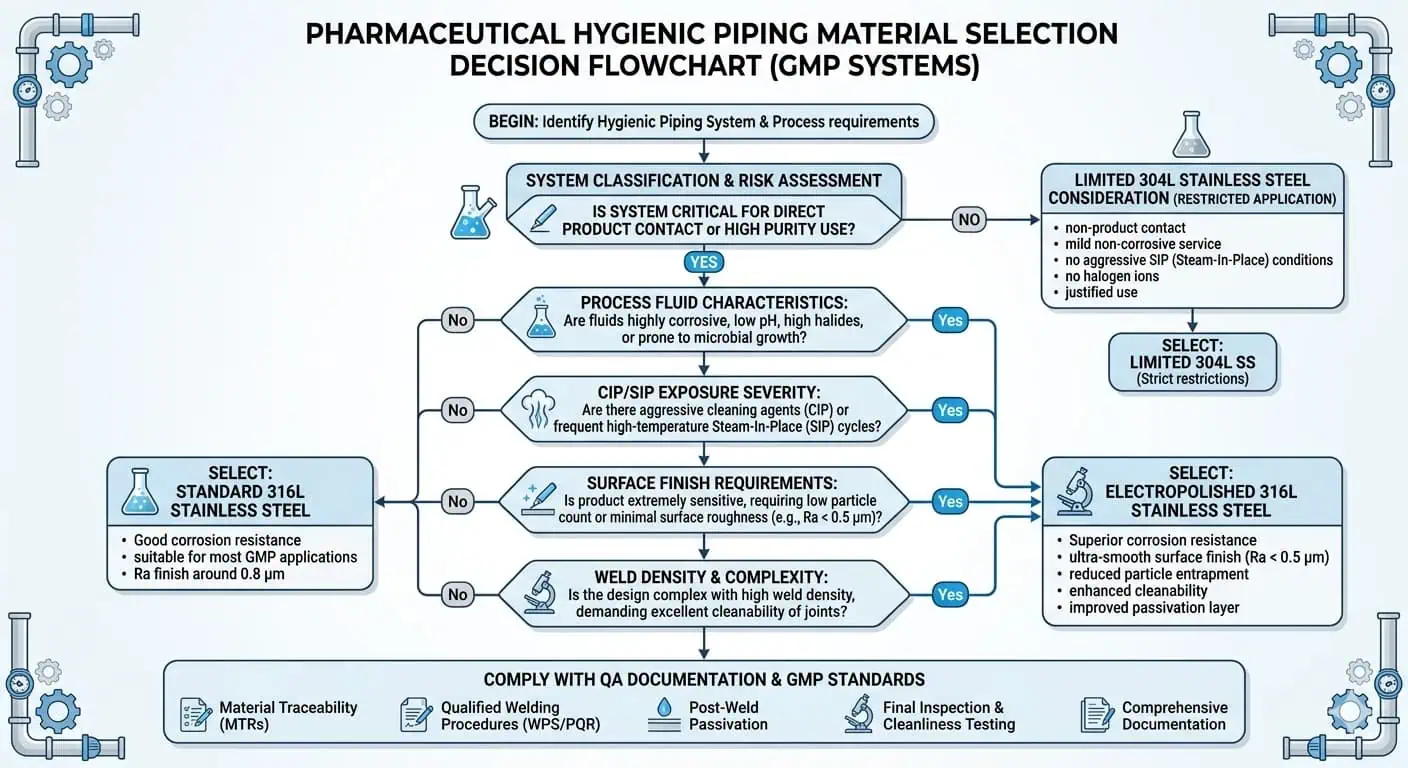
As Famílias de Materiais Principais Usadas em Tubulação Sanitária Farmacêutica
Por que o 316L É a Base Prática para Muitos Sistemas Sanitários GMP
O aço 316L é comumente tratado como o material metálico de referência para tubulações higiênicas críticas na indústria farmacêutica, pois oferece uma combinação prática de resistência à corrosão, soldabilidade e ampla aceitação no setor. O grau de baixo carbono suporta a fabricação higiênica soldada de forma mais confiável do que o 316 padrão em muitas condições de processo, e a composição com molibdênio melhora a resistência à corrosão localizada em comparação com o 304/304L em ambientes de limpeza e serviço mais exigentes.
Isso não torna o 316L uma solução mágica. Significa que o 316L é frequentemente o ponto de partida mais defensável para tubulações metálicas em contato com produtos quando o sistema também deve atender a expectativas de fabricação e documentação de alta pureza. Em projetos reais, os engenheiros muitas vezes escolhem o 316L não porque cada seção do sistema seja quimicamente severa, mas porque o risco total do projeto é suportado por conjuntos soldados, limpeza local, exposição a SIP/CIP e expectativas de validação em conjunto.
Quando o 304/304L ainda pode aparecer—e por que é frequentemente limitado
O 304 ou 304L ainda pode aparecer em alguns projetos farmacêuticos, mas geralmente em funções mais limitadas. Serviços auxiliares de baixo risco, sistemas legados, áreas de suporte não críticas ou projetos históricos orientados por custos ainda podem usar materiais da família 304. Mas em tubulações higiênicas críticas em contato com produtos, a indústria geralmente se move em direção ao 316L porque o risco total é mais amplo do que apenas a corrosão em massa.
Este é um dos erros de especificação mais comuns em projetos em estágio inicial: tratar a escolha entre 304 e 316L como uma simples questão de preço, em vez de uma escolha baseada em limpeza, fabricação e risco de QA. Na prática, quando uma equipe pergunta se o 304L ainda pode ser usado, a melhor pergunta de acompanhamento geralmente é: usado onde, sob qual regime de limpeza, com qual requisito de acabamento e sob qual padrão de documentação?
Onde os materiais não metálicos ainda importam
A seleção de materiais para tubulações farmacêuticas não para na parede do tubo. Diafragmas, assentos de válvula, juntas, mangueiras e outras partes molhadas não metálicas frequentemente determinam se o conjunto final funciona conforme o planejado. PTFE, PTFE modificado, EPDM, FKM, silicone ou compostos específicos para aplicação podem estar envolvidos, dependendo da química, temperatura, exposição a SIP e requisitos de validação.
Em muitos desvios de GMP, o ponto fraco não é o tubo de aço inoxidável. É o material da interface que foi tratado como um consumível menor em vez de um componente molhado controlado. Um exemplo comum é um sistema metálico quimicamente compatível emparelhado com um material de vedação que envelhece mais rápido sob SIP repetido do que a revisão de risco original assumiu. A lição não é que a seleção do metal estava errada isoladamente; é que o sistema molhado não foi revisado como um todo.
Como os Engenheiros Decidem Entre 316L Padrão, 316L Eletropolidos e Opções de Especificação Superior
316L Padrão vs 316L Eletropolidos
316L Padrão e 316L eletropolidos não são famílias de ligas concorrentes. São decisões diferentes de condição de superfície construídas na mesma família de material base. 316L Padrão pode ser totalmente aceitável onde o acabamento necessário, a capacidade de limpeza e as expectativas de inspeção são moderadas. 316L Eletropolidos torna-se mais atraente onde a consistência da superfície, o comportamento de liberação de resíduos, a capacidade de inspeção e os requisitos de capacidade de limpeza de alta pureza são mais rigorosos.
A melhor pergunta não é “O eletropolidos é melhor?” mas “Este processo precisa das vantagens relacionadas ao acabamento suficientemente para justificar o requisito mais rigoroso?” Em revisões de engenharia reais, o eletropolidos é frequentemente selecionado não porque o 316L Padrão falhou em todos os lugares, mas porque o processo exigia uma superfície mais controlada para confiança na inspeção, resposta a resíduos ou disciplina operacional de alta pureza. Para a discussão detalhada sobre acabamento, conecte este artigo com Aço Inoxidável 316L Eletropolidado vs 316L Padrão.
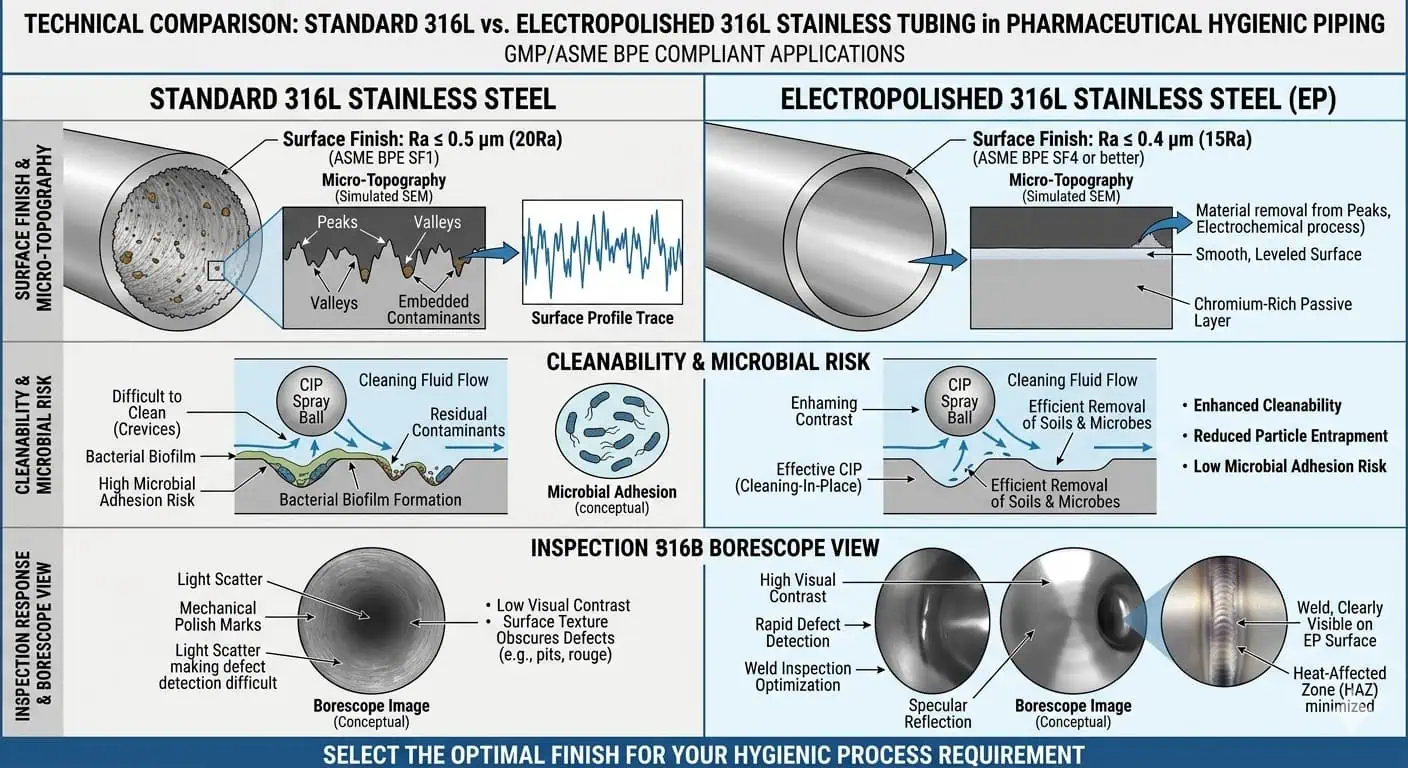
Quando o Acabamento de Superfície Altera o Desempenho Higiênico Real
O acabamento de superfície não é uma atualização cosmética em serviço farmacêutico. Ele altera a capacidade de limpeza, a resposta à inspeção e o comportamento de retenção de resíduos. Um requisito de acabamento é mais importante onde o processo é sensível a resíduos, onde a repetibilidade de SIP/CIP é crítica, onde a inspeção de contato com o produto é rigorosa ou onde a geometria local torna qualquer defeito de superfície mais consequente.
Em ambientes de alta pureza e biofarmacêuticos, os engenheiros não separam a seleção de liga da seleção de acabamento porque o resultado higiênico é criado por ambos juntos. Uma lição repetida de investigações de campo é que um sistema pode usar a liga correta e ainda ter desempenho inferior se a condição de acabamento local variar mais do que o modelo de risco permitiu.
Quando uma Revisão de Liga Superior ou Material Especial é Justificada
Às vezes, o 316L ainda não é suficiente, mas essa decisão deve vir da química e do mecanismo de falha, não do hábito. Exposição mais agressiva a haletos, sistemas de solventes incomuns, química de processo forte ou histórico de falhas repetidas podem justificar uma revisão de liga superior. Essa etapa deve ser baseada em dados reais de serviço, revisão do mecanismo de corrosão e química do processo, não em uma suposição genérica de que “a farmacêutica sempre usa o grau mais alto disponível”.”
O conselho de especialistas aqui é direto: não aumente a liga porque o sistema é “importante”. Aumente-a apenas quando você puder definir o modo de falha que está tentando prevenir e o motivo pelo qual a opção de base não fornece margem suficiente.
Seleção de Material por Área de Processo em Instalações Farmacêuticas
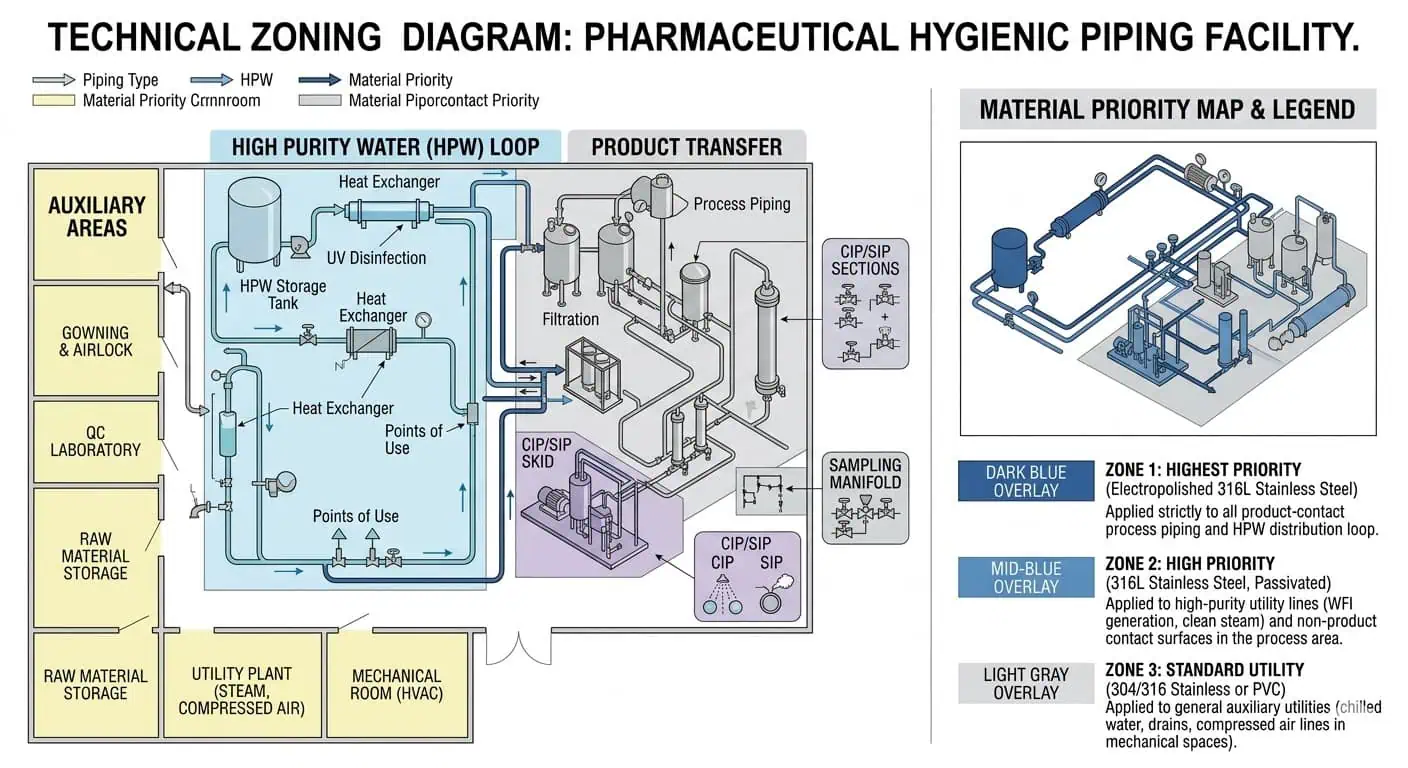
Sistemas Relacionados a Água de Alta Pureza e Utilidades Limpas
A água de alta pureza e circuitos de utilidades limpas relacionados exercem pressão sobre a consistência do material, qualidade da solda e estabilidade superficial de longo prazo. Nesses sistemas, a decisão sobre o material está intimamente ligada à tendência de formação de ferrugem, consistência do acabamento, aceitação da solda e compatibilidade com sanitização. As especificações mais rigorosas geralmente se concentram menos apenas no nome da liga e mais em se o conjunto completo de tubulação e solda pode suportar um desempenho higiênico estável e repetível ao longo do tempo.
Nota típica de engenharia: em circuitos de água de alta pureza, a primeira preocupação geralmente não é a corrosão generalizada da parede. É a inconsistência local do acabamento, a condição da solda ou a restauração incompleta da superfície de contato com o produto após fabricação e retrabalho. É por isso que engenheiros que já viram investigações repetidas de circuitos tendem a focar precocemente na execução da solda e nas evidências de acabamento, não apenas na designação da liga.
Linhas de Processo e Conjuntos de Transferência em Contato com o Produto
Linhas de processo em contato com o produto geralmente justificam o pensamento mais conservador sobre materiais. É aqui que corrosão, alteração superficial, preocupação com extraíveis ou inconsistência de fabricação podem ter o efeito mais direto na qualidade do produto e na confiança do lote. O grau do material, acabamento, interfaces de conexões e pacote de documentação devem ser todos definidos antes da RFQ, não esclarecidos após a fabricação.
Em termos de projeto, é aqui que “aceitável para uso sanitário geral” e “aceitável para uso validado em contato com o produto” se separam mais claramente. A penalidade por esclarecimento tardio geralmente não é apenas retrabalho técnico, mas atraso no FAT, SAT ou fechamento de QA.
Seções Expostas a CIP/SIP
Seções expostas a CIP/SIP frequentemente revelam fraquezas do material mais rapidamente do que o próprio processo. Ciclos repetidos de água quente, vapor limpo, cáustico, ácido, sanitizante e resfriamento alteram significativamente o ambiente de serviço. Na prática, muitos problemas relacionados a materiais em tubulações farmacêuticas não são revelados primeiro pelo produto; são revelados por ciclos repetidos de limpeza e esterilização.
Esta é uma das razões pelas quais um engenheiro deve revisar os materiais molhados metálicos e não metálicos juntos sempre que o sistema é submetido a ciclos repetidos de SIP/CIP. Um padrão comum no campo é que a tubulação permanece aceitável, enquanto uma vedação local, assento ou conjunto de ramificação envelhece mais rápido do que o esperado sob o ciclo térmico e químico real.
Válvulas de Amostragem, Colectores de Válvulas e Outros Conjuntos Locais de Alto Risco
As decisões de material mais difíceis geralmente estão nos conjuntos locais, não nos trechos retos de tubulação. Válvulas de amostragem, colectores de distribuição, conexões de ramificação, válvulas de diafragma e tês de instrumentação combinam maior densidade de solda, mais interfaces, mais risco de pernas mortas e maior sensibilidade de inspeção. É aqui que o pacote higiênico total importa mais.
É por isso que este artigo deve se conectar diretamente com Seleção de Conexões de Grau Alimentício para Instalações GMP. Na indústria farmacêutica, a liga correta no conjunto errado ainda é o resultado errado. Engenheiros que solucionam problemas nesses sistemas regularmente sabem que a linha raramente falha “em todos os lugares”. Ela falha primeiro no detalhe local que foi tratado como normal quando, na verdade, era o ponto de maior risco no circuito.
Soldabilidade, Condição da Superfície e Tratamento Pós-Fabricação
Por que a Densidade de Solda Altera o Risco do Material
Quanto mais soldas um sistema higiênico contém, menos útil é falar sobre a escolha do material como se apenas o tubo base importasse. Zonas afetadas pelo calor da solda, qualidade do purga, condição do cordão interno, consistência da solda orbital e histórico de retrabalho influenciam se o sistema final se comporta como um ativo GMP limpo ou uma fonte de desvio recorrente.
Um sistema com excelente escolha de liga, mas com execução de solda deficiente, ainda é um sistema farmacêutico fraco. Em termos práticos, cada solda adicionada aumenta a importância da disciplina de fabricação, não apenas a importância do certificado da liga.
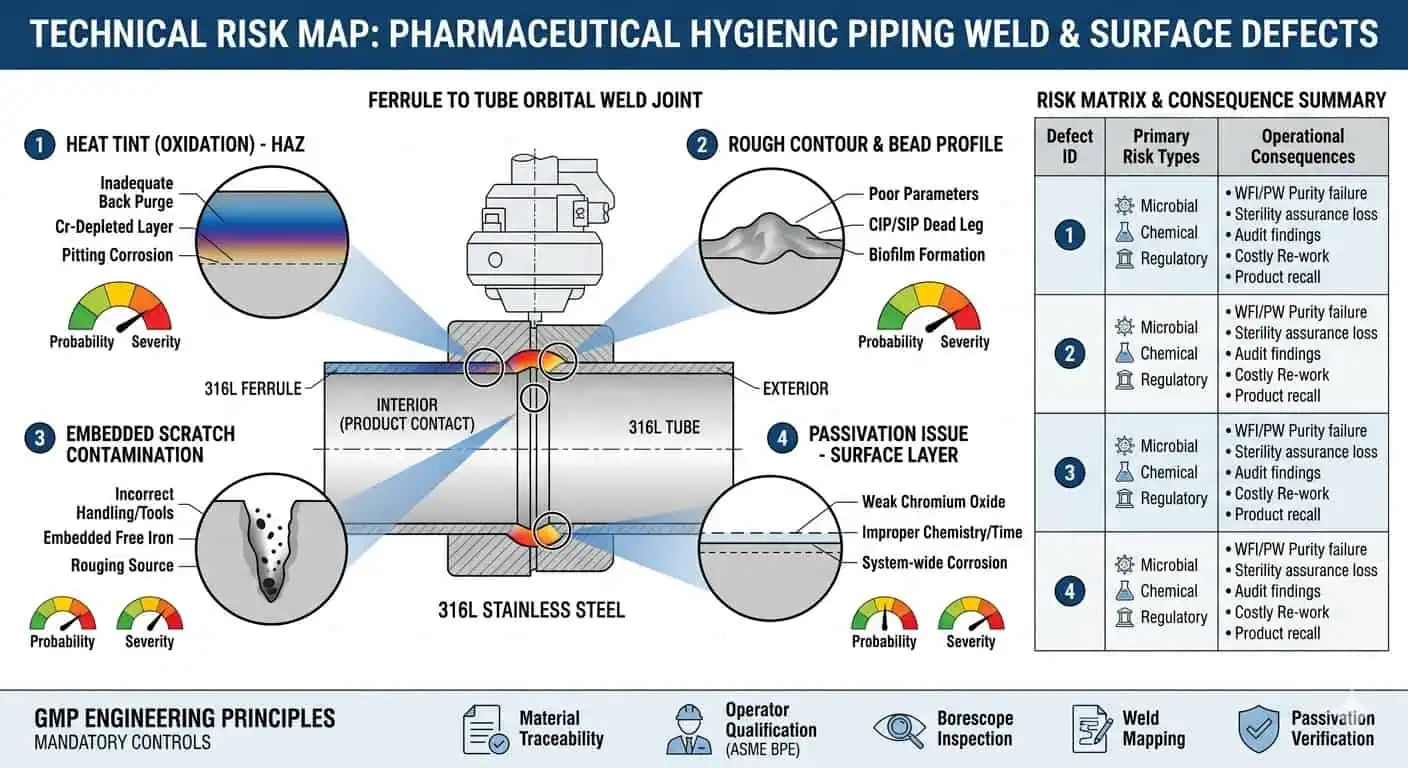
Por que Defeitos de Superfície Podem Derrotar uma Boa Escolha de Material
Uma liga correta não resgata uma superfície de contato com o produto deficiente. Irregularidades de superfície, descoloração de solda, contorno deficiente, arranhões, contaminação por manuseio na fabricação ou retrabalho não controlado podem reduzir o valor higiênico de uma boa seleção de material. É aqui que os engenheiros frequentemente veem a primeira lacuna entre a intenção da especificação e a realidade instalada.
Caso típico da indústria: O projeto especificou corretamente 316L para um circuito crítico de contato com o produto, mas o pacote de entrega ainda desencadeou preocupação porque a aparência local da solda, a consistência do acabamento e a revisão por boroscópio não suportavam o padrão higiênico reivindicado. A liga não era o problema. A condição da superfície fabricada era.
Esse caso é comum o suficiente para importar. É uma das razões pelas quais revisores experientes não aprovam mentalmente um circuito apenas porque o certificado de teste de material parece correto.
Passivação, Compatibilidade de Limpeza e Estabilidade de Longo Prazo
A passivação e o tratamento pós-fabricação fazem parte da estratégia de material, não são um toque final opcional. Um material que é correto no papel, mas mal acabado, mal limpo após a fabricação ou inadequadamente restaurado após o trabalho de solda, não terá o desempenho pretendido para o material especificado. Isso importa ainda mais em sistemas com limpeza repetida, sanitização e escrutínio de validação.
Conselho especializado aqui é simples: nunca trate a condição da superfície pós-fabricação como um item cosmético de fechamento. Em serviço farmacêutico higiênico, isso faz parte do desempenho técnico da própria decisão do material.
Documentação e Rastreabilidade: Por Que a Seleção de Materiais Também é uma Decisão de QA
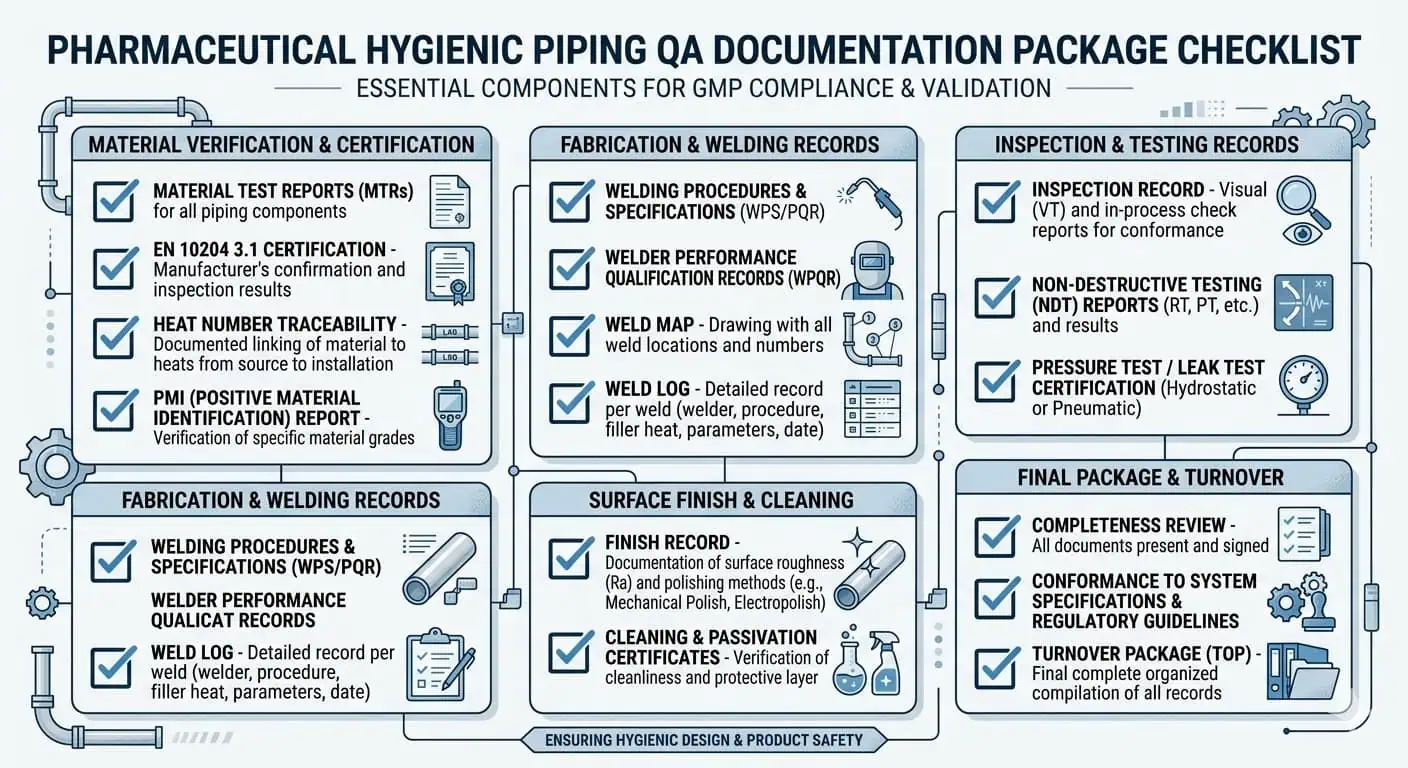
O Que o QA Geralmente Quer Ver
Em projetos de tubulação GMP, o material correto é apenas metade da resposta. O QA geralmente precisa de provas. Dependendo do escopo do projeto, isso pode incluir números de forno, certificados de teste de material, certificados EN 10204 3.1, registros PMI quando exigidos, registros de acabamento superficial, mapas de solda, registros de solda, registros de inspeção e documentação de entrega que vincula o conjunto instalado à especificação aprovada.
O pacote exato varia por projeto, mas o padrão é consistente: se a escolha do material não puder ser rastreada e verificada, ela permanece um risco do projeto. É aqui que muitos pacotes tecnicamente capazes perdem tempo durante a entrega: não porque a metalurgia estava errada, mas porque a cadeia de evidências era mais fina do que o ambiente GMP exigia.
Por Que “Material Correto” Sem Registros Ainda é um Risco de Projeto
Uma das falhas mais comuns em projetos farmacêuticos não é a seleção errada de liga. É o fechamento incompleto da cadeia de evidências. A tubulação pode estar correta. As conexões podem estar corretas. As soldas podem até ser aceitáveis. Mas se a rastreabilidade, registros de acabamento ou documentação de inspeção estiverem incompletos, a liberação do QA ainda pode parar.
Caso típico da indústria: Um pacote de tubulação GMP passou na revisão de fabricação, mas falhou na prontidão de entrega porque a rastreabilidade de forno e os registros de acabamento para um grupo de peças de tubulação de grau alimentício estavam incompletos. O problema não era metalurgia técnica. Era controle de documentação.
É por isso que engenheiros experientes tratam a documentação como parte da seleção de materiais desde o início, não como um exercício burocrático para o final do projeto.
Como Definir Requisitos de Materiais Antes da RFQ
O melhor momento para definir as expectativas de materiais é antes da RFQ, não durante a revisão da lista de pendências. Uma RFQ forte geralmente define o grau da liga, o padrão da tubulação, o alvo de acabamento, os requisitos de solda, as expectativas de passivação, os entregáveis de documentação e quaisquer requisitos específicos de inspeção para aceitação.
Para o lado completo de QA desse tópico, conecte este artigo com Documentação e Rastreabilidade em Projetos de Tubulação Farmacêutica.
Exemplos de Pesquisa, Casos da Indústria e Conselhos de Especialistas
Caso de Engenharia Típico 1: 316L Estava Correto, mas a Zona de Solda Falhou na Intenção Higiênica
Esta é uma das falhas mais realistas em tubulação farmacêutica. A equipe de projeto escolheu a família de liga correta, mas a zona de solda instalada não preservou a intenção higiênica da escolha do material. A preocupação resultante pode aparecer como inconsistência de acabamento, falha na inspeção, resposta de limpeza difícil ou hesitação do QA sobre a qualidade local de contato com o produto.
A lição é direta: na farmacêutica, a seleção de materiais e a execução da solda não podem ser separadas. Os sistemas mais fortes não são aqueles com a descrição de material mais cara. São aqueles em que o material, acabamento, fabricação e lógica de inspeção apoiam o mesmo alvo higiênico.
Caso de Engenharia Típico 2: O Problema de QA Era Documentação, Não a Liga
Outro modo de falha comum aparece durante a entrega. O projeto usou o grau de material correto, mas o pacote carecia dos registros necessários para comprovar conformidade. Certificados ausentes, rastreabilidade pouco clara, registros de acabamento incompletos ou documentação de solda fraca podem atrasar a aprovação mesmo quando o metal instalado está tecnicamente correto.
É por isso que engenheiros experientes tratam a documentação como parte da seleção de materiais desde o início. No trabalho prático de GMP, uma escolha correta não documentada ainda é uma escolha incompleta.
Caso de Engenharia Típico 3: O Eletropolimento Era Necessário Devido à Limpeza, Não Porque o 316L Estava “Errado”
Às vezes, o 316L padrão não é rejeitado porque a liga é inadequada, mas porque o requisito de acabamento alterou o alvo higiênico. Nesses casos, a melhor resposta não é dizer que o projeto escolheu a família de metal errada. A melhor resposta é que o projeto eventualmente reconheceu um requisito de limpeza e inspecionabilidade mais rigoroso do que o especificado originalmente no acabamento.
Isso é um refinamento de engenharia normal, não uma vergonha. É exatamente como uma equipe de processo forte melhora a precisão da especificação ao longo do tempo.
Conselho de Especialista: Pergunte Qual Falha Você Está Realmente Tentando Evitar
A melhor pergunta de seleção de material não é “Qual grau a maioria das pessoas usa?” É “Que falha estamos tentando prevenir neste sistema específico?” A resposta pode ser corrosão. Pode ser risco de enferrujamento. Pode ser preocupação com extraíveis. Pode ser limpeza orientada pelo acabamento. Pode ser inconsistência de solda. Pode ser falha no fechamento de QA. Uma vez que esse modo de falha esteja claro, a decisão do material se torna muito mais racional.
Esse é o conselho mais consistente de engenheiros que trabalharam com desvios reais em tubulações farmacêuticas: defina o modo de falha primeiro, e a lógica do material se torna mais clara, mais restrita e mais fácil de defender.
Erros Comuns na Seleção de Materiais para Tubulações Sanitárias Farmacêuticas
Escolher Apenas pelo Nome da Liga
A família da liga importa, mas o resultado sanitário instalado depende também do acabamento, soldas, geometria, interfaces e documentação.
Separar Grau do Acabamento de Superfície
316L padrão e 316L eletropolidos não são intercambiáveis se o alvo sanitário for definido por limpeza relacionada ao acabamento e expectativas de inspeção.
Ignorar Soldabilidade e Realidade de Fabricação
Um material base correto com execução de solda ruim ainda é um pacote de tubulação GMP fraco.
Tratar a Documentação como um Problema Pós-Aquisição
Em projetos farmacêuticos, a documentação faz parte da aceitação, não é uma reflexão tardia para a entrega.
Usando a Regra de Um Material para Cada Área de Processo
Circuitos de água de alta pureza, transferências de contato com o produto, seções expostas a CIP/SIP e áreas auxiliares não têm todas a mesma consequência higiênica ou de conformidade.
Lista de Verificação Prática para Seleção de Materiais de Tubulação Higiênica Farmacêutica
Perguntas a Responder Antes da Aprovação Final do Material
- Qual fluido ou produto de processo realmente entra em contato com a superfície?
- Qual exposição CIP/SIP o sistema realmente enfrentará?
- Qual nível de acabamento é necessário para limpeza e inspeção?
- Quais conjuntos locais apresentam o maior risco de contaminação ou retenção?
- Qual pacote de documentação é necessário para liberação de QA?
- O padrão 316L é suficiente, ou o requisito de acabamento e fabricação altera a resposta?
O que Definir na RFQ
- Grau da Liga
- Padrão da Tubulação
- Requisito de Acabamento Superficial
- Critérios de Aceitação de Solda
- Expectativas de Passivação / Pós-fabricação
- Certificados e Entregáveis de Rastreabilidade
- Requisitos de Inspeção para Liberação
Conclusão: Boa Seleção de Material Farmacêutico é uma Decisão de Sistema, Não uma Compra de Metal
Boa seleção de material para tubulação higiênica farmacêutica é uma decisão de sistema, não uma compra de metal. Os projetos mais robustos escolhem materiais considerando juntos a resistência à corrosão, acabamento, soldabilidade, regime de limpeza, documentação de QA e risco do processo. É por isso que o 316L é tão comum em tubulações higiênicas críticas de GMP, mas também por isso que o 316L sozinho nunca é a resposta completa.
Se você deseja um cluster de tópicos farmacêuticos mais limpo, conecte este artigo com Aço Inoxidável 316L Eletropolidado vs 316L Padrão, Seleção de Conexões de Grau Alimentício para Instalações GMPe Documentação e Rastreabilidade em Projetos de Tubulação Farmacêutica.
PERGUNTAS FREQUENTES
A liga 316L é sempre necessária em tubulações de grau alimentício farmacêutico?
Não. O 316L é a linha de base prática para muitos sistemas higiênicos críticos farmacêuticos, mas a escolha final ainda depende da química do processo, requisito de acabamento, densidade de solda, expectativas de validação e risco do projeto.
Qual é a diferença entre o aço 316L eletropolidido e o 316L padrão em serviço farmacêutico?
A família de liga base pode ser a mesma, mas a condição da superfície não é. O 316L eletropolidado é escolhido onde são necessários maior consistência de acabamento, limpeza e inspecionabilidade.
304L ainda pode ser usado em projetos de tubulação farmacêutica?
Às vezes. Ele ainda pode aparecer em aplicações de baixo risco ou legadas, mas sistemas críticos de contato com produto higiênicos de GMP frequentemente migram para o 316L porque a decisão é mais ampla do que apenas o custo da corrosão.
Por que a documentação faz parte da seleção de materiais em projetos de GMP?
Porque a liberação de QA depende de prova, não apenas de intenção. Um material correto sem rastreabilidade, certificados e registros de inspeção relacionados ainda é um risco para o projeto.
Quais padrões são mais importantes ao selecionar materiais de tubulação de grau alimentício para farmacêutica?
ASME BPE, FDA 21 CFR 211.65 e 211.67, ASTM A270 e o framework GMP incluindo o Anexo 1 estão entre os pontos de partida mais úteis. Eles moldam como os engenheiros definem materiais, qualidade de fabricação, capacidade de limpeza e expectativas de documentação.
A seleção adequada da liga elimina a necessidade de controle de solda e acabamento?
Não. Uma liga correta com consistência de acabamento deficiente, qualidade de solda fraca ou tratamento pós-fabricação incompleto ainda pode falhar na intenção higiênica do projeto.


