
La progettazione di tubazioni ad alta purezza per impianti biotecnologici non è solo un esercizio di tracciamento. È una decisione di controllo della contaminazione, pulibilità, saldabilità, drenabilità e validazione. Nella produzione biotecnologica, un sistema di tubazioni fa più che spostare fluidi da un recipiente all'altro. Deve proteggere l'integrità del processo, supportare la pulizia e sterilizzazione ripetibili, minimizzare il rischio microbiologico e di residui, rimanere ispezionabile dopo la fabbricazione e resistere al carico di documentazione e qualificazione di un ambiente regolamentato.
Ecco perché una buona progettazione di tubazioni ad alta purezza inizia con la geometria, non con l'aspetto. Un sistema può apparire igienico su un P&ID e comunque fallire in esercizio se la disposizione dei rami crea tratti morti, la pendenza non drena come installata, la strategia di saldatura è irrealistica o le valvole locali e gli assemblaggi di campionamento sono più difficili da pulire della linea principale. Negli impianti biotecnologici, il dettaglio igienico più debole di solito conta più del tratto rettilineo più pulito.
Questa guida spiega come gli ingegneri progettano tubazioni ad alta purezza per impianti biotecnologici, dove le decisioni su 316L e finitura superficiale contano veramente, come il controllo dei tratti morti e la drenabilità modellano il layout, perché la progettazione della saldatura non può essere separata dalla progettazione delle tubazioni e come le aspettative di manutenzione e validazione dovrebbero essere integrate nel sistema prima dell'inizio della fabbricazione.
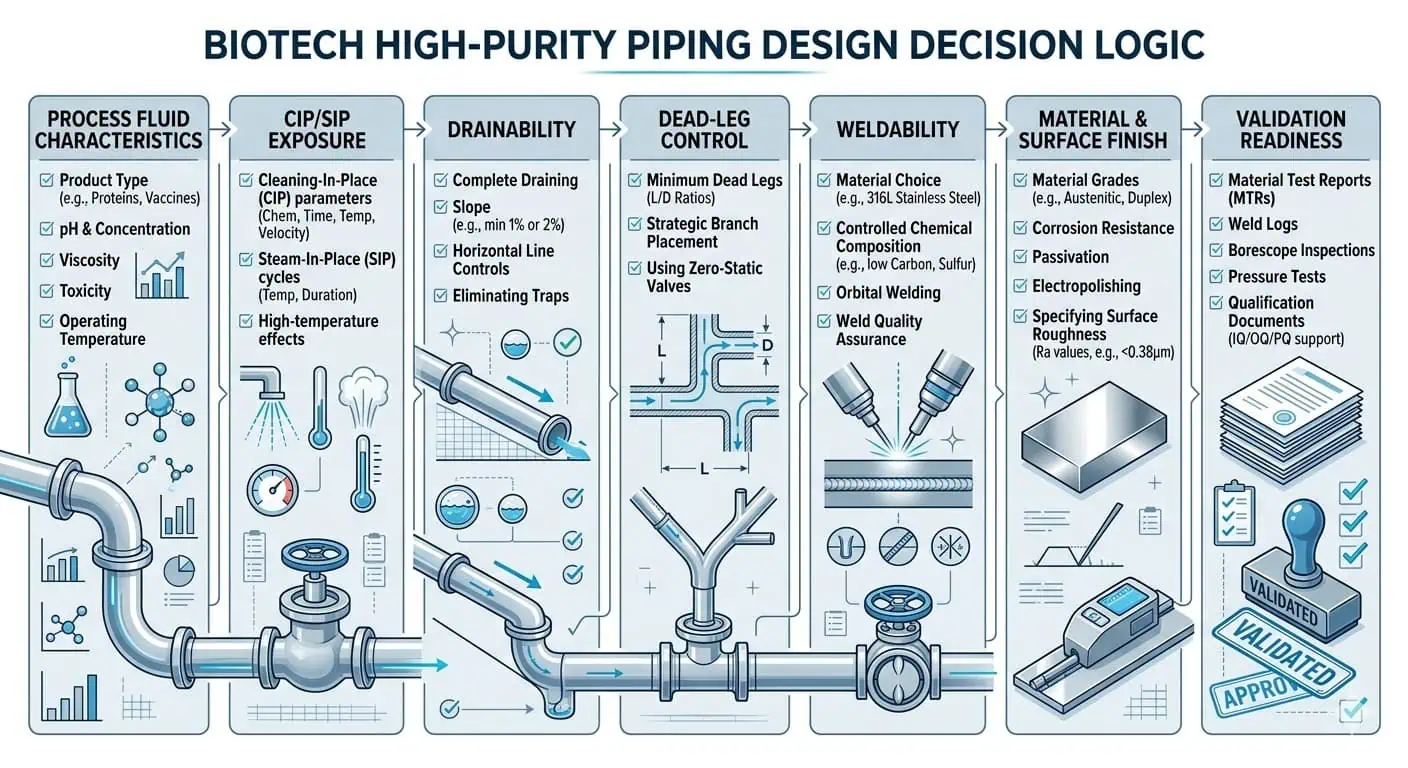
Cosa Significa Veramente la Progettazione di Tubazioni ad Alta Purezza negli Impianti Biotecnologici
La Progettazione ad Alta Purezza è una Decisione di Controllo della Contaminazione
Nei sistemi biotecnologici, la progettazione delle tubazioni è parte del controllo della contaminazione. ASME BPE è utile qui perché non tratta materiali, requisiti superficiali, progettazione per pulibilità e sterilità, fabbricazione, esame, ispezione, test e certificazione come argomenti isolati. Li tratta come un unico quadro ingegneristico igienico connesso. Norme FDA per le attrezzature punto nella stessa direzione: le attrezzature devono essere progettate in modo appropriato, le superfici a contatto con il prodotto devono essere non reattive, non additive e non assorbenti, e le attrezzature devono essere pulibili e mantenibili sotto controllo scritto.
Realtà ingegneristica tipica: il circuito di tubazioni che crea più problemi raramente è la linea principale tra i recipienti. Più spesso è il ramo di campionamento, il tee per strumenti, il punto di distribuzione o il collettore locale che è stato trattato come un dettaglio minore durante la progettazione. Nel lavoro biotecnologico, la domanda di progettazione non è mai solo “Questo fluido si trasferirà?” È “Questo assemblaggio sarà ancora pulibile, drenabile, ispezionabile e difendibile dopo la fabbricazione e la validazione?”
Consiglio esperto: se la revisione del progetto si concentra solo sulla portata, la caduta di pressione e il percorso della linea, è ancora incompleta per un sistema biotecnologico ad alta purezza. Il progetto deve essere rivisto attraverso la lente del fallimento igienico, non solo del flusso del processo.
Perché gli impianti biotecnologici necessitano di più della pratica generale di tubazioni alimentari
Gli impianti biotecnologici di solito impongono richieste più stringenti sulle tubazioni rispetto al servizio alimentare generale. Le conseguenze della ritenzione di residui, della contaminazione microbica, della scarsa risposta al vapore pulito o della modifica non documentata in campo sono maggiori. In molti impianti biotecnologici, il sistema di tubazioni non è giudicato solo in base al fatto che funzioni in sicurezza. È giudicato in base alla sua capacità di supportare la qualificazione, la verifica della pulizia, la cronologia della manutenzione, il controllo delle modifiche e la coerenza del processo a lungo termine.
Caso tipico del settore: un concetto di layout che funziona accettabilmente in un impianto alimentare generale può ancora essere rifiutato in un progetto biotecnologico perché la disposizione del ramo locale, la condizione della superficie o l'onere documentale sono più difficili da difendere in un ambiente focalizzato sulla validazione. Il problema non è che la biotecnologia utilizza una fisica completamente diversa. Il problema è che la tolleranza per comportamenti igienici ambigui è molto più bassa.
Un sistema ad alta purezza deve funzionare igienicamente, non solo apparire igienico
L'hardware dall'aspetto alimentare non crea automaticamente un sistema ad alta purezza. Un tubo lucidato, un raccordo igienico o un tappo di saldatura dall'aspetto pulito non dimostrano che il sistema installato scarichi correttamente, che la geometria del ramo sia accettabile o che l'assemblaggio locale più difficile si pulirà in modo affidabile in loco. La progettazione delle tubazioni biotecnologiche ha successo quando la geometria locale e le pratiche di fabbricazione supportano l'intento igienico della specifica.
Questo è il motivo per cui questo articolo dovrebbe essere letto insieme a Selezione di Raccordi Alimentari per Sistemi di Fermentazione. Un assemblaggio locale errato può compromettere un design di sistema altrimenti robusto.
Iniziare con il Processo Reale: Fluido, Pulizia e Carico di Validazione
Le Caratteristiche del Fluido di Processo Cambiano il Design
Diversi fluidi biotecnologici creano diversi carichi di design igienico. Le soluzioni tampone, i terreni di coltura, gli intermedi di prodotto, i flussi di raccolta, i servizi correlati all'acqua per iniezione (WFI), i prodotti chimici per la pulizia in posto (CIP), il vapore per la sterilizzazione in posto (SIP) e i fluidi igienici correlati alle utility non si comportano allo stesso modo nelle tubazioni. Alcuni mettono alla prova il margine di corrosione. Alcuni mettono alla prova la compatibilità delle guarnizioni. Alcuni rendono il design dei punti morti e dei punti di campionamento più sensibili perché il comportamento dei residui o le conseguenze microbiche sono maggiori.
Considerazione ingegneristica: Un buon design delle tubazioni inizia con il processo effettivo e i mezzi di pulizia, non con uno standard di tubazione predefinito. Se il team di progettazione non può descrivere chiaramente cosa trasporterà la linea, quali temperature incontrerà e come verrà pulita o sterilizzata, è troppo presto per finalizzare i dettagli delle tubazioni.
CIP, SIP e l'Esposizione Termo-Chimica Sono Input di Design
La pulizia e la sterilizzazione non sono dettagli operativi aggiunti successivamente. Sono input di progettazione. FDA 21 CFR 211.67 richiede che le attrezzature vengano pulite, manutenute e, ove appropriato, sanificate e/o sterilizzate secondo procedure controllate. Nella progettazione pratica delle tubazioni, ciò significa che il sistema deve essere progettato per il reale regime termico e chimico a cui sarà sottoposto. L'esposizione al vapore pulito, l'acqua per iniezione calda, la soda caustica, l'acido, il sanificante, il raffreddamento e i ripetuti cicli termici influenzano tutti quali materiali, guarnizioni, saldature e raccordi locali sopravviveranno in modo affidabile.
Caso tipico del settore: una linea è stata dimensionata e instradata correttamente per il trasferimento del processo, ma ripetute esposizioni SIP hanno successivamente rivelato debolezze alle interfacce di tenuta locali e orientamenti delle valvole difficili da drenare. Il problema non era che il flusso del processo fosse sbagliato. Il problema era che l'ambiente di pulizia e sterilizzazione non era stato trattato come parte della base di progettazione originale.
Consiglio esperto: se un assemblaggio locale non sopravvivesse alla sua reale esposizione CIP/SIP senza particolari precauzioni, allora il problema è legato alla progettazione anche se la linea principale appare ancora accettabile.
Il Carico di Validazione Cambia il Significato di “Buona Progettazione”
Negli impianti biotecnologici, la progettazione è in parte valutata in base a quanto bene il sistema può essere validato e mantenuto sotto controllo delle modifiche. Una linea che è operabile ma difficile da ispezionare, documentare o difendere durante la qualificazione non è una progettazione ad alta purezza robusta. Ecco perché gli ingegneri esperti chiedono presto: dove sono gli assemblaggi locali a più alto rischio, come verranno ispezionati e quali prove saranno necessarie dopo la fabbricazione e l'avvio?
Per il lato del ciclo di vita di questa logica, collegare questo articolo con Considerazioni sulla Manutenzione e Validazione di Tubazioni Alimentari.
I Principi di Progettazione Fondamentali che Decidono se il Sistema Avrà Successo
Drenabilità
La vera drenabilità è uno dei primi requisiti di progettazione in un sistema di tubazioni ad alta purezza. Il liquido residuo dopo la pulizia o la vaporizzazione non è solo un fastidio per la manutenzione. Modifica il comportamento igienico del ciclo successivo, aumenta il rischio di contaminazione locale, complica l'asciugatura e rende meno affidabile la risoluzione dei problemi. Domande e risposte dell'FDA sull'attrezzatura collega insieme la progettazione dell'attrezzatura, la pulizia, la manutenzione e l'idoneità delle superfici a contatto con il prodotto, che è esattamente come dovrebbe essere valutata la drenabilità in un circuito biotecnologico.
Caso tipico del settore: il disegno di progetto mostrava una linea di drenaggio, ma dopo che i supporti sono stati regolati in campo, una campata installata ha creato un punto basso sottile che ha ripetutamente trattenuto liquido dopo il CIP. Il problema non è apparso nel modello di processo principale. È apparso nella geometria installata.
Consiglio esperto: non assumere mai la drenabilità solo dall'intento del disegno. Rivedere insieme pendenza, spaziatura dei supporti, orientamento del corpo della valvola, posizione del punto di drenaggio e comportamento finale installato.
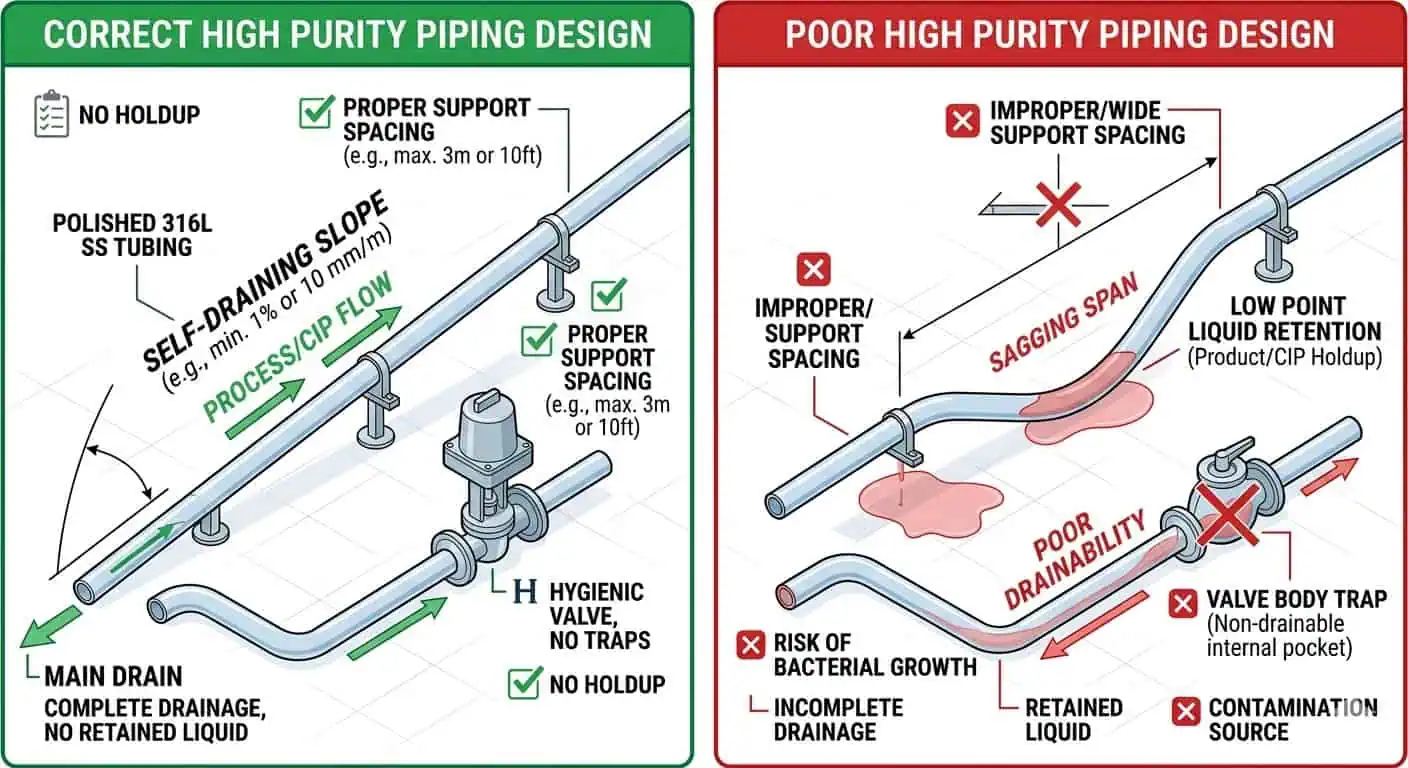
Controllo dei Ramo Morto
Il controllo del ramo morto rimane una delle parti più importanti e più sottovalutate della progettazione di tubazioni ad alta purezza. Una linea può essere realizzata con il materiale corretto, avere la finitura giusta e comunque diventare difficile da pulire se la progettazione del ramo crea zone stagnanti. I prelievi campione, i tee per strumenti, i collettori locali e i rami aggiunti sono dove questo problema appare più spesso.
Caso tipico del settore: il circuito principale ha ripetutamente raggiunto gli obiettivi operativi e di pulizia, ma un ramo campione ha continuato a generare preoccupazioni igieniche. La causa principale non era la concentrazione del detergente o il tempo del ciclo. Era lo scarso scambio di fluido locale in un ramo che non era mai stato esaminato criticamente come parte della progettazione CIP/SIP.
Consiglio esperto: Valutare il ramo locale più difficile, non la condotta principale più semplice. Se un'assemblaggio locale non può scambiare fluido e drenare in modo affidabile, è quel progetto che conta.
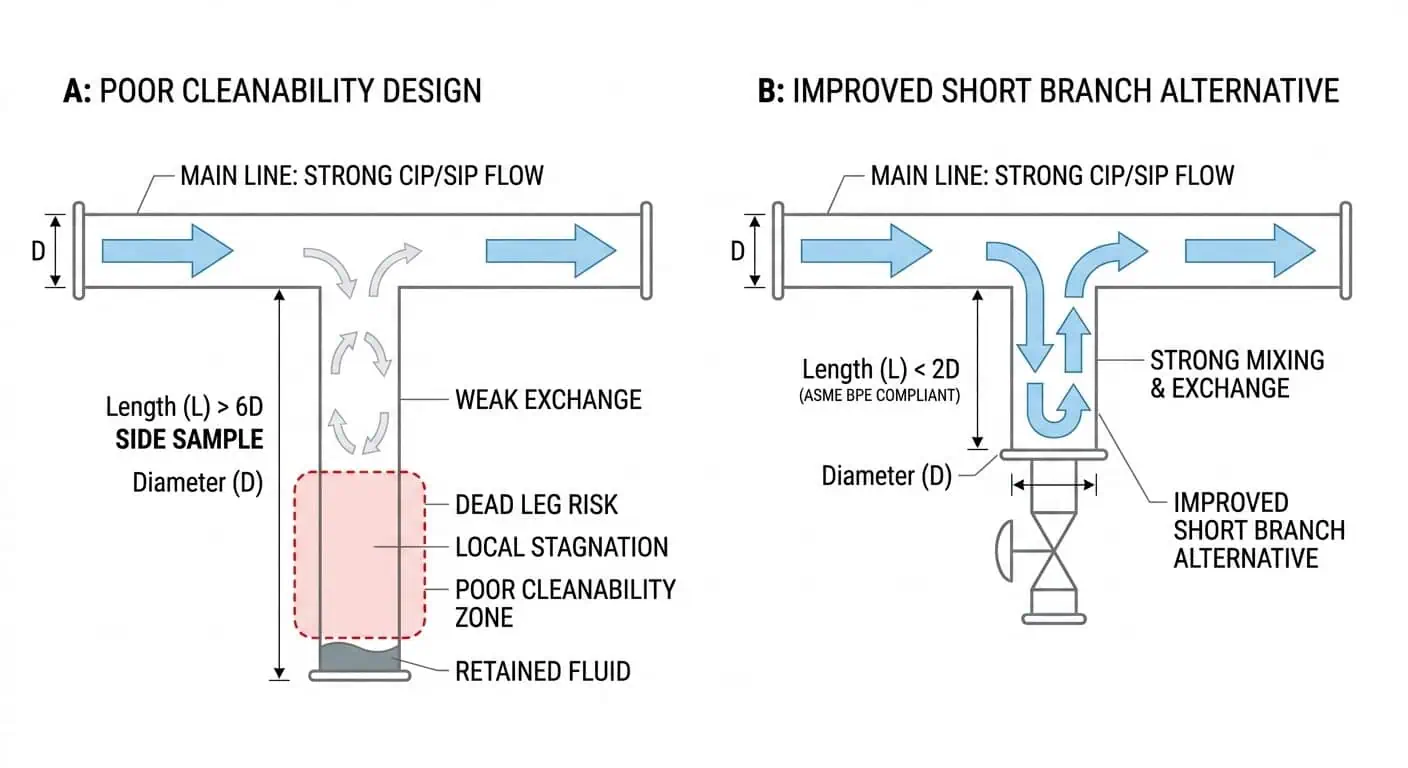
Percorso di Flusso Pulibile
Una linea che trasferisce bene il prodotto non si pulisce automaticamente bene. Il flusso di produzione e il flusso di pulizia sono problemi di progettazione correlati ma non identici. Nei sistemi ad alta purezza, il percorso principale del processo può essere idraulicamente accettabile mentre un assemblaggio locale rimane ancora il punto debole perché il suo percorso interno, orientamento o configurazione del ramo impedisce un'azione di pulizia efficace.
Logica di progettazione basata sulla ricerca: Panoramica dello scopo ASME BPE collega direttamente i requisiti di superficie, la progettazione per la pulibilità e la sterilità, la fabbricazione dei componenti, la fabbricazione inclusa la giunzione dei materiali, la tubazione, gli esami, le ispezioni, i test e le certificazioni. Questo è importante perché rafforza una verità ingegneristica pratica: la pulibilità non è solo un'impostazione chimica. È progettata nel percorso bagnato.
Accesso all'Ispezione e Intervento Controllato
Non ogni posizione dovrebbe essere progettata per l'apertura di routine, e non ogni posizione dovrebbe essere permanentemente chiusa senza una buona ragione. I sistemi ad alta purezza necessitano di un equilibrio controllato tra la minimizzazione delle interfacce e il consentire un accesso giustificato dove guarnizioni, diaframmi o assemblaggi locali richiederanno attenzione durante il ciclo di vita. Questo è uno dei compromessi di progettazione più importanti nella tubazione biotecnologica, perché ogni interfaccia di smontaggio aggiunta può migliorare l'accesso mentre aumenta anche il rischio igienico legato alle guarnizioni.
Materiali e requisiti di superficie nelle tubazioni biotecnologiche ad alta purezza
Perché l'acciaio 316L è comunemente la linea di base
L'acciaio 316L è comunemente utilizzato nelle tubazioni biotecnologiche ad alta purezza perché offre un equilibrio pratico tra margine di corrosione, saldabilità e accettazione del settore per servizi igienici critici. Ciò non lo rende la soluzione a ogni problema di processo, ma spiega perché molti progetti lo trattano come il materiale metallico di base per servizi critici a contatto con il prodotto e ad alta purezza. ASME BPE copre i materiali e i requisiti di superficie all'interno del più ampio quadro di progettazione igienica, che è esattamente come gli ingegneri dovrebbero valutare l'acciaio 316L nella pratica.
Per la discussione completa sul lato materiali, collega questo articolo con Acciaio Inossidabile 316L in Applicazioni di Bioprocesso.
La finitura superficiale è una variabile di prestazione igienica
La finitura superficiale non è una scelta estetica nelle tubazioni biotecnologiche. Influisce sulla pulibilità locale, sulla sicurezza dell'ispezione e sul comportamento pratico delle superfici a contatto con il prodotto dopo la fabbricazione. La domanda chiave di progettazione non è se una finitura sembri “più premium”. È se la finitura scelta supporta l'obiettivo igienico del processo e le aspettative di ispezione dell'impianto.
Caso tipico del settore: la lega era accettabile, ma il progetto ha successivamente rivisto il requisito di finitura perché l'aspettativa superficiale originale non corrispondeva più al carico di pulibilità e ispezione dell'area di processo finale. La lezione non era che la famiglia di metalli fosse sbagliata. La lezione era che la finitura non era stata definita con sufficiente disciplina specifica del processo.
Punto di fatto: ASTM A270 esplicitamente afferma che la qualità farmaceutica può essere richiesta come requisito supplementare, il che è un utile promemoria che le decisioni sui tubi nei progetti ad alta purezza spesso vanno oltre la fornitura generica di tubi alimentari.
Anche le Parti Bagnate Non Metalliche Sono Importanti
La progettazione di tubazioni ad alta purezza non si ferma alla parete del tubo in acciaio inossidabile. Guarnizioni, diaframmi, sedi di valvole, tubi flessibili e altre parti bagnate non metalliche spesso diventano il primo punto debole nella pulizia, nell'esposizione al vapore o nell'affidabilità del ciclo di vita. In molte deviazioni di progetto, l'acciaio inossidabile era accettabile, ma la strategia locale per elastomeri o polimeri non era controllata abbastanza strettamente per il processo reale e il regime di sterilizzazione.
Consiglio esperto: se il team di progettazione sta discutendo la scelta della lega ma non ha definito la compatibilità delle guarnizioni e la logica di sostituzione, la revisione del design igienico è ancora incompleta.
Costruzione Saldata, Saldatura Orbitale e Realtà della Fabbricazione
La Progettazione delle Tubazioni Non Può Essere Separata dalla Progettazione delle Saldature
In un sistema biotecnologico ad alta purezza, la saldabilità è parte della progettazione, non un ripensamento della fabbricazione. Più un sistema dipende dalla qualità controllata delle saldature per le prestazioni igieniche, più diventa irrealistico finalizzare il percorso e la logica di diramazione senza considerare come le saldature saranno effettivamente realizzate, purgate, ispezionate e documentate.
Caso ingegneristico tipico: Il materiale e il percorso erano accettabili sulla carta, ma un'assemblaggio locale è diventato difficile da difendere perché l'accesso alla saldatura, la qualità della purga e la praticità dell'ispezione non erano stati considerati quando la disposizione del ramo era stata inizialmente pianificata. La debolezza non è iniziata solo nella fabbricazione. È iniziata nella progettazione.
Perché la Logica della Saldatura Orbitale è Importante
La logica della saldatura orbitale è importante nel biotech non perché suona più avanzata, ma perché la ripetibilità, la controllabilità e la documentazione contano di più nei servizi ad alta purezza. Nella pratica, gli ingegneri devono pensare se una disposizione proposta supporta un'esecuzione affidabile della saldatura, condizioni di purga ripetibili e accesso all'ispezione nelle posizioni esatte che in seguito saranno più importanti per il controllo qualità e la manutenzione.
Consiglio esperto: Durante la revisione del progetto, chiedersi sempre se la linea è semplicemente disegnabile o effettivamente saldabile in condizioni controllate ad alta purezza.
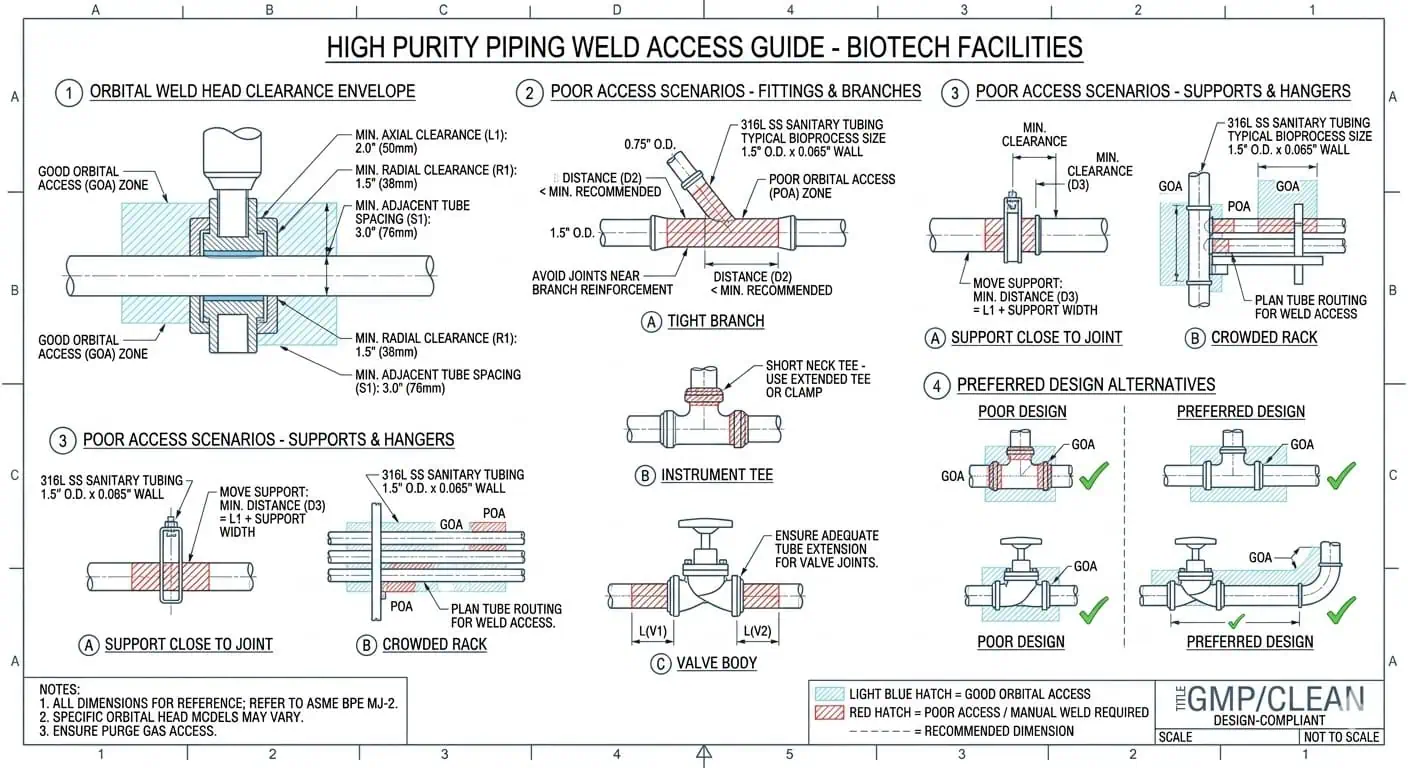
Il Materiale Base è Spesso Corretto, ma la Zona di Saldatura Diventa il Punto Debole
Uno dei guasti più realistici nelle tubazioni biotech è un sistema in cui il materiale selezionato era corretto, ma la condizione adiacente alla saldatura è diventata il punto debole alimentare. Quando ciò accade, i team a volte si concentrano eccessivamente sull'aggiornamento del materiale quando il vero problema è l'esecuzione della saldatura, il controllo della finitura locale o la geometria originale dell'assemblaggio. La lezione ingegneristica è semplice: una lega corretta non può salvare una zona di saldatura alimentare inconsistente.
Valvole, Rami, Punti di Campionamento e Assemblaggi Locali
Progettazione del Punto di Prelievo
I punti di prelievo sono di piccole dimensioni ma di grande importanza. Combinano geometria del ramo, interazione dell'operatore, numero di tenute, rischio locale di scambio di fluido e ripetuti controlli igienici. Ecco perché la progettazione del punto di prelievo merita più attenzione ingegneristica di quanto suggerisca la sua impronta. In molte strutture biotecnologiche, la domanda igienica più ripetuta non riguarda la linea di trasferimento principale. Riguarda l'assemblaggio locale di prelievo.
Caso tipico del settore: un circuito principale ha funzionato in modo accettabile, ma lo stesso punto di prelievo ha ripetutamente innescato revisioni aggiuntive perché l'assemblaggio intrappolava il fluido e non scambiava mai il mezzo di pulizia in modo efficace come il circuito principale.
Manifold di Valvole e Aree ad Alta Densità di Rami
I gruppi di valvole e i manifold ad alta densità di rami sono dove i buoni progetti ad alta purezza spesso diventano fragili. Il problema non è che le valvole siano cattive. Il problema è che valvole, rami, tenute e strumentazione moltiplicano tutti la complessità igienica locale. Man mano che la complessità locale aumenta, il progetto necessita di un controllo più forte sulla drenabilità, densità delle saldature, interfacce di tenuta e logica di ispezione.
Tee per Strumenti e Connessioni per Sensori
I tee per strumenti e i raccordi per sensori sono spesso sottovalutati perché sono piccoli, ma possono dominare il rischio di pulibilità locale. Se il team di progettazione non li tratta come assemblaggi locali critici, spesso diventano il luogo dove la ritenzione di residui, la stagnazione locale o la discrepanza nella documentazione diventano visibili per la prima volta.
Consiglio esperto: progettare l'assemblaggio locale che è più difficile da pulire e più facile da trascurare. Di solito è lì che risiede il vero rischio del sistema.
Strategia di Connessione: Saldata Versus a Morsetto Versus Accesso Controllato
Dove Sono Preferite Connessioni Saldate Più Permanenti
Le connessioni saldate più permanenti sono spesso la scelta più sicura dove le conseguenze igieniche sono elevate e l'accesso di routine non è necessario. Nelle aree stabili a contatto con il prodotto, ridurre il numero di interfacce può ridurre la variabilità legata alle guarnizioni e rimuovere uno strato di rischio dell'assemblaggio locale. Ciò non rende la saldatura automaticamente migliore ovunque. Significa che il giunto permanente spesso diventa preferibile dove la posizione non beneficia abbastanza dall'apertura ripetuta per giustificare l'interfaccia aggiuntiva.
Dove Ha Ancora Senso l'Accesso Alimentare a Morsetto
Le connessioni a morsetto hanno ancora senso dove l'accesso controllato, la sostituzione della guarnizione o il cambio modulare sono un requisito reale del ciclo di vita. L'errore non è usare affatto le connessioni a morsetto. L'errore è posizionarle in posizioni ad alta conseguenza senza riconoscere il carico aggiuntivo di controllo della tenuta che creano.
Per la logica lato raccordo locale, collegare questo articolo con Selezione di Raccordi Alimentari per Sistemi di Fermentazione.
La domanda migliore non è “Quale connessione è migliore?”
La domanda migliore è se la posizione trae maggior beneficio dall'accesso o dalla riduzione del numero di interfacce. Questo è il vero compromesso ingegneristico. Uno stile di connessione eccellente in un'area può diventare la scelta sbagliata altrove se introduce un controllo di tenuta non necessario, un carico di pulizia aggiuntivo o un intervento di manutenzione eccessivo in una zona ad alta purezza.
Progettare per la Manutenzione e la Validazione fin dal Primo Giorno
Un Buon Progetto è Più Facile da Mantenere
Il sistema di tubazioni ad alta purezza più facile da mantenere è quello i cui rischi igienici locali sono stati ridotti durante la progettazione invece di essere delegati alla manutenzione successiva. Scarso drenaggio, accesso scomodo alle tenute, valvole mal orientate e assemblaggi locali difficili da ispezionare diventano tutti oneri di manutenzione dopo l'avvio. Sono più facili da correggere su un disegno che in un impianto biotecnologico in funzione.
Per il lato del ciclo di vita, collega questo articolo con Considerazioni sulla Manutenzione e Validazione di Tubazioni Alimentari.
La Validazione Inizia nella Progettazione
La validazione non inizia dopo l'installazione. Inizia quando il team di progettazione decide cosa il sistema deve essere in grado di dimostrare. Se la linea richiederà prove evidenti di pulibilità, ispezionabilità o geometria locale controllata, tali requisiti devono già essere visibili nella progettazione. I sistemi che sono operativi ma difficili da validare di solito rivelano che il team di progettazione ha trattato la logica di qualificazione troppo tardi nel progetto.
Caso tipico del settore: Un circuito di tubazioni ha avuto successo meccanico, ma la qualificazione ha richiesto più tempo del previsto perché gli assemblaggi locali più difficili da pulire non erano stati chiaramente identificati durante la progettazione. La soluzione tecnica è stata minore. L'impatto sulla pianificazione non lo è stato.
Documentazione e Tracciabilità Devono Essere Anticipate nella Progettazione
Una progettazione ad alta purezza richiede anche una catena di prove realistica. L'identità dei materiali, i registri di saldatura, le aspettative di finitura e le modifiche in campo diventano molto più difficili da chiudere se la progettazione non ha mai definito come il sistema finale sarebbe stato documentato e rilasciato. Ecco perché la progettazione di tubazioni ad alta purezza dovrebbe anche collegarsi alla logica di consegna e tracciabilità del progetto.
Errori Comuni di Progettazione nelle Tubazioni Biotech ad Alta Purezza
Progettare per il Flusso del Prodotto ma Non per il Flusso di Pulizia
Un circuito può trasferire bene il fluido di processo e comunque sottoperformare durante la pulizia se gli assemblaggi locali non scambiano mai il mezzo di pulizia in modo sufficientemente efficace.
Accettare Layout di Aspetto Alimentare Senza Verificare i Punti Morti
L'aspetto non sostituisce la revisione dei rami locali. Il comportamento dei punti morti spesso si nasconde in piccoli assemblaggi, non nel percorso principale.
Concentrarsi eccessivamente sull'acciaio 316L trascurando saldature e geometria
Una lega più resistente non corregge una saldatura eseguita male, un drenaggio insufficiente o una geometria di diramazione complessa.
Utilizzare una sola logica di progettazione per tutte le aree di processo
Le linee a contatto con prodotti ad alto rischio, le diramazioni di campionamento, i servizi igienici ausiliari e le aree a rischio inferiore non dovrebbero essere tutte progettate secondo uno standard indifferenziato.
Rimandare le questioni di validazione e documentazione alle fasi avanzate del progetto
Se il sistema inizia a pensare a prove, tracciabilità e qualificazione solo dopo la fabbricazione, il progetto opera già con un controllo inferiore a quello necessario.
Lista di controllo pratica per la progettazione di tubazioni ad alta purezza negli impianti biotecnologici
Prima del congelamento del P&ID
- Definire i veri mezzi di processo e pulizia.
- Identificare gli assemblaggi locali a più alto rischio.
- Decidere dove il sistema necessita di accesso e dove richiede meno interfacce.
- Definire il carico igienico e di validazione di ogni area di processo principale.
Prima del Tracciamento Dettagliato
- Verificare la drenabilità, la logica della pendenza e il rischio di punti bassi.
- Controllare la lunghezza dei rami, la direzione di derivazione e il potenziale di ristagno locale.
- Verificare l'orientamento delle valvole e dei punti di campionamento come assemblaggi installati, non solo come simboli.
- Confermare l'accesso alla saldatura e la praticità di spurgo nelle posizioni critiche.
Prima della Fabbricazione
- Definire insieme i requisiti di materiale, finitura e tenuta.
- Allineare il tracciamento con una strategia di saldatura realistica e una logica di ispezione.
- Identificare gli assemblaggi che richiederanno una revisione igienica più rigorosa dopo la fabbricazione.
- Assicurarsi che la catena documentale sia compatibile con l'intento progettuale finale.
Prima dell'Avvio e della Qualifica
- Confermare che il circuito installato scarichi ancora come previsto.
- Rivedere gli assemblaggi locali più difficili da pulire, non solo la linea principale.
- Confermare che le modifiche in campo non abbiano introdotto nuovi punti deboli igienici.
- Verificare che il sistema finale supporti ancora l'approccio di validazione e manutenzione previsto.
| Argomento di Progettazione | Come si presenta una Buona Progettazione | Cosa Solitamente Va Storto |
|---|---|---|
| Drenabilità | La linea installata scarica in modo prevedibile nei punti locali a basso e alto rischio. | Lo scarico del disegno, ma la geometria del supporto installato non lo è |
| Controllo dei rami morti | I rami sono esaminati come assemblaggi igienici locali | I punti di campionamento e i tee per strumenti sono trattati come dettagli minori |
| Strategia di saldatura | Il percorso supporta la purga, l'accesso e l'ispezione realistici | Il progetto presuppone la qualità della saldatura senza verificare la praticità di fabbricazione |
| Logica di connessione | L'accesso e il conteggio delle interfacce sono bilanciati dalle esigenze del processo | Le scelte di morsetto o saldato sono copiate senza una revisione specifica della posizione |
| Pronto per la validazione | Le assemblaggi più critici sono identificabili e difendibili | La logica di qualificazione inizia dopo la fabbricazione invece che durante la progettazione |
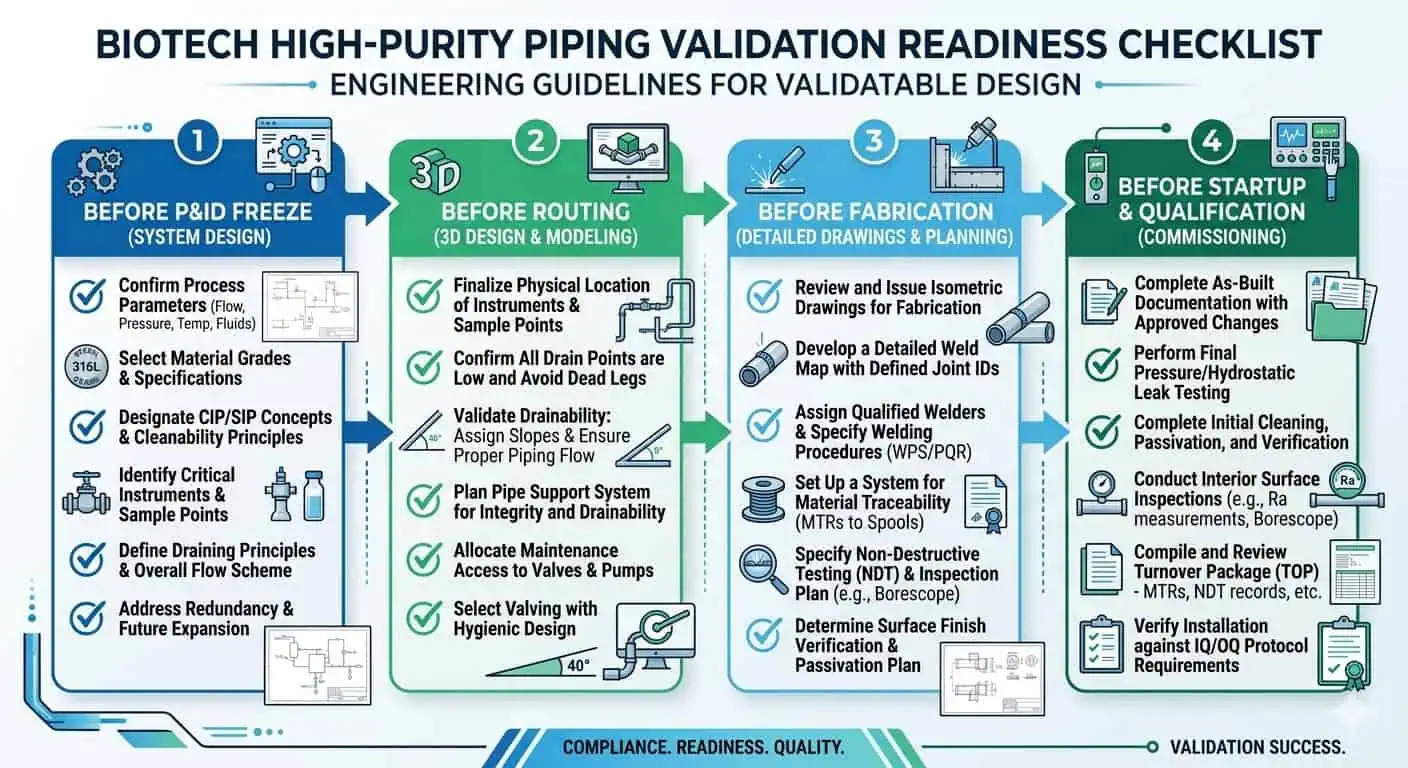
Conclusione: La progettazione di tubazioni ad alta purezza ha successo quando geometria, materiali, saldabilità e logica di validazione sono trattati come un unico sistema
La progettazione di tubazioni ad alta purezza per impianti biotecnologici ha successo quando geometria, materiali, saldabilità, pulibilità, drenabilità e logica di validazione sono progettati come un unico sistema. I progetti di tubazioni biotecnologici più robusti non si basano solo sul nome della lega, sull'aspetto superficiale o sullo stile del componente da catalogo. Essi riducono il rischio igienico locale nel ramo, nel punto di campionamento, nell'assemblaggio della valvola e nella zona di saldatura dove il processo è meno tollerante ai guasti.
Se desideri un cluster di argomenti biotecnologici più forte, collega questo articolo con Acciaio Inossidabile 316L in Applicazioni di Bioprocesso, Selezione di Raccordi Alimentari per Sistemi di Fermentazione, e Considerazioni sulla Manutenzione e Validazione di Tubazioni Alimentari.
FAQ
Qual è il fattore di progettazione più importante nelle tubazioni biotecnologiche ad alta purezza?
Il fattore più importante è solitamente la geometria pulibile e drenabile. Se il sistema non drena bene o crea comportamenti di dead-leg negli assemblaggi locali, materiali più resistenti e finiture dall'aspetto migliore non risolveranno il problema igienico di base.
È sempre richiesto l'acciaio 316L nelle tubazioni alimentari biotecnologiche?
Non automaticamente. 316L è una linea di base comune per servizi critici ad alta purezza, ma la decisione finale dipende ancora dalla chimica del processo, dall'esposizione a pulizia e sterilizzazione, dal requisito di finitura e dal profilo di rischio dell'assemblaggio locale.
Perché i tratti morti rappresentano un problema così grave nei sistemi ad alta purezza?
Poiché i tratti morti indeboliscono lo scambio locale del fluido, l'efficacia della pulizia e la drenabilità. Sono uno dei motivi più comuni per cui un ramo locale o un punto di campionamento continua a creare preoccupazioni igieniche anche quando il circuito principale sembra accettabile.
Quando dovrebbero essere utilizzate le connessioni a morsetto nelle tubazioni biotecnologiche?
Utilizzarli dove l'accesso controllato, la sostituzione della tenuta o l'intervento modulare sono effettivamente necessari. Possono essere la scelta giusta, ma ogni interfaccia aggiunta aumenta anche il rischio igienico legato alla tenuta, quindi non dovrebbero essere utilizzati per impostazione predefinita in ogni ubicazione ad alta purezza.
L'elettrolucidatura risolve problemi di saldatura scadente o di geometria difettosa?
No. Una finitura più stretta può supportare un obiettivo igienico più elevato, ma non risolve la debole drenabilità, la cattiva geometria del ramo o una zona di saldatura scadente.
In che modo la convalida influisce sulle decisioni di progettazione delle tubazioni?
La convalida cambia ciò che il sistema deve essere in grado di dimostrare, non solo come deve funzionare. Un progetto di tubazioni che è operabile ma difficile da ispezionare, documentare o difendere può ancora essere un progetto biotecnologico debole.




