La documentation et la traçabilité dans les projets de tuyauterie pharmaceutique ne sont pas des formalités administratives ajoutées après l'installation. Elles constituent la chaîne de preuves qui démontre que le système installé correspond aux matériaux, finitions, soudures, inspections et intentions de conception hygiénique approuvés. Dans les projets GMP, une boucle de tuyauterie peut être mécaniquement terminée et rester non libérable parce que la documentation ne prouve pas clairement ce qui a été installé, comment il a été fabriqué, ce qui a changé sur le terrain, et si l'assemblage final respecte toujours la norme du projet approuvée.
C'est pourquoi les ingénieurs expérimentés ne traitent pas les documents de transfert comme une simple remise administrative. Ils les considèrent comme faisant partie du contrôle de conception du projet dès le début. Si la traçabilité des matériaux, les registres de soudure, les registres de finition, les preuves d'inspection, les modifications rouges et les livrables de transfert ne sont pas définis avant l'appel d'offres, le projet tente souvent de reconstruire la chaîne de preuves plus tard à un coût bien plus élevé et avec moins de confiance. Ce guide explique ce que signifient réellement la documentation et la traçabilité dans les projets de tuyauterie pharmaceutique, quels registres sont les plus importants, où la chaîne de preuves se brise généralement, et comment les équipes GMP peuvent définir le bon ensemble de documentation avant le début de la fabrication.
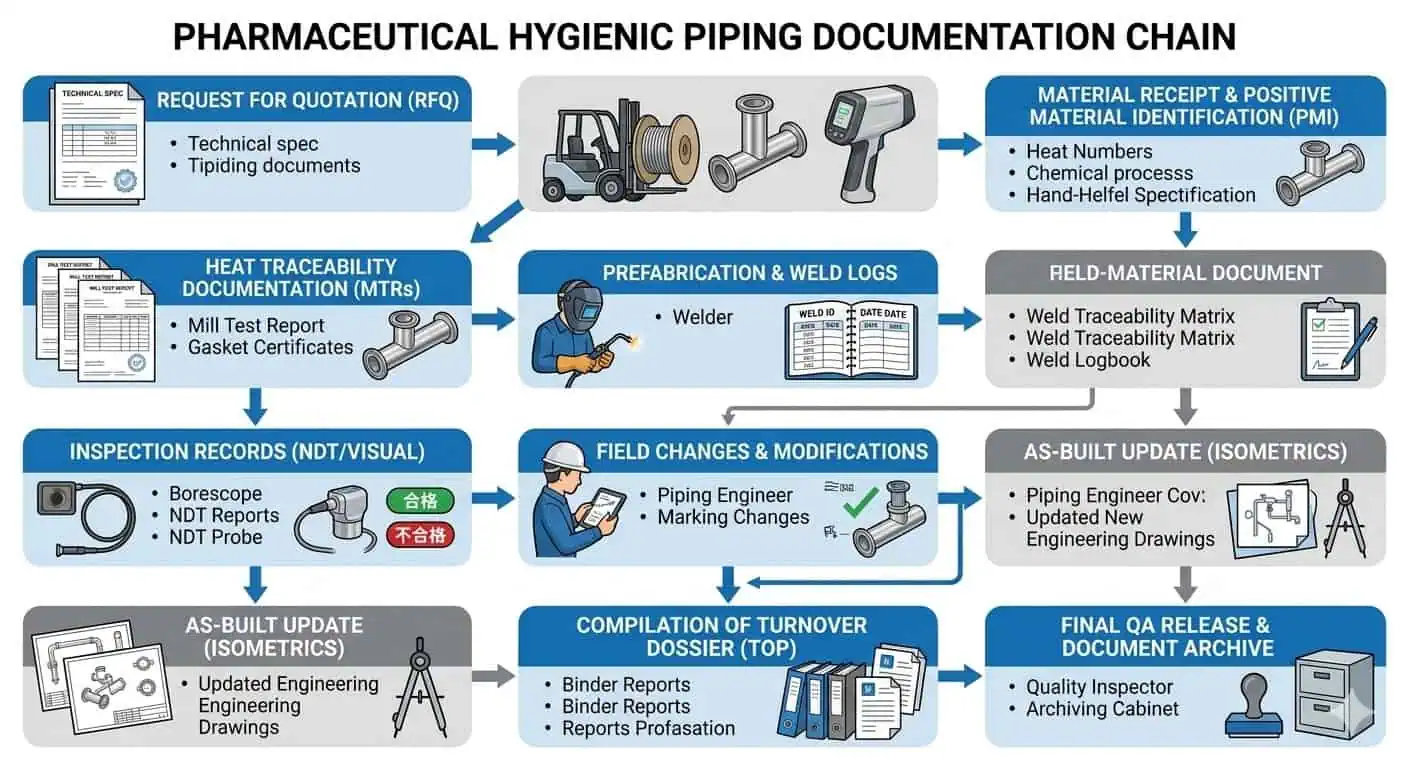
Dans les travaux pharmaceutiques réels, les problèmes de documentation apparaissent rarement comme des défaillances mécaniques dramatiques. Ils se manifestent par une clôture QA plus lente, des commentaires de transfert non résolus, une lignée de soudure peu claire, des historiques de tronçons incohérents, ou une incertitude quant à savoir si la boucle installée finale reflète toujours l'intention hygiénique approuvée. C'est pourquoi une documentation solide n'est pas une préférence administrative. C'est un contrôle d'ingénierie.
Pourquoi la documentation et la traçabilité sont importantes dans les projets de tuyauterie pharmaceutique
C'est un sujet de QA et de libération, pas seulement un sujet de classement d'ingénierie
Dans la tuyauterie pharmaceutique, la documentation fait partie du contrôle de libération, pas seulement de l'administration de projet. Le chapitre 4 de l'EU GMP ne décrit pas la documentation comme une commodité de classement. Il décrit une bonne documentation comme une partie essentielle du système d'assurance qualité et le mécanisme utilisé pour établir, contrôler, surveiller et enregistrer les activités qui affectent la qualité du produit. La logique de la FDA va dans le même sens : l'équipement en contact avec le produit doit être adapté à l'usage, et le nettoyage, la maintenance et l'historique de l'équipement doivent être contrôlés et enregistrés. En d'autres termes, la boucle installée doit être techniquement correcte et prouvablement correcte en même temps.
Cas typique de l'industrie : une boucle de transfert en contact avec le produit est entièrement installée, testée sous pression et visuellement acceptable. Les opérations voient un système de tuyauterie terminé. La QA voit une chaîne de preuves incomplète parce que le dossier final ne peut toujours pas clairement relier l'identité du matériau approuvé, l'historique des soudures et la configuration finale telle que construite. La tuyauterie est physiquement présente, mais la logique de libération reste non résolue.
Conseil d'expert : Si l'équipe projet considère la documentation comme quelque chose qui commence à la livraison, il est déjà trop tard. Dans la tuyauterie GMP, l'histoire de la libération doit être construite pendant que la boucle est conçue, fabriquée, inspectée et modifiée—et non après que la dernière bride est serrée.
Note d'ingénierie : dans la tuyauterie GMP, la boucle installée n'est aussi libérable que la chaîne de preuves qui démontre son état final en contact avec le fluide.
Pourquoi les projets de tuyauterie pharmaceutique échouent souvent à la livraison, et non à la fabrication
De nombreux projets de tuyauterie pharmaceutique n'échouent pas parce que la boucle a été mal construite. Ils échouent parce que le projet ne peut pas prouver, sous une forme prête pour la libération, que la boucle installée finale correspond toujours à l'intention hygiénique approuvée. C'est un type d'échec différent, mais dans le travail GMP, c'est souvent le plus dangereux car il apparaît tard, après que le système semble déjà mécaniquement complet. Le chapitre 4 de l'EU GMP et la logique de tenue des dossiers de la FDA soutiennent la même conclusion pratique : si l'historique de nettoyage, l'identité des composants, l'état des soudures et la configuration installée ne peuvent pas être reconstruits de manière fiable, le système devient plus difficile à défendre lors de la libération et plus tard pendant l'exploitation.
Cas typique de l'industrie : L'équipe d'installation sur site termine une boucle hygiénique et suppose que le travail difficile est terminé. Un examen ultérieur montre que plusieurs tronçons ont été révisés sur site pour améliorer le tracé et la pente, mais la carte de soudure finale, la matrice matériaux-emplacement et le dossier tel que construit n'ont jamais été pleinement réconciliés. Personne ne prétend que le métal est incorrect. Le problème est que le projet ne peut plus prouver clairement quels matériaux certifiés, dossiers de soudure et résultats d'inspection appartiennent à l'arrangement installé final. À ce stade, la boucle ne lutte pas contre un défaut de fabrication. Elle lutte contre un défaut de preuve de libération.
Les ingénieurs de projet expérimentés définissent donc la chaîne de documentation avant l'appel d'offres, et non après l'achèvement mécanique. Une fois que la fabrication commence, chaque coupe sur site non contrôlée, échange de tronçon ou redirection de branche devient plus difficile à clôturer rétroactivement. La leçon d'ingénierie est simple : dans la tuyauterie GMP, si vous attendez la livraison pour décider de ce qui doit être traçable, le projet finit généralement par reconstruire la chaîne de preuves à un coût plus élevé et avec une confiance moindre.
Ce que le cadre GMP et réglementaire exige réellement
Les réglementations les plus utiles sont celles qui changent ce que l'équipe projet définit et enregistre avant la livraison. Dans ce sujet, le cadre de base comprend généralement :
- tolérances dimensionnelles ASME BPE, qui couvre les matériaux, la conception, la fabrication, les inspections, les tests et la logique de certification pour les équipements de bioprocédés et pharmaceutiques.
- FDA 21 CFR 211.65, qui exige que les surfaces en contact avec le produit soient non réactives, non additives et non absorbantes.
- FDA 21 CFR 211.67, qui lie le nettoyage et la maintenance des équipements à des procédures écrites et des enregistrements.
- FDA 21 CFR 211.182, qui traite des journaux de nettoyage, de maintenance et d'utilisation des équipements principaux.
- FDA 21 CFR 211.184, qui couvre les enregistrements des composants, conteneurs, fermetures et étiquettes.
- EU GMP Chapitre 4, qui définit la documentation comme une partie essentielle du système d'assurance qualité et exige que les enregistrements soient contrôlés, précis, traçables et conservés de manière appropriée.
Conclusion de la recherche : ces sources ne traitent pas la documentation comme un support d'arrière-plan. Elles la traitent comme une partie contrôlée de l'exécution des BPF. Pour les équipes de tuyauterie, cela signifie que la question n'est jamais simplement “ quels enregistrements avons-nous ? ” mais “ ces enregistrements prouvent-ils encore suffisamment clairement le système mouillé final pour la libération QA ? ”
Ce qui doit être traçable dans un projet de tuyauterie BPF
Tubes, raccords, vannes et autres composants mouillés
La traçabilité doit suivre le chemin mouillé, pas seulement les composants les plus grands ou les plus faciles. De nombreuses équipes gèrent bien les tubes mais traitent trop légèrement les petits raccords, diaphragmes, vannes d'échantillonnage, ferrules, joints et composants de branchement. Dans les projets BPF, c'est une erreur. Les plus petites pièces mouillées sont souvent les plus faciles à substituer, les plus difficiles à suivre ultérieurement et les premières à soulever des questions QA lors de la remise.
Cas typique de l'industrie : la traçabilité des tubes est complète, mais le dossier de remise devient faible au niveau des assemblages locaux parce que les raccords, joints ou internes de vannes d'échantillonnage ont été traités en dehors du flux de travail de contrôle principal. La ligne semble correcte lors de la visite, mais le maillon le plus faible de la traçabilité se situe exactement là où l'assemblage hygiénique est le plus complexe.
Conseil d'expert : si un composant est suffisamment important pour être spécifié dans la conception hygiénique, il est suffisamment important pour être traçable dans la logique de remise. En pratique, les équipes obtiennent une meilleure clôture QA lorsqu'elles définissent la traçabilité autour du chemin mouillé complet plutôt qu'autour des seuls tubes.
Certificats de matériaux, numéros de coulée et identité de lot
La traçabilité des matériaux n'est utile que lorsque l'emplacement installé peut être clairement relié à l'ensemble d'enregistrements d'origine. Les rapports d'essai de matériaux, les certificats EN 10204 3.1, les numéros de coulée et les enregistrements de réception sont tous importants, mais seulement si le projet préserve le lien entre l'identité du fournisseur et l'emplacement installé de la pièce, du raccord ou de l'assemblage. Un tas de certificats sans matrice d'emplacement claire n'est pas un dossier de traçabilité solide.
Cas typique de l'industrie : le projet dispose des certificats de matériaux appropriés, mais après les découpes sur site, le réenroulement et les modifications locales de tracé, l'équipe de remise en service ne peut pas prouver rapidement quels numéros de coulée ont fini dans quelles sections de branche installées. Le problème n'est pas le manque de papier. Le problème est que le papier ne correspond plus clairement à la réalité installée.
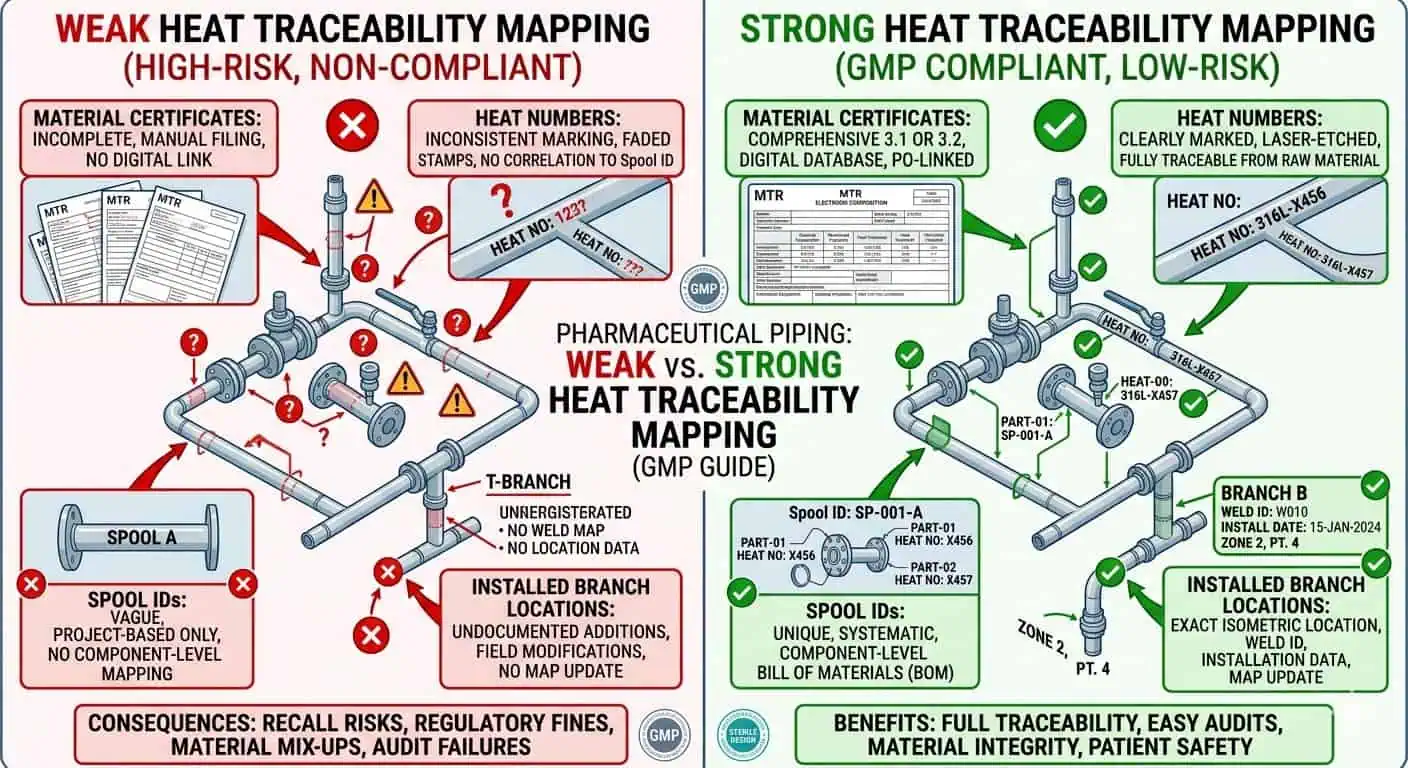
Conseil d'expert : dans les systèmes à contact produit à haute conséquence, définissez la matrice de traçabilité tôt au lieu de laisser les enregistrements de matériaux et les enregistrements de tuyaux évoluer séparément. Une fois que les modifications sur site commencent, reconstruire ce lien devient plus lent et moins fiable.
Cartes de soudure, Journaux de soudure orbitale et État d'inspection
La documentation de soudure est souvent la partie opérationnellement la plus importante de la chaîne de preuve de tuyauterie. Dans les systèmes agroalimentaires pharmaceutiques, les numéros de soudure, les paramètres machine, l'identité de l'opérateur, les dates, l'état d'inspection, l'historique des réparations et l'état d'acceptation sont souvent plus décisifs que les équipes ne le pensent. C'est parce que la soudure est l'endroit où l'identité du matériau, la qualité de fabrication, les preuves d'inspection et la performance hygiénique finale convergent. L'ASME BPE est utile ici non pas parce qu'il crée de la paperasse pour elle-même, mais parce qu'il traite la fabrication, l'examen, les tests et la certification comme un cadre de contrôle connecté. Dans les projets pharmaceutiques, les journaux de soudure ne sont donc pas seulement des enregistrements d'atelier. Ce sont des enregistrements de libération.
Cas d'ingénierie typique : une boucle semble acceptable lors de la visite, mais l'QA la signale toujours parce que la carte de soudure et la révision finale du tuyau ne sont plus alignées après les modifications sur site. Les soudures installées peuvent être physiquement acceptables, mais l'ensemble de documentation ne prouve plus quels enregistrements appartiennent à quels emplacements de soudure finaux.
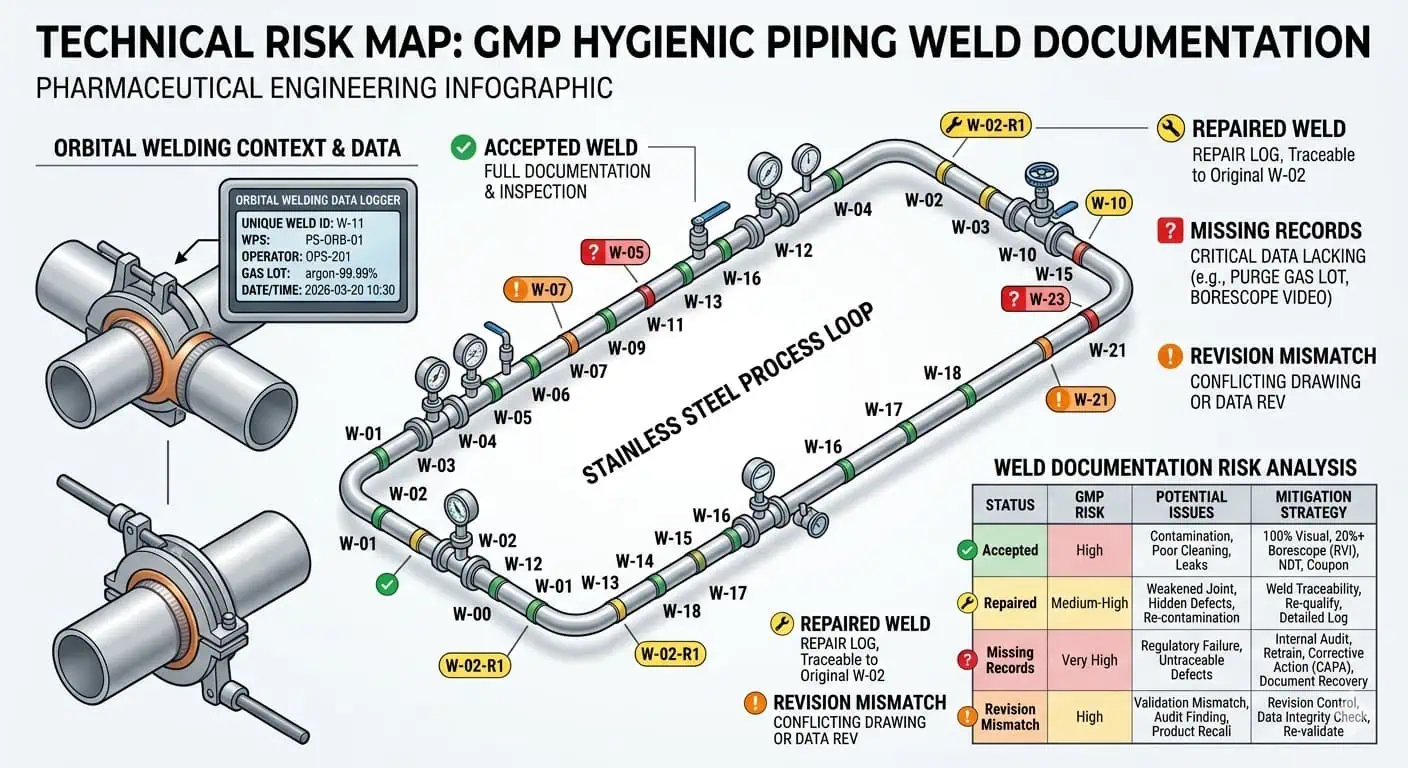
Conseil d'expert : ne gérez pas les enregistrements de soudure comme un ensemble de données uniquement de fabrication. Gérez-les comme un ensemble de données de libération qui doit encore avoir du sens après les modifications sur site, la substitution de tuyau et la clôture finale telle que construite.
Finition de surface, Électropolissage, Passivation et documents associés
Les exigences de finition n'ont d'importance que lorsque le projet peut prouver quelle finition était requise, quelle a été fournie et comment l'état final mouillé a été préservé. Dans les systèmes GMP plus exigeants, la décision de finition n'est pas séparée de la documentation. Si le projet différencie l'acier 316L standard de l'acier 316L électropoli, ou exige des preuves de passivation et de traitement post-fabrication, ces exigences nécessitent leur propre chemin d'enregistrement dans le dossier de remise.
Cas typique de l'industrie : La qualité du tube était acceptable, mais la discussion de libération s'est déplacée sur le fait de savoir si l'état final de surface de plusieurs pièces de tuyauterie en contact avec le produit correspondait toujours à l'attente hygiénique spécifiée après fabrication et retouche. L'alliage n'était pas le point faible. C'était l'état de finition documenté.
Conseil d'expert : Définissez la documentation liée à la finition avant le début de la fabrication. Si un projet décide tardivement que l'état de surface est plus important que prévu, les enregistrements manquants sont souvent beaucoup plus difficiles à reconstruire après fabrication que les certificats de matériau.
Lignes rouges, Plans d'exécution et Modifications sur site
Les modifications sur site sont là où les chaînes de traçabilité se rompent le plus souvent. Une branche est déplacée pour l'accès. Une pièce de tuyauterie est refaite pour s'adapter à l'assemblage réel. Un point d'instrumentation est révisé. L'orientation d'une vanne change. Aucune de ces actions n'est automatiquement fatale, mais chacune crée un risque documentaire si le processus de ligne rouge à plan d'exécution est faible. L'un des principes de documentation les plus importants dans la pratique GMP est que les enregistrements doivent être créés au moment où le travail se produit. Cela importe car les enregistrements reconstruits sont presque toujours plus faibles que ceux contemporains.
Cas industriel : Une connexion de skid GMP a été modifiée sur site pour améliorer le routage et l'accès à la maintenance. Le changement lui-même était raisonnable. Le problème était que les références de soudure mises à jour, les références de pièces de tuyauterie et les plans d'exécution ont pris du retard par rapport à l'installation. Au moment de la remise, l'équipe essayait de concilier deux versions techniquement similaires mais documentairement incohérentes de la même boucle.
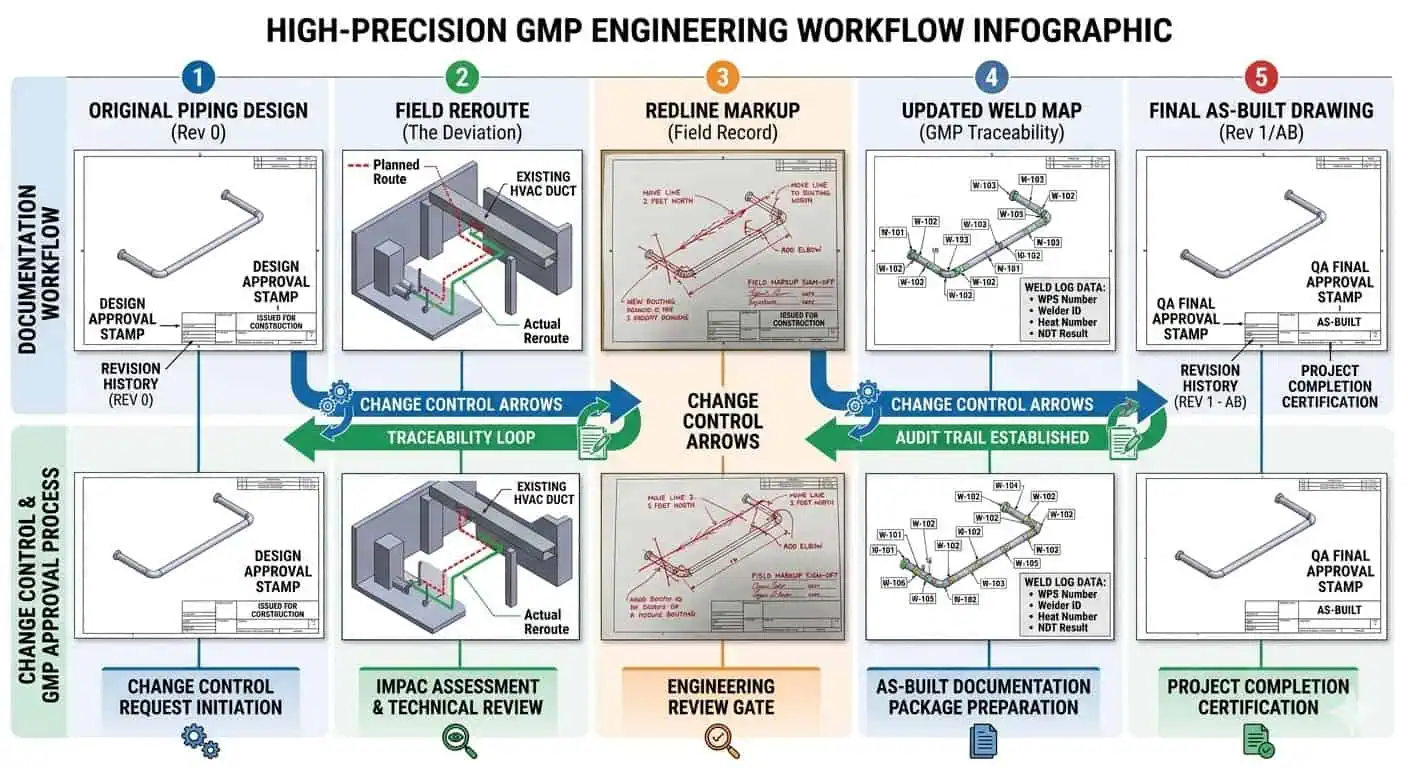
Conseil d'expert : Les redirections sur site ne sont pas le vrai problème. Les preuves non fermées provenant des redirections sur site sont le vrai problème. Le projet doit traiter les lignes rouges et les documents tels que construits comme des outils de contrôle actifs, et non comme des tâches de dessin en fin de phase.
Le paquet de documentation de base que les équipes GMP attendent généralement
Documentation des matériaux
La documentation des matériaux prouve que les matériaux approuvés en contact avec le fluide sont effectivement entrés dans le système. Au minimum, cela signifie généralement des certificats de matériaux, la traçabilité des lots, le contrôle de réception et une forme de cartographie de localisation qui lie les composants installés à l'ensemble des enregistrements de matériaux approuvés. Plus les conséquences hygiéniques ou de contact avec le produit sont importantes, moins il est acceptable de laisser cette relation vague.
Documentation de fabrication et de soudage
La documentation de fabrication prouve comment le système est devenu ce qu'il est. C'est là que se trouvent généralement les cartes de soudure, les journaux de soudure orbitale, les résultats d'inspection des soudures, les historiques de réparation, les enregistrements de boroscope si requis, et le suivi de l'état de fabrication. L'objectif n'est pas de créer un dossier épais pour lui-même. L'objectif est de maintenir la boucle installée vérifiable et techniquement défendable.
Documentation de surface et de traitement
Les enregistrements de surface sont importants chaque fois que la finition ou le traitement post-fabrication fait partie de l'exigence hygiénique. Si le projet spécifie l'électropolissage, la passivation ou un objectif de finition défini, le dossier de réception doit montrer comment cette exigence a été appliquée et comment les pièces concernées ont été identifiées. Sinon, le projet risque d'avoir une exigence de finition sur papier mais aucune preuve solide que la surface installée y corresponde encore.
Documentation des essais et de la réception
Les enregistrements des essais et de la réception transforment l'historique de fabrication en preuve de libération. Les essais de pression, les essais d'étanchéité, la clôture des inspections, la clôture de la liste des réserves et l'assemblage du dossier final sont les étapes où le projet démontre que la boucle fabriquée a non seulement été construite, mais aussi vérifiée et clôturée d'une manière qui soutient l'exploitation GMP.
Cas typique de l'industrie : le projet dispose de tous les enregistrements individuels quelque part, mais la réception est toujours bloquée parce que le dossier n'est pas structuré de la manière dont l'Assurance Qualité a besoin pour examiner et approuver la boucle. Ce n'est pas seulement un problème de document manquant. C'est un problème de logique de dossier.

Conseil d'expert : si les documents de réception sont assemblés pour la première fois seulement après l'achèvement mécanique, le projet est déjà en retard du point de vue du contrôle de la documentation.
Contrôle des modifications et enregistrements des écarts
La documentation des modifications est ce qui maintient la chaîne de preuves finale crédible. Le projet doit pouvoir montrer ce qui a changé, qui l'a approuvé, quelles inspections ou retouches ont suivi, et comment la condition finale telle que construite a intégré ce changement. Sans cela, même les modifications sur site techniquement raisonnables peuvent créer des hésitations inutiles en matière d'assurance qualité.
| Ensemble de documentation | Ce que cela prouve | Où cela échoue couramment |
|---|---|---|
| Certificats de matériaux et matrice de traçabilité | Les matériaux en contact avec le fluide approuvés ont effectivement été installés | La cartographie des emplacements devient floue après coupe ou reroutage sur site |
| Cartes de soudure et journaux de soudage | Les soudures finales ont été réalisées et inspectées sous contrôle | Les numéros de soudure cessent de correspondre aux révisions finales des tronçons |
| Finition / EP / enregistrements de passivation | L'état de surface spécifié a été atteint et préservé | Les retouches ou modifications tardives de finition ne sont pas entièrement documentées |
| Redlines et as-builts | La boucle installée correspond à la configuration finale approuvée | Les modifications sur site se produisent plus rapidement que la clôture des dessins |
| Dossier de remise | La chaîne complète de preuves est prête pour la revue QA | Des enregistrements existent, mais pas dans une structure prête pour la diffusion |
Où les chaînes de documentation se rompent généralement
Le matériau était correct, mais la matrice de traçabilité était faible.
L'un des échecs les plus courants n'est pas l'absence de matériau, mais une cartographie faible entre le matériau et son emplacement. Les équipes supposent parfois que la possession des certificats suffit. Ce n'est pas suffisant si le projet ne peut pas prouver rapidement où le matériau certifié s'est retrouvé après la coupe, la fabrication, le spooling et les modifications sur site.
Les soudures étaient acceptables, mais l'ensemble des enregistrements de soudure était incomplet.
Une boucle peut être techniquement correcte et échouer à la clôture de la documentation parce que l'ensemble des enregistrements de soudure est incomplet. L'absence de statut de soudure, un historique de réparation peu clair ou une numérotation de soudure mal alignée créent généralement plus de retard que les équipes ne l'attendent. Dans la tuyauterie GMP, la preuve de soudure n'est pas seulement un outil de fabrication. Elle fait partie de la préparation à la mise en service.
Les modifications sur site se sont produites plus rapidement que la mise à jour de la documentation.
La documentation prend souvent du retard sur le projet précisément au moment où le projet devient le plus dynamique. Les changements de tracé en fin de projet, les révisions de raccordement, les ajustements d'ajustement sur site et les branches ajoutées se produisent souvent sous pression de planning. Si l'ensemble des documents ne suit pas, le dossier final de remise devient un exercice de reconstruction au lieu d'une transmission contrôlée.
Les plus petits composants ont créé le plus gros problème d'assurance qualité.
Les petites pièces en contact avec le fluide créent un risque disproportionné de documentation. Les raccords, composants d'échantillonnage, diaphragmes, joints et pièces en contact avec le fluide liées aux instruments sont souvent là où la chaîne de preuve la plus propre se brise en premier. Les équipes ont tendance à penser en termes de conduites, mais l'assurance qualité vit souvent le projet en termes d'assemblages locaux non résolus.
Leçon d'expert tirée des travaux de clôture sur le terrain : plus l'assemblage est local et remplaçable, moins il est sûr de supposer que ses dossiers se géreront d'eux-mêmes.
Comment les ingénieurs doivent établir les exigences de documentation avant l'appel d'offres
Définir ce qui doit être traçable
Avant l'appel d'offres, définir quels composants en contact avec le fluide doivent rester traçables pendant l'installation et la mise en service. Si seul le tubage est contrôlé et que les plus petites pièces en contact avec le fluide sont laissées vagues, la chaîne de preuve sera généralement la plus faible là où l'assemblage hygiénique est le plus complexe.
Définir ce qui doit être enregistré pendant la fabrication
Les projets doivent définir ce qui doit être enregistré pendant que le travail se déroule, pas seulement ce qui doit exister à la fin. Les journaux de soudage, les points d'inspection, les enregistrements liés à la finition, les preuves de passivation le cas échéant, et les mises à jour des modifications sur site doivent faire partie du flux de projet défini.
Définir ce que l'assurance qualité doit recevoir lors de la remise
Le dossier de remise doit être défini comme un livrable de libération, et non comme une collection vague de ce que l'entrepreneur peut assembler ultérieurement. Si l'assurance qualité attend une structure de dossier spécifique, une matrice de traçabilité ou un format d'enregistrement, le projet doit le définir pendant qu'il a encore le temps de générer ces enregistrements correctement.
Définir ce qui doit être maintenu après la mise en service
La chaîne de documentation doit survivre en exploitation, et non s'arrêter à la remise. Les journaux d'équipement, les enregistrements de maintenance, la traçabilité des pièces de rechange, et les mises à jour contrôlées du système installé font tous partie du maintien de la chaîne de preuves originale. Un système prêt pour la libération peut devenir beaucoup plus difficile à défendre ultérieurement si les enregistrements du cycle de vie sont faibles.
Le conseil de projet le plus solide est simple : définir la chaîne de preuves avant l'approvisionnement. N'attendez pas que la fabrication soit en cours pour décider si la traçabilité thermique, les enregistrements de finition, l'état de soudage ou la documentation des modifications sur site seront importants. À ce stade, le projet finit généralement par collecter des documents de manière réactive au lieu de les contrôler délibérément. C'est l'une des leçons pratiques les plus claires du travail de remise GMP : les projets qui définissent l'ensemble des enregistrements avant l'appel d'offres se terminent généralement plus rapidement et avec moins de surprises pour l'assurance qualité que les projets qui tentent de le reconstruire ultérieurement.
Comment cela se connecte à la conception, aux matériaux et à la sélection des raccords
Sélection des matériaux sans contrôle documentaire n'est pas un risque clos
Une bonne décision matérielle ne devient une décision de projet sûre que lorsqu'elle est documentée clairement. Pour la logique plus large côté matériaux, connectez cette page avec Sélection des matériaux pour tuyauterie hygiénique pharmaceutique.
Les exigences de finition n'ont d'importance que si elles sont prouvées
L'électropolissage, les cibles de finition et les attentes post-traitement ne ferment pas le risque à moins que les dossiers ne les prouvent. Liez ce sujet avec Acier inoxydable 316L électropoli vs 316L standard.
Les raccords et assemblages échantillons ont besoin de leur propre chaîne de preuve
Plus l'assemblage devient petit et local, plus sa documentation risque de devenir la partie la plus faible du dossier de remise. Liez ce sujet avec Sélection de raccords agroalimentaires pour installations GMP.
La documentation telle que construite doit refléter le réel risque de nettoyabilité
La documentation ne doit pas seulement prouver ce qui a été installé. Elle doit également refléter la réalité hygiénique finale locale du système. Pour cette logique, connectez cette page avec Considérations de conception CIP pour les tuyauteries agroalimentaires.
Erreurs courantes dans la documentation et la traçabilité pour les projets de tuyauterie pharmaceutique
Traiter la documentation comme une activité de remise au lieu d'une entrée de conception
Les projets qui définissent le dossier documentaire tardivement finissent généralement par reconstruire les dossiers sous pression de planning.
Suivi des tubes mais pas des petits composants en contact avec le fluide
Le maillon le plus faible de la traçabilité apparaît souvent dans les raccords, joints, diaphragmes ou assemblages d'échantillonnage locaux.
Conserver les données de soudure séparées de la logique de libération au niveau de la ligne
Les dossiers de soudure sont beaucoup moins utiles s'ils ne sont pas clairement associés à la boucle installée finale et son statut de libération.
Laisser les modifications rouges s'éloigner de la réalité installée
Lorsque les modifications sur site avancent plus vite que les mises à jour contrôlées, le dossier de remise devient plus difficile à faire confiance.
En supposant que l'assurance qualité l'acceptera plus tard
Dans les tuyauteries GMP, l'absence de preuve est rarement plus facile à corriger à la fin du projet que pendant l'exécution contrôlée.
Surcollecte de documents mais sous-définition de ce qui compte réellement
De grands volumes de documents ne créent pas automatiquement un dossier de remise solide. Ce qui compte, c'est si l'ensemble des enregistrements prouve suffisamment clairement le système hygiénique installé pour la libération et le contrôle ultérieur du cycle de vie.
Liste de contrôle pratique : questions à poser avant de libérer un système de tuyauterie pharmaceutique
Avant le début de la fabrication
- Quels composants en contact avec le fluide doivent être traçables ?
- Quels enregistrements doivent être créés pendant la fabrication ?
- Quelles preuves de soudure, de finition et d'inspection l'assurance qualité exigera-t-elle plus tard ?
- Comment les modifications sur site seront-elles intégrées dans les enregistrements contrôlés ?
Avant l'achèvement mécanique
- Les modifications sont-elles à jour ?
- Les composants installés correspondent-ils clairement aux enregistreements de matériaux approuvés ?
- L'état des soudures et l'historique des réparations sont-ils clôturés ?
- Les enregistrements de finition et de traitement sont-ils complets là où requis ?
Avant la libération QA
- Le dossier de remise correspond-il à la boucle installée réelle ?
- Des assemblages locaux sont-ils encore non résolus dans la traçabilité ou les enregistrements d'inspection ?
- Le projet peut-il prouver l'état final tel que construit suffisamment clairement pour la libération ?
Après la mise en service
- Comment les journaux d'équipement et les dossiers de maintenance vont-ils continuer ?
- Comment les pièces de rechange resteront-elles traçables ?
- Comment les changements futurs seront-ils rattachés à la chaîne de preuves originale ?
| Étape du projet | Question clé de documentation | À quoi ressemble un bon contrôle |
|---|---|---|
| Avant le RFQ | Qu'est-ce qui doit être traçable et livrable ? | L'ensemble des dossiers est défini, non supposé |
| Pendant la fabrication | Les enregistrements sont-ils créés en temps réel ? | Les enregistrements de soudure, de matériau, de finition et de modification restent à jour |
| Avant la remise | Le dossier correspond-il à la réalité installée ? | Les documents d'exécution, la traçabilité et la clôture des inspections sont alignés |
| Après la mise en service | La chaîne de preuves survivra-t-elle aux changements du cycle de vie ? | Les enregistrements de maintenance et de remplacement restent sous contrôle |
Conclusion : Dans la tuyauterie pharmaceutique, la documentation prouve que le système que vous pensez avoir construit est le système que vous avez réellement installé
Une bonne documentation et une traçabilité efficace n'ajoutent pas de valeur après le projet. Elles protègent le projet de devenir inexploitable au moment précis où il devrait être prêt à fonctionner. Dans les canalisations pharmaceutiques, le système installé n'est acceptable que si la chaîne de preuves qui atteste de la maîtrise de son matériau, de sa fabrication, de sa finition, de son inspection et de ses modifications est établie.
Les projets les plus solides ne tentent pas de reconstituer cette chaîne de preuves lors de la remise. Ils la définissent avant l'appel d'offres, la maintiennent pendant la fabrication et la clôturent avant la libération. Pour l'ensemble du cluster thématique pharmaceutique, reliez cet article avec Sélection des matériaux pour tuyauterie hygiénique pharmaceutique, Acier inoxydable 316L électropoli vs 316L standard, Sélection de raccords agroalimentaires pour installations GMPet Considérations de conception CIP pour les tuyauteries agroalimentaires.
FAQ
Quelle documentation est requise pour les projets de tuyauterie pharmaceutique ?
Le package exact dépend de la portée du projet, mais elle inclut généralement des certificats de matériaux, des registres de traçabilité, une documentation de soudage, des registres d'inspection, des preuves de finition ou de traitement si nécessaire, des modifications rouges, des plans d'exécution et des registres de remise qui soutiennent la libération QA.
Quelle traçabilité est requise dans les tuyauteries agroalimentaires ?
La traçabilité doit suivre le chemin mouillé. Cela signifie souvent que les tubes, les raccords, les vannes, les assemblages locaux et d'autres composants critiques en contact avec le produit doivent être traçables jusqu'à des registres approuvés d'une manière qui correspond toujours à l'état installé.
Pourquoi les projets de tuyauterie pharmaceutique échouent-ils lors de la mise en service ?
Ils échouent souvent parce que la chaîne de preuves est incomplète. L'installation peut être physiquement acceptable, mais des registres manquants ou faibles sur le matériau, la soudure, la finition ou les plans d'exécution peuvent encore retarder la libération QA.
Les raccords et les joints nécessitent-ils une traçabilité dans les projets GMP ?
Dans de nombreuses applications agroalimentaires critiques, oui. Les plus petits composants mouillés sont souvent là où le maillon de documentation le plus faible apparaît, ils ne doivent donc pas être traités comme des consommables occasionnels s'ils influencent la performance hygiénique ou le risque de libération.
Les registres de soudage sont-ils requis pour les tuyauteries agroalimentaires pharmaceutiques ?
Les projets s'appuient couramment sur des cartes de soudage et une documentation de soudage parce qu'elles sont centrales pour prouver l'état de fabrication et d'inspection. Le format exact varie selon le projet, mais la documentation de soudure insuffisante est l'un des problèmes de transfert les plus courants.
Quelle est la différence entre les dossiers d'exécution et les documents de remise ?
Les enregistrements tels que construits montrent la configuration finale installée. Les documents de transfert constituent le dossier de preuves plus large utilisé pour soutenir la libération, y compris la traçabilité, l'inspection, les essais et les dossiers de projet connexes.



