La documentación y trazabilidad en proyectos de tuberías farmacéuticas no son papeleo añadido después de la instalación. Son la cadena de evidencia que demuestra que el sistema instalado coincide con el material aprobado, acabado, soldadura, inspección e intención de diseño higiénico. En proyectos GMP, un circuito de tuberías puede estar mecánicamente completo y aún permanecer no liberable porque la documentación no demuestra claramente qué se instaló, cómo se fabricó, qué cambió en campo y si el ensamblaje final aún cumple con el estándar aprobado del proyecto.
Por eso los ingenieros experimentados no tratan los documentos de entrega como una transferencia administrativa. Los tratan como parte del control de diseño del proyecto desde el principio. Si la trazabilidad de materiales, registros de soldadura, registros de acabado, evidencia de inspección, modificaciones en rojo y entregables de entrega no se definen antes de la RFQ, el proyecto a menudo intenta reconstruir la cadena de evidencia después a un costo mucho mayor y con menor confianza. Esta guía explica qué significan realmente la documentación y trazabilidad en proyectos de tuberías farmacéuticas, qué registros importan más, dónde suele romperse la cadena de evidencia y cómo los equipos GMP pueden definir el paquete de documentación correcto antes de que comience la fabricación.
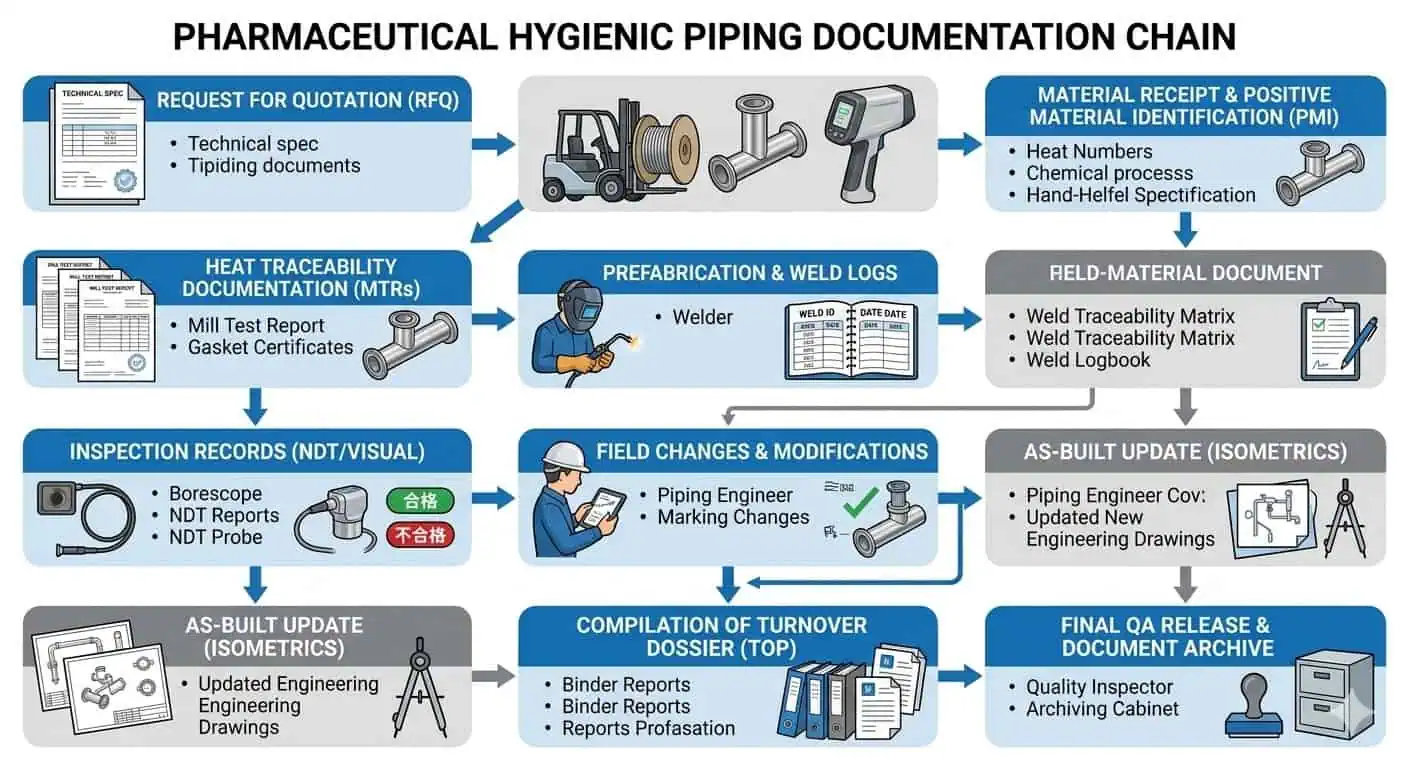
En el trabajo farmacéutico real, los problemas de documentación rara vez aparecen como fallas mecánicas dramáticas. Se manifiestan como cierre de QA más lento, comentarios de entrega no resueltos, linaje de soldadura poco claro, historiales de tramos no coincidentes o incertidumbre sobre si el circuito instalado final aún refleja la intención higiénica aprobada. Por eso una documentación sólida no es una preferencia de papeleo. Es un control de ingeniería.
Por qué importan la documentación y trazabilidad en proyectos de tuberías farmacéuticas
Este es un tema de QA y liberación, no solo un tema de archivo de ingeniería
En tuberías farmacéuticas, la documentación es parte del control de liberación, no solo de la administración del proyecto. El Capítulo 4 de la GMP de la UE no describe la documentación como una conveniencia de archivo. Describe la buena documentación como una parte esencial del sistema de garantía de calidad y el mecanismo utilizado para establecer, controlar, monitorear y registrar actividades que afectan la calidad del producto. La lógica de la FDA apunta en la misma dirección: el equipo en contacto con el producto debe ser adecuado para su uso, y la limpieza, mantenimiento e historial del equipo deben controlarse y registrarse. En otras palabras, el circuito instalado debe ser técnicamente correcto y demostrablemente correcto al mismo tiempo.
Caso típico de la industria: Un circuito de transferencia en contacto con el producto está completamente instalado, probado a presión y visualmente aceptable. Operaciones ve un sistema de tuberías terminado. QA ve una cadena de evidencia incompleta porque el expediente final aún no puede vincular claramente la identidad del material aprobado, el historial de soldadura y la configuración final como-construido. La tubería está físicamente allí, pero la lógica de liberación aún no está resuelta.
Consejo experto: Si el equipo del proyecto trata la documentación como algo que comienza en la entrega, ya es demasiado tarde. En tuberías GMP, la historia de liberación debe construirse mientras el circuito se está diseñando, fabricando, inspeccionando y modificando, no después de que se apriete la última abrazadera.
Nota de ingeniería: en tuberías GMP, el circuito instalado solo es tan liberable como la cadena de evidencia que demuestra su condición final mojada.
Por qué los proyectos de tuberías farmacéuticas a menudo fallan en la entrega, no en la fabricación
Muchos proyectos de tuberías farmacéuticas no fallan porque el circuito estuviera mal construido. Fallan porque el proyecto no puede demostrar, en forma lista para liberación, que el circuito instalado final aún coincide con la intención higiénica aprobada. Ese es un tipo diferente de falla, pero en el trabajo GMP a menudo es el más peligroso porque aparece tarde, después de que el sistema ya parece mecánicamente completo. La lógica de mantenimiento de registros del Capítulo 4 de la UE GMP y la FDA respaldan la misma conclusión práctica: si el historial de limpieza, la identidad de los componentes, el estado de las soldaduras y la configuración instalada no pueden reconstruirse de manera confiable, el sistema se vuelve más difícil de defender en la liberación y más tarde durante la operación.
Caso típico de la industria: El equipo de instalación en campo termina un circuito higiénico y asume que el trabajo difícil ha terminado. Una revisión posterior muestra que varias piezas de tramo se revisaron en el campo para mejorar el enrutamiento y la pendiente, pero el mapa final de soldaduras, la matriz de ubicación de materiales y el paquete como construido nunca se reconciliaron por completo. Nadie afirma que el metal esté mal. El problema es que el proyecto ya no puede demostrar claramente qué materiales certificados, registros de soldadura y resultados de inspección pertenecen al arreglo instalado final. En ese punto, el circuito no está luchando contra un defecto de fabricación. Está luchando contra un defecto de evidencia de liberación.
Por lo tanto, los ingenieros de proyecto experimentados definen la cadena de documentación antes de la RFQ, no después de la finalización mecánica. Una vez que comienza la fabricación, cada corte de campo no controlado, intercambio de tramo o redirección de ramal se vuelve más difícil de cerrar retroactivamente. La lección de ingeniería es simple: en tuberías GMP, si espera hasta la entrega para decidir qué debe ser rastreable, el proyecto generalmente termina reconstruyendo la cadena de evidencia a un costo mayor y con menor confianza.
Lo que realmente requiere el marco GMP y regulatorio
Las regulaciones más útiles son las que cambian lo que el equipo del proyecto define y registra antes de la entrega. En este tema, el marco central generalmente incluye:
- ASME BPE, que abarca materiales, diseño, fabricación, inspecciones, pruebas y lógica de certificación para equipos de bioprocesamiento y farmacéuticos.
- FDA 21 CFR 211.65, que requiere que las superficies en contacto con el producto sean no reactivas, no aditivas y no absorbentes.
- FDA 21 CFR 211.67, que vincula la limpieza y el mantenimiento del equipo con procedimientos escritos y registros.
- FDA 21 CFR 211.182, que aborda los registros de limpieza, mantenimiento y uso para equipos principales.
- FDA 21 CFR 211.184, que cubre registros de componentes, contenedores, cierres y etiquetado.
- EU GMP Capítulo 4, que define la documentación como una parte esencial del sistema de garantía de calidad y requiere que los registros sean controlados, precisos, trazables y retenidos adecuadamente.
Conclusión de la investigación: estas fuentes no tratan la documentación como soporte de fondo. La tratan como una parte controlada de la ejecución de GMP. Para los equipos de tuberías, eso significa que la pregunta nunca es solo “¿qué registros tenemos?” sino “¿estos registros aún prueban el sistema húmedo final con suficiente claridad para la liberación de QA?”
Qué Debe Ser Rastreable en un Proyecto de Tuberías GMP
Tubería, Accesorios, Válvulas y Otros Componentes Húmedos
La rastreabilidad debe seguir la ruta húmeda, no solo los componentes más grandes o más fáciles. Muchos equipos gestionan bien la tubería pero tratan los accesorios más pequeños, diafragmas, válvulas de muestreo, férulas, juntas y componentes de ramificación con demasiada informalidad. En proyectos GMP, eso es un error. Las partes húmedas más pequeñas suelen ser las más fáciles de sustituir, las más difíciles de rastrear después y las primeras en generar preguntas de QA durante la entrega.
Caso típico de la industria: la rastreabilidad de la tubería está completa, pero el paquete de entrega se debilita en los ensamblajes locales porque los accesorios, juntas o internos de válvulas de muestreo se manejaron fuera del flujo de trabajo de control principal. La línea parece bien en la inspección, pero el eslabón más débil de rastreabilidad se encuentra exactamente donde el ensamblaje higiénico es más complejo.
Consejo experto: si un componente es lo suficientemente importante como para ser especificado como parte del diseño higiénico, es lo suficientemente importante como para ser rastreable como parte de la lógica de entrega. En la práctica, los equipos obtienen un mejor cierre de QA cuando definen la rastreabilidad alrededor de la ruta húmeda completa en lugar de solo alrededor de la tubería.
Certificados de Material, Números de Lote e Identidad de Lote
La rastreabilidad de materiales solo es útil cuando la ubicación instalada puede vincularse claramente con el conjunto de registros original. Los informes de prueba de materiales, certificados EN 10204 3.1, números de lote y registros de recepción son importantes, pero solo si el proyecto preserva el vínculo entre la identidad del proveedor y la ubicación instalada del tramo, accesorio o ensamblaje. Un montón de certificados sin una matriz de ubicación clara no es un paquete de rastreabilidad sólido.
Caso típico de la industria: el proyecto tiene los certificados de material correctos en mano, pero después del corte en campo, el reenrollado y el redireccionamiento local, el equipo de entrega no puede demostrar rápidamente qué números de colada terminaron en qué secciones de ramal instaladas. El problema no es la falta de papel. El problema es que el papel ya no se corresponde claramente con la realidad instalada.
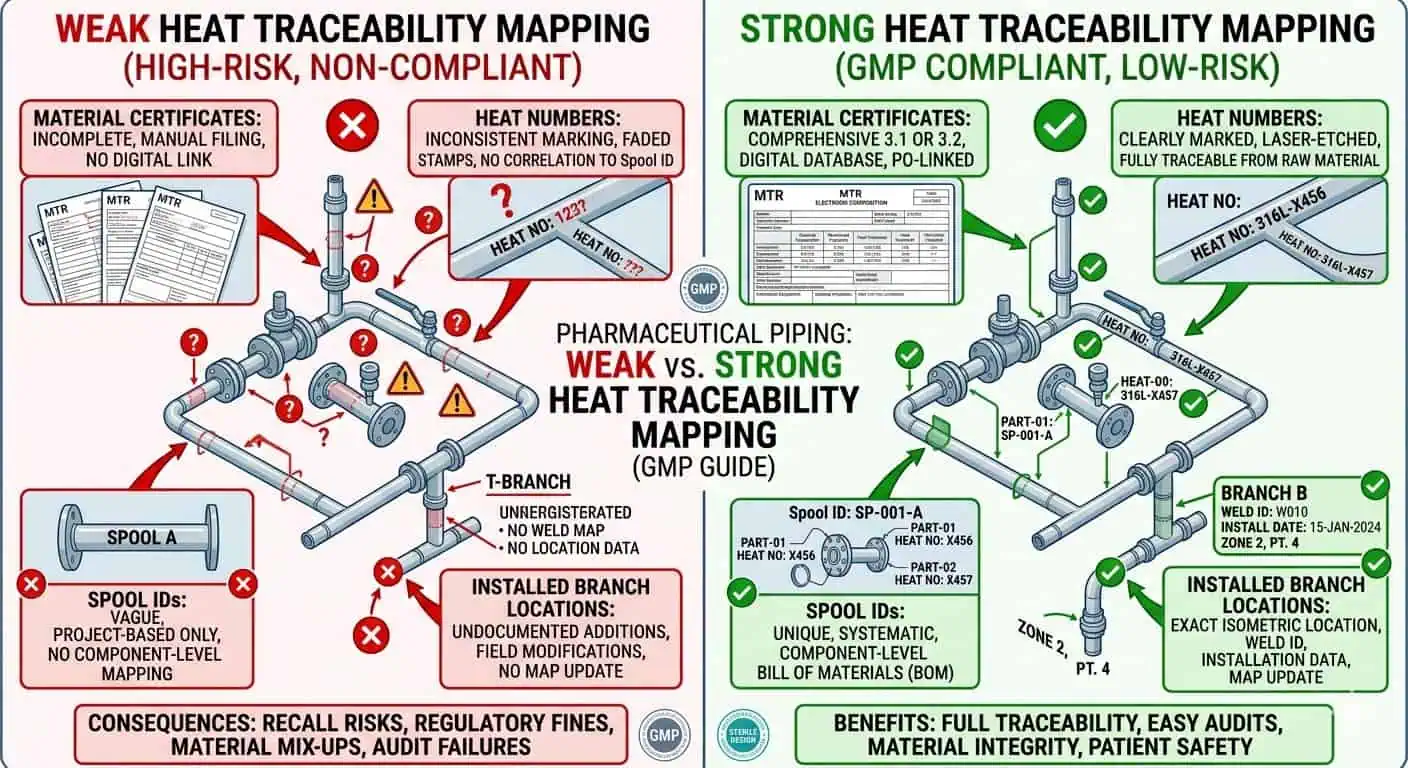
Consejo experto: en sistemas de contacto con productos de alta consecuencia, defina la matriz de trazabilidad temprano en lugar de permitir que los registros de material y los registros de tramos evolucionen por separado. Una vez que comienzan las modificaciones en campo, reconstruir ese vínculo se vuelve más lento y menos confiable.
Mapas de Soldadura, Registros de Soldadura Orbital y Estado de Inspección
La documentación de soldadura es a menudo la parte operativamente más importante de la cadena de evidencia de tuberías. En sistemas higiénicos farmacéuticos, los números de soldadura, configuraciones de máquina, identidad del operador, fechas, estado de inspección, historial de reparaciones y estado de aceptación suelen ser más decisivos de lo que los equipos esperan. Esto se debe a que la soldadura es donde convergen la identidad del material, la calidad de fabricación, la evidencia de inspección y el rendimiento higiénico final. ASME BPE es útil aquí no porque cree papeleo por sí mismo, sino porque trata la fabricación, el examen, las pruebas y la certificación como un marco de control conectado. En proyectos farmacéuticos, los registros de soldadura no son solo registros de taller. Son registros de liberación.
Caso típico de ingeniería: un circuito parece aceptable en la inspección visual, pero QA aún lo marca porque el mapa de soldadura y la revisión final del tramo ya no están alineados después de los cambios en campo. Las soldaduras instaladas pueden ser físicamente aceptables, pero el conjunto de documentación ya no prueba qué registros pertenecen a qué ubicaciones finales de soldadura.
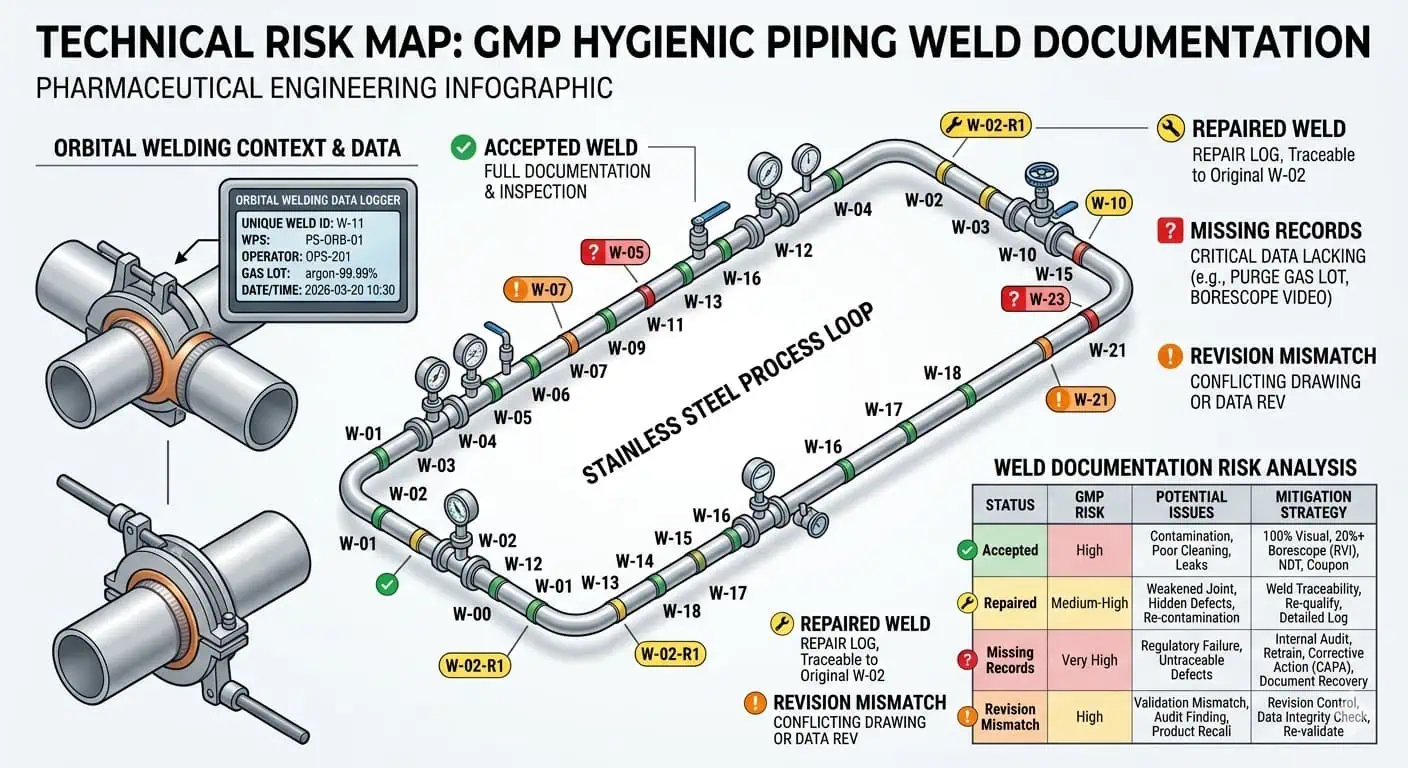
Consejo experto: no gestione los registros de soldadura como un conjunto de datos solo de fabricación. Gestiónelos como un conjunto de datos de liberación que aún debe tener sentido después de los cambios en campo, la sustitución de tramos y el cierre final como construido.
Acabado Superficial, Electropulido, Pasivación y Registros Relacionados
Los requisitos de acabado solo importan cuando el proyecto puede demostrar qué acabado se requería, qué se suministró y cómo se preservó la condición final mojada. En sistemas GMP más exigentes, la decisión de acabado no está separada de la documentación. Si el proyecto diferencia entre 316L estándar y 316L electropulido, o requiere evidencia de pasivación y tratamiento posterior a la fabricación, esos requisitos necesitan su propia ruta de registro en el dossier de entrega.
Caso típico de la industria: el grado del tubo era aceptable, pero la discusión de liberación cambió a si la condición superficial final de varias piezas de tramo en contacto con el producto aún coincidía con la expectativa higiénica especificada después de la fabricación y el reprocesamiento. La aleación no era el punto débil. La condición de acabado documentada sí lo era.
Consejo experto: definir la documentación relacionada con el acabado antes de que comience la fabricación. Si un proyecto decide tarde que la condición superficial importa más de lo esperado, los registros faltantes a menudo son mucho más difíciles de reconstruir después de la fabricación que los certificados de material.
Líneas Rojas, Como Construido y Cambios en Campo
Los cambios en campo son donde las cadenas de trazabilidad se rompen con mayor frecuencia. Una rama se mueve para acceso. Un tramo se rehace para adaptarse al ajuste real. Un punto de instrumento se revisa. La orientación de una válvula cambia. Ninguna de estas acciones es automáticamente fatal, pero cada una crea riesgo de documentación si el proceso de línea roja a como construido es débil. Uno de los principios de documentación más importantes en la práctica GMP es que los registros deben crearse en el momento en que ocurre el trabajo. Eso importa porque los registros reconstruidos casi siempre son más débiles que los contemporáneos.
Caso de la industria: una conexión de skid GMP se cambió en el campo para mejorar el enrutamiento y el acceso de mantenimiento. El cambio en sí era razonable. El problema fue que las referencias de soldadura actualizadas, las referencias de tramo y los dibujos como construido se retrasaron respecto a la instalación. Para la entrega, el equipo intentaba reconciliar dos versiones técnicamente similares pero documentalmente inconsistentes del mismo bucle.
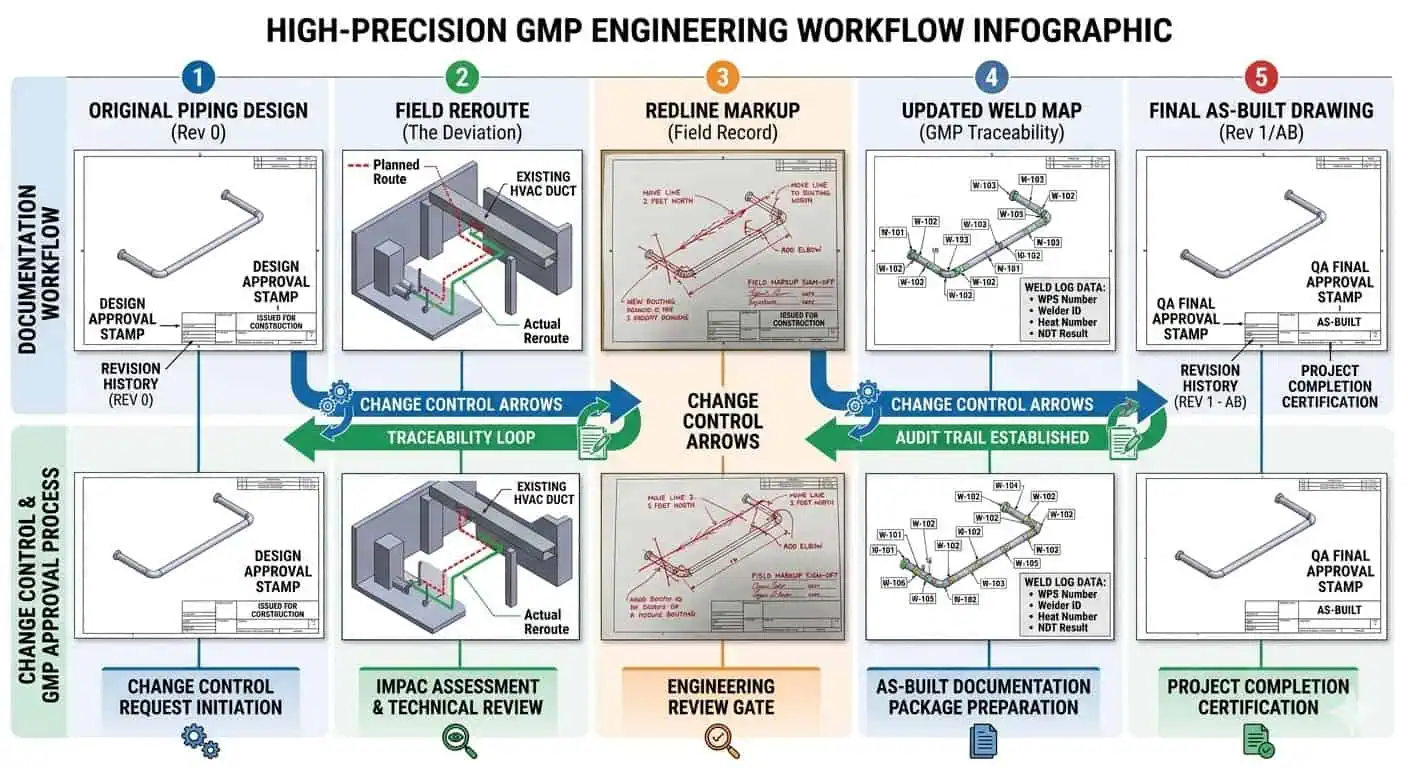
Consejo experto: Las reubicaciones de campo no son el problema real. La evidencia no cerrada de las reubicaciones de campo es el problema real. El proyecto debe tratar las líneas rojas y los como construidos como herramientas de control activas, no como tareas de dibujo en etapa final.
El Paquete de Documentación Central que los Equipos de GMP Generalmente Esperan
Documentación de Materiales
La documentación de materiales demuestra que los materiales húmedos aprobados realmente ingresaron al sistema. Como mínimo, esto generalmente significa certificados de materiales, trazabilidad térmica, control de recepción y alguna forma de mapeo de ubicación que vincula los componentes instalados con el conjunto de registros de materiales aprobados. Cuanto más fuerte sea la consecuencia higiénica o de contacto con el producto, menos aceptable se vuelve dejar esta relación vaga.
Documentación de Fabricación y Soldadura
La documentación de fabricación demuestra cómo el sistema se convirtió en lo que es. Aquí es donde generalmente se encuentran los mapas de soldadura, los registros de soldadura orbital, los resultados de inspección de soldadura, los historiales de reparación, los registros de boroscopio cuando se requieren y el seguimiento del estado de fabricación. El punto no es crear un dossier grueso por sí mismo. El punto es mantener el circuito instalado auditable y técnicamente defendible.
Documentación de Superficie y Tratamiento
Los registros de superficie importan cuando el acabado o el tratamiento posterior a la fabricación forman parte del requisito de grado alimentario. Si el proyecto especifica electropulido, pasivación o un objetivo de acabado definido, el paquete de entrega debe mostrar cómo se aplicó ese requisito y cómo se identificaron las partes relevantes. De lo contrario, el proyecto corre el riesgo de tener un requisito de acabado en papel pero sin evidencia sólida de que la superficie instalada aún coincida con él.
Documentación de Pruebas y Entrega
Los registros de pruebas y entrega convierten el historial de fabricación en evidencia de liberación. Las pruebas de presión, pruebas de fugas, cierre de inspección, cierre de lista de pendientes y ensamblaje del dossier final son donde el proyecto demuestra que el circuito fabricado no solo se construyó, sino que también se verificó y cerró de una manera que respalda la operación GMP.
Caso típico de la industria: el proyecto tiene todos los registros individuales en algún lugar, pero la entrega aún se estanca porque el paquete no está estructurado de la manera que QA necesita para revisar y aprobar el circuito. Esto no es solo un problema de documentos faltantes. Es un problema de lógica del dossier.

Consejo experto: si los documentos de entrega se están ensamblando por primera vez solo después de la finalización mecánica, el proyecto ya está retrasado desde una perspectiva de control de documentación.
Registros de Control de Cambios y Desviaciones
La documentación de cambios es lo que mantiene creíble la cadena de evidencia final. El proyecto debe poder mostrar qué cambió, quién lo aprobó, qué inspección o retrabajo siguió y cómo la condición final as-built absorbió ese cambio. Sin eso, incluso los cambios de campo técnicamente razonables pueden crear una indecisión innecesaria en el control de calidad.
| Conjunto de Documentación | Lo que Demuestra | Donde Falla Comúnmente |
|---|---|---|
| Certificados de material y matriz de trazabilidad | Los materiales húmedos aprobados fueron realmente instalados | El mapeo de ubicación se vuelve poco claro después del corte o reruteo de campo |
| Mapas de soldadura y registros de soldadura | Las soldaduras finales se completaron e inspeccionaron bajo control | Los números de soldadura dejan de coincidir con las revisiones finales de los spools |
| Acabado / EP / registros de pasivación | La condición superficial especificada fue lograda y preservada | Retrabajos o cambios de acabado tardíos no están completamente documentados |
| Marcas rojas y como-construidos | El circuito instalado coincide con la configuración final aprobada | Los cambios en campo ocurren más rápido que el cierre de planos |
| Dossier de entrega | La cadena completa de evidencia está lista para revisión de QA | Existen registros, pero no en una estructura lista para liberación |
Donde las Cadenas de Documentación Usualmente se Rompen
El material era correcto, pero la matriz de trazabilidad era débil
Una de las fallas más comunes no es la falta de material, sino un mapeo débil entre el material y su ubicación. Los equipos a veces asumen que tener los certificados es suficiente. No es suficiente si el proyecto no puede demostrar rápidamente dónde terminó el material certificado después del corte, fabricación, enrollado y cambios en campo.
Las soldaduras eran aceptables, pero el conjunto de registros de soldadura estaba incompleto
Un circuito puede ser técnicamente sólido y aún así fallar en el cierre de documentación porque el conjunto de registros de soldadura está incompleto. La falta de estado de soldadura, historial de reparación poco claro o numeración de soldadura desalineada generalmente crea más retraso del que los equipos esperan. En tuberías GMP, la evidencia de soldadura no es solo una herramienta de fabricación. Es parte de la preparación para la liberación.
Los cambios en campo ocurrieron más rápido que la actualización de la documentación
La documentación a menudo se queda atrás del proyecto justo en el momento en que el proyecto se vuelve más dinámico. Los cambios de enrutamiento en etapas tardías, revisiones de conexión, ajustes de ajuste en campo y ramas agregadas a menudo ocurren bajo presión de programación. Si el conjunto de documentos no se mantiene al día, el paquete de entrega final se convierte en un ejercicio de reconstrucción en lugar de una entrega controlada.
Los componentes más pequeños crearon el mayor problema de QA
Las pequeñas partes en contacto con el fluido generan un riesgo documental desproporcionado. Los accesorios, componentes de muestreo, diafragmas, juntas y partes en contacto con el fluido relacionadas con instrumentos suelen ser donde la cadena de evidencia más limpia se rompe primero. Los equipos tienden a pensar en términos de tramos de tubería, pero el control de calidad a menudo experimenta el proyecto en términos de ensamblajes locales no resueltos.
Lección experta del trabajo de cierre en campo: cuanto más local y reemplazable sea el ensamblaje, menos seguro es asumir que sus registros se cuidarán solos.
Cómo deben los ingenieros construir los requisitos de documentación antes de la RFQ
Definir lo que debe ser rastreable
Antes de la RFQ, defina qué componentes en contacto con el fluido deben permanecer rastreables durante la instalación y entrega. Si solo se controla la tubería y las partes más pequeñas en contacto con el fluido se dejan vagas, la cadena de evidencia generalmente será más débil donde el ensamblaje higiénico es más complejo.
Definir lo que debe registrarse durante la fabricación
Los proyectos deben definir lo que debe registrarse mientras se realiza el trabajo, no solo lo que debe existir al final. Los registros de soldadura, los puntos de inspección, los registros relacionados con el acabado, la evidencia de pasivación cuando sea relevante y las actualizaciones de cambios en campo deben ser parte del flujo de proyecto definido.
Definir lo que QA debe recibir en la entrega
El paquete de entrega debe definirse como un entregable de liberación, no como una colección vaga de lo que el contratista pueda reunir después. Si QA espera una estructura específica de dossier, una matriz de trazabilidad o un formato de registro, el proyecto debe definir eso mientras aún tiene tiempo para generar esos registros correctamente.
Definir lo que debe mantenerse después del arranque
La cadena de documentación debe sobrevivir en la operación, no detenerse en la entrega. Los registros de equipos, los registros de mantenimiento, la trazabilidad de piezas de repuesto y las actualizaciones controladas al sistema instalado son parte de mantener viva la cadena de evidencia original. Un sistema listo para liberación puede volverse mucho más difícil de defender después si los registros del ciclo de vida son débiles.
El consejo de proyecto más sólido es simple: defina la cadena de evidencia antes de la adquisición. No espere hasta que la fabricación esté en marcha para decidir si la trazabilidad térmica, los registros de acabado, el estado de soldadura o la documentación de cambios en campo importarán. En ese punto, el proyecto generalmente termina recopilando documentos de manera reactiva en lugar de controlarlos deliberadamente. Esta es una de las lecciones prácticas más claras del trabajo de entrega GMP: los proyectos que definen el conjunto de registros antes de la RFQ generalmente se cierran más rápido y con menos sorpresas de QA que los proyectos que intentan reconstruirlo después.
Cómo esto se conecta con la selección de diseño, material y accesorios
Selección de Material Sin Control de Documentación No Es Riesgo Cerrado
Una buena decisión de material solo se convierte en una decisión de proyecto segura cuando está documentada claramente. Para la lógica más amplia del lado de materiales, conecte esta página con Selección de Material de Tuberías Higiénicas Farmacéuticas.
Los Requisitos de Acabado Solo Importan Si Se Prueban
El electropulido, los objetivos de acabado y las expectativas de postratamiento no cierran el riesgo a menos que los registros los prueben. Enlace este tema con Acero Inoxidable 316L Electropulido vs 316L Estándar.
Los Accesorios y Ensamblajes de Muestra Necesitan Su Propia Cadena de Evidencia
Cuanto más pequeño y más local se vuelve el ensamblaje, más probable es que su documentación se convierta en la parte más débil del paquete de entrega. Enlace este tema con Selección de Conexiones de Grado Alimentario para Instalaciones GMP.
La Documentación Como Construida Debe Reflejar el Riesgo Real de Limpieza
La documentación no solo debe probar lo que se instaló. También debe reflejar la realidad higiénica final local del sistema. Para esa lógica, conecte esta página con Consideraciones de Diseño de CIP para Tubería Higiénica.
Errores Comunes en la Documentación y Trazabilidad para Proyectos de Tuberías Farmacéuticas
Tratar la Documentación como una Actividad de Entrega en Lugar de una Entrada de Diseño
Los proyectos que definen el paquete de documentación tarde suelen terminar reconstruyendo registros bajo presión de cronograma.
Rastrear Tubos pero No Rastrear Componentes Mojados Pequeños
El eslabón más débil de trazabilidad a menudo aparece en accesorios, sellos, diafragmas o ensamblajes locales de muestras.
Mantener Datos de Soldadura Separados de la Lógica de Liberación a Nivel de Línea
Los registros de soldadura son mucho menos útiles si no se asignan claramente al circuito instalado final y su estado de liberación.
Permitir que las Marcas Rojas se Alejen de la Realidad Instalada
Cuando los cambios en campo avanzan más rápido que las actualizaciones controladas, el paquete de entrega se vuelve más difícil de confiar.
Suponiendo que QA lo aceptará más tarde
En tuberías GMP, la falta de evidencia rara vez es más fácil de corregir al final del proyecto que durante la ejecución controlada.
Recopilación excesiva de documentos pero definición insuficiente de lo que realmente importa
Los grandes volúmenes de documentos no crean automáticamente un paquete de entrega sólido. Lo que importa es si el conjunto de registros demuestra el sistema higiénico instalado con suficiente claridad para la liberación y el control posterior del ciclo de vida.
Lista de verificación práctica: qué preguntar antes de liberar un sistema de tuberías farmacéutico
Antes de que comience la fabricación
- ¿Qué componentes mojados deben ser rastreables?
- ¿Qué registros deben crearse durante la fabricación?
- ¿Qué evidencia de soldadura, acabado e inspección requerirá QA más tarde?
- ¿Cómo se incorporarán los cambios en el campo a los registros controlados?
Antes de la Finalización Mecánica
- ¿Están actualizadas las líneas rojas?
- ¿Los componentes instalados se corresponden claramente con los registros de materiales aprobados?
- ¿Están cerrados el estado de las soldaduras y el historial de reparaciones?
- ¿Están completos los registros de acabado y tratamiento donde se requieren?
Antes de la Liberación de Control de Calidad
- ¿Coincide el paquete de entrega con el circuito instalado real?
- ¿Hay algún ensamblaje local aún sin resolver en trazabilidad o registros de inspección?
- ¿Puede el proyecto demostrar la condición final tal como se construyó con suficiente claridad para la liberación?
Después del Arranque
- ¿Cómo continuarán los registros de equipos y mantenimiento?
- ¿Cómo se mantendrá la trazabilidad de las piezas de repuesto?
- ¿Cómo se vincularán los cambios futuros con la cadena de evidencia original?
| Etapa del Proyecto | Pregunta Clave de Documentación | Cómo se ve un Buen Control |
|---|---|---|
| Antes de la Solicitud de Cotización (RFQ) | ¿Qué debe ser trazable y entregable? | El conjunto de registros está definido, no asumido |
| Durante la fabricación | ¿Se están creando registros en tiempo real? | Los registros de soldadura, material, acabado y cambios se mantienen actualizados |
| Antes de la entrega | ¿Coincide el dossier con la realidad instalada? | El as-built, la trazabilidad y el cierre de inspección se alinean |
| Después del arranque | ¿Sobrevivirá la cadena de evidencia a los cambios del ciclo de vida? | Los registros de mantenimiento y reemplazo continúan bajo control |
Conclusión: En Tuberías Farmacéuticas, la Documentación Prueba que el Sistema que Crees que Construiste es el Sistema que Realmente Instalaste
La buena documentación y trazabilidad no añaden valor después del proyecto. Protegen el proyecto de volverse irrealizable en el momento exacto en que debería estar listo para funcionar. En tuberías farmacéuticas, el sistema instalado solo es tan aceptable como la cadena de evidencia que demuestra que su material, fabricación, acabado, inspección y cambios fueron controlados.
Los proyectos más sólidos no intentan reconstruir esta cadena de evidencia en la entrega. La definen antes de la solicitud de cotización, la mantienen durante la fabricación y la cierran antes de la liberación. Para el grupo completo de temas farmacéuticos, conecte este artículo con Selección de Material de Tuberías Higiénicas Farmacéuticas, Acero Inoxidable 316L Electropulido vs 316L Estándar, Selección de Conexiones de Grado Alimentario para Instalaciones GMPy Consideraciones de Diseño de CIP para Tubería Higiénica.
PREGUNTAS FRECUENTES
¿Qué documentación se requiere para proyectos de tuberías farmacéuticas?
El paquete exacto depende del alcance del proyecto, pero generalmente incluye certificados de material, registros de trazabilidad, documentación de soldadura, registros de inspección, evidencia de acabado o tratamiento donde se requiera, modificaciones en rojo, as-built y registros de entrega que respaldan la liberación de control de calidad.
¿Qué trazabilidad se requiere en tuberías de GMP?
La trazabilidad debe seguir la ruta húmeda. Eso a menudo significa que los tubos, accesorios, válvulas, ensamblajes locales y otros componentes críticos en contacto con el producto deben ser trazables hasta registros aprobados de una manera que aún coincida con la condición instalada.
¿Por qué fallan los proyectos de tuberías farmacéuticas en la entrega?
A menudo fallan porque la cadena de evidencia está incompleta. La instalación puede ser físicamente aceptable, pero los registros faltantes o débiles de material, soldadura, acabado o as-built aún pueden retrasar la liberación de control de calidad.
¿Los accesorios y juntas necesitan trazabilidad en proyectos de GMP?
En muchas aplicaciones higiénicas críticas, sí. Los componentes húmedos más pequeños son a menudo donde aparece el eslabón de documentación más débil, por lo que no deben tratarse como consumibles casuales si influyen en el rendimiento higiénico o el riesgo de liberación.
¿Se requieren registros de soldadura para tuberías higiénicas de grado farmacéutico?
Los proyectos comúnmente dependen de mapas de soldadura y documentación de soldadura porque son centrales para demostrar el estado de fabricación e inspección. El formato exacto varía según el proyecto, pero la documentación deficiente de soldaduras es uno de los problemas de entrega más comunes.
¿Cuál es la diferencia entre los registros de construcción final y los documentos de entrega?
Los registros como-construido muestran la configuración final instalada. Los documentos de entrega son el paquete de evidencia más amplio utilizado para respaldar la liberación, incluyendo trazabilidad, inspección, pruebas y registros relacionados del proyecto.




