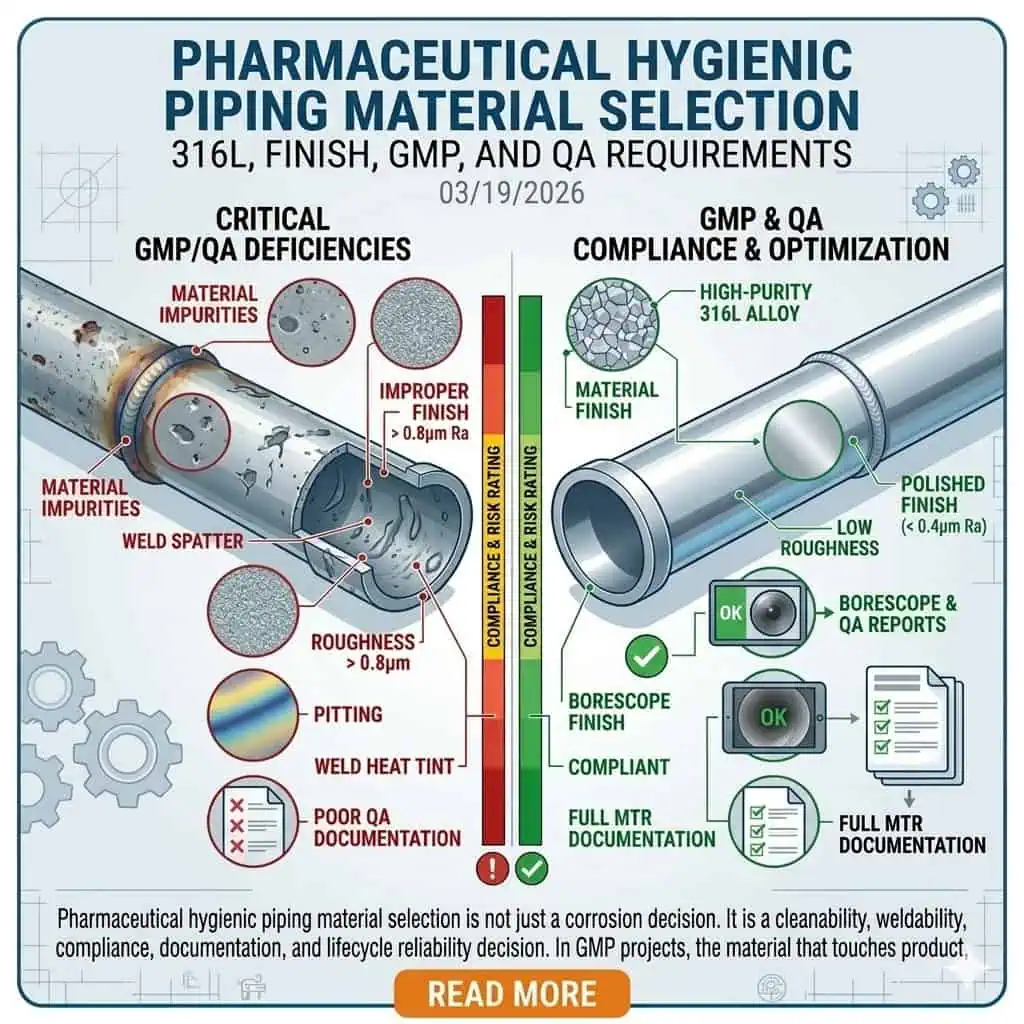
La selección de materiales para tuberías higiénicas farmacéuticas no es solo una decisión sobre corrosión. Es una decisión sobre limpiabilidad, soldabilidad, cumplimiento, documentación y confiabilidad del ciclo de vida. En proyectos GMP, el material que toca el producto, fluidos de proceso, agua de alta pureza o medios de limpieza debe hacer más que “resistir la oxidación”. Debe permanecer no reactivo, no aditivo, no absorbente, limpiable, inspeccionable y soportar fabricación repetible y liberación de control de calidad. Por eso, los ingenieros experimentados no seleccionan tubos y accesorios solo por el nombre de la aleación.
En la mayoría de los sistemas de tuberías higiénicas farmacéuticas, el acero inoxidable 316L es la línea base práctica para servicio crítico de contacto con productos metálicos porque equilibra margen de corrosión, soldabilidad, aceptación de la industria y compatibilidad con prácticas de fabricación de alta pureza. Esto no significa que cada línea, cada accesorio o cada ensamblaje deba manejarse de la misma manera. La decisión correcta depende de la química real del proceso, régimen de CIP/SIP, requisito de acabado superficial, densidad de soldadura, sensibilidad a la contaminación y el paquete de documentación requerido para la entrega y validación.
Esta guía explica cómo los ingenieros seleccionan materiales para tuberías higiénicas farmacéuticas, donde el 316L tiene sentido claro, donde el 316L estándar puede no ser suficiente sin el acabado y calidad de soldadura adecuados, y donde la documentación y trazabilidad se vuelven tan importantes como el metal mismo. En revisiones reales de proyectos, la decisión final de material rara vez se cambia por una gran falla. Generalmente se cambia por un patrón de problemas menores: una soldadura más difícil de inspeccionar de lo esperado, un registro de acabado que no cierra limpiamente con control de calidad, una rama de muestra que experimenta ciclos SIP más severos que el resto del circuito, o un ensamblaje local que se comporta como una zona de mayor riesgo de lo que sugería el P&ID.
Lo que realmente significa la selección de materiales para tuberías higiénicas farmacéuticas
La elección de material es una decisión de GMP y control de contaminación
En sistemas farmacéuticos, la selección de materiales es parte del control de contaminación. Una tubería, cuerpo de válvula, férula o accesorio no se acepta porque parezca de grado alimentario. Se acepta porque la superficie en contacto con el producto puede soportar el proceso previsto sin alterar la seguridad, identidad, resistencia, calidad o pureza. Ese principio se alinea con FDA 21 CFR 211.65, que requiere que las superficies en contacto con el producto sean no reactivas, no aditivas y no absorbentes.
En la práctica, eso significa que los ingenieros revisan la elección del material junto con el acabado superficial, el estado de la soldadura, la capacidad de drenaje, la pasivación, la química de limpieza y la accesibilidad para inspección. Una aleación correcta con una purga de soldadura deficiente, una condición superficial no controlada o una documentación débil aún puede convertirse en un problema de GMP. Una lección común en campo es que un paquete de tuberías puede parecer técnicamente aceptable en la liberación de fabricación y aún así volverse difícil durante la calificación porque la decisión del material se trató como un artículo de compra en lugar de una decisión de control de contaminación.
Nota de ingeniería: en trabajos de GMP, la pregunta no es solo “¿Sobrevivirá esta aleación?” sino también “¿Se comportará esta superficie terminada, soldada y documentada de manera predecible en inspección, limpieza y liberación de QA?”
Por qué la selección de tuberías farmacéuticas es diferente del servicio higiénico general
La tubería higiénica farmacéutica generalmente se mantiene a un estándar más estricto que el servicio higiénico general de alimentos o servicios. La razón no es solo el valor del producto. Es la consecuencia de la contaminación, la retención de residuos, las sustituciones no documentadas, la fabricación inconsistente y la liberación de QA retrasada en entornos validados. El mismo grado de acero inoxidable puede ser aceptable en una aplicación higiénica general pero aún así quedarse corto en un sistema GMP si la consistencia del acabado, los registros de soldadura o la trazabilidad no se controlan al nivel que requiere el proyecto.
Por eso, la revisión de materiales en proyectos farmacéuticos debe estar junto a la selección de conexiones, el control de tramos muertos, la aceptación de soldaduras y la planificación de entrega de QA. Una aleación correcta en el ensamblaje equivocado sigue siendo el resultado de ingeniería incorrecto.
Qué estándares realmente impulsan la decisión
Los estándares más útiles son los que cambian lo que especificas, inspeccionas y aceptas. En tuberías higiénicas farmacéuticas, las referencias más relevantes suelen incluir:
- ASME BPE para materiales, diseño, fabricación, inspección, pruebas y lógica de certificación en equipos de bioprocesamiento y farmacéuticos.
- FDA 21 CFR 211.65 para construcción de equipos e idoneidad de superficies en contacto con productos.
- FDA 21 CFR 211.67 para expectativas de limpieza y mantenimiento.
- ASTM A270/A270M para tubería de grado alimentario, incluyendo la opción de especificar calidad farmacéutica como requisito suplementario.
- Anexo 1 de la GMP de la UE para control de contaminación, gestión de riesgos de calidad y expectativas de fabricación estéril.
El trabajo del ingeniero es convertir esos requisitos en decisiones reales de material, acabado, soldadura y documentación que puedan sobrevivir a la adquisición, fabricación, inspección, puesta en marcha y revisión de QA. En proyectos sólidos, los estándares no se citan al final para justificar una elección terminada. Se traducen al principio en lenguaje de RFQ, criterios de inspección, requisitos de entrega y límites de control de cambios.
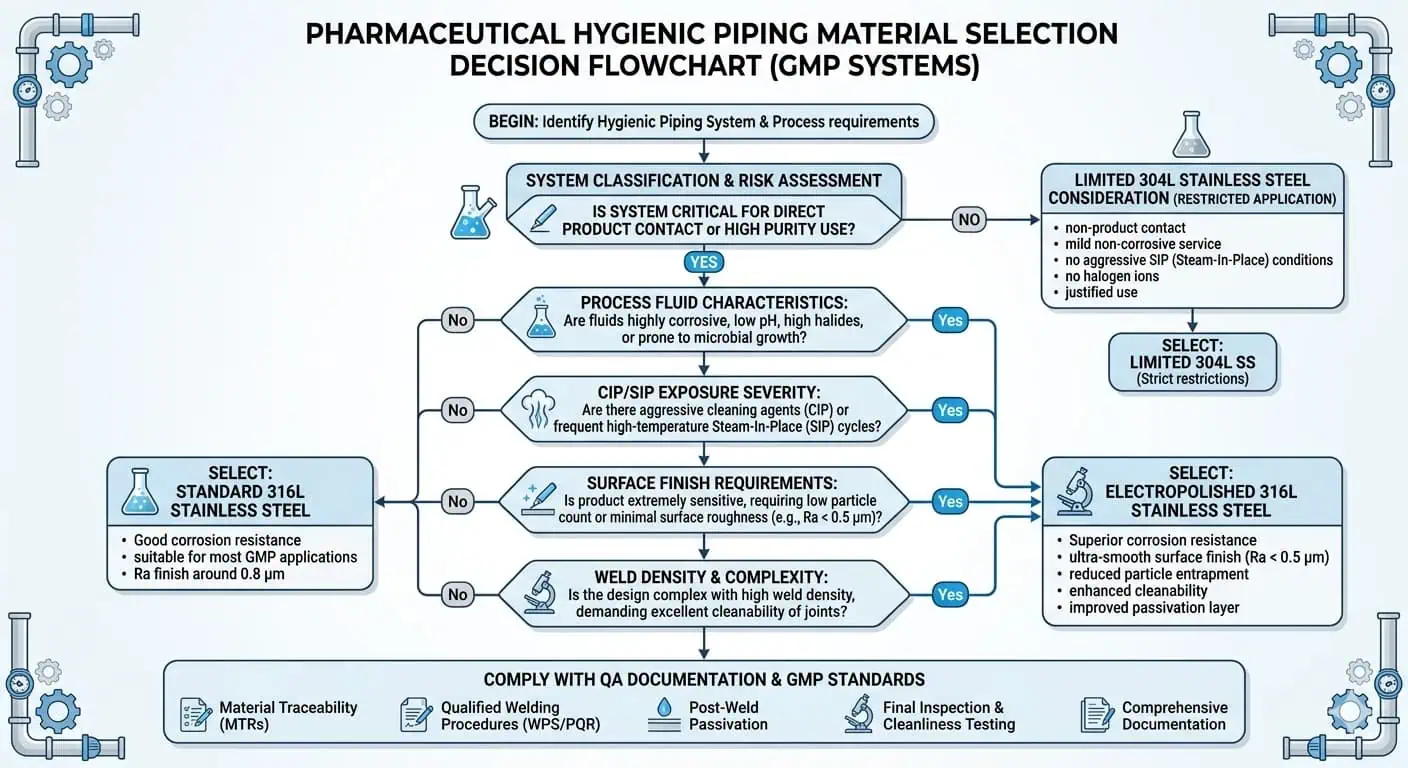
Las Familias de Materiales Principales Utilizadas en Tuberías Higiénicas Farmacéuticas
¿Por qué el 316L es la base práctica para muchos sistemas higiénicos GMP?
El 316L se trata comúnmente como el material metálico de base para tuberías higiénicas farmacéuticas críticas porque ofrece una combinación práctica de resistencia a la corrosión, soldabilidad y amplia aceptación en la industria. El grado bajo en carbono soporta la fabricación higiénica soldada de manera más confiable que el 316 estándar en muchas condiciones de proceso, y la química con molibdeno mejora la resistencia a la corrosión localizada en comparación con el 304/304L en entornos de limpieza y servicio más exigentes.
Eso no convierte al 316L en una solución mágica. Significa que el 316L es a menudo el punto de partida más defendible para tuberías metálicas en contacto con productos cuando el sistema también debe respaldar expectativas de fabricación de alta pureza y documentación. En proyectos reales, los ingenieros a menudo eligen el 316L no porque cada sección del sistema sea químicamente severa, sino porque el riesgo total del proyecto recae en los ensamblajes soldados, la limpiabilidad local, la exposición a SIP/CIP y las expectativas de validación en conjunto.
Cuándo el 304/304L aún puede aparecer—y por qué a menudo está limitado
El 304 o 304L aún puede aparecer en algunos proyectos farmacéuticos, pero generalmente en roles más limitados. Servicios auxiliares de menor riesgo, sistemas heredados, áreas de soporte no críticas o diseños históricos impulsados por costos aún pueden usar materiales de la familia 304. Pero en tuberías higiénicas críticas en contacto con productos, la industria generalmente se inclina hacia el 316L porque el riesgo total es más amplio que solo la corrosión masiva.
Este es uno de los errores de especificación más comunes en proyectos en etapas tempranas: tratar el 304 frente al 316L como una simple elección de precio en lugar de una elección de limpiabilidad, fabricación y riesgo de control de calidad. En la práctica, cuando un equipo pregunta si aún se puede usar el 304L, la mejor pregunta de seguimiento suele ser: ¿usado dónde, bajo qué régimen de limpieza, con qué requisito de acabado y bajo qué estándar de documentación?
Dónde aún importan los materiales no metálicos
La selección de materiales para tuberías farmacéuticas no se detiene en la pared del tubo. Los diafragmas, asientos de válvulas, juntas, mangueras y otras partes húmedas no metálicas a menudo determinan si el ensamblaje final funciona según lo previsto. PTFE, PTFE modificado, EPDM, FKM, silicona o compuestos específicos de la aplicación pueden estar involucrados dependiendo de la química, temperatura, exposición SIP y requisitos de validación.
En muchas desviaciones de GMP, el punto débil no es la tubería de acero inoxidable. Es el material de interfaz que se trató como un consumible menor en lugar de un componente húmedo controlado. Un ejemplo común es un sistema metálico químicamente compatible emparejado con un material de sellado que envejece más rápido bajo SIP repetido de lo que asumió la revisión de riesgo original. La lección no es que la selección del metal estuviera equivocada de forma aislada; es que el sistema húmedo no se revisó en su conjunto.
Cómo los ingenieros deciden entre 316L estándar, 316L electropulido y opciones de mayor especificación
316L estándar vs 316L electropulido
316L estándar y 316L electropulido no son familias de aleaciones competidoras. Son diferentes decisiones de condición de superficie construidas sobre la misma familia de material base. 316L estándar puede ser totalmente aceptable donde los requisitos de acabado, limpiabilidad y expectativas de inspección son moderados. 316L electropulido se vuelve más atractivo donde los requisitos de consistencia superficial, comportamiento de liberación de residuos, inspeccionabilidad y limpiabilidad de alta pureza son más estrictos.
La mejor pregunta no es “¿Es mejor el electropulido?” sino “¿Necesita este proceso las ventajas relacionadas con el acabado lo suficientemente como para justificar el requisito más estricto?” En revisiones de ingeniería reales, el electropulido a menudo se selecciona no porque el 316L estándar fallara en todas partes, sino porque el proceso exigía una superficie más controlada para confianza en la inspección, respuesta a residuos o disciplina operativa de alta pureza. Para la discusión detallada del acabado, conecte este artículo con Acero Inoxidable 316L Electropulido vs 316L Estándar.
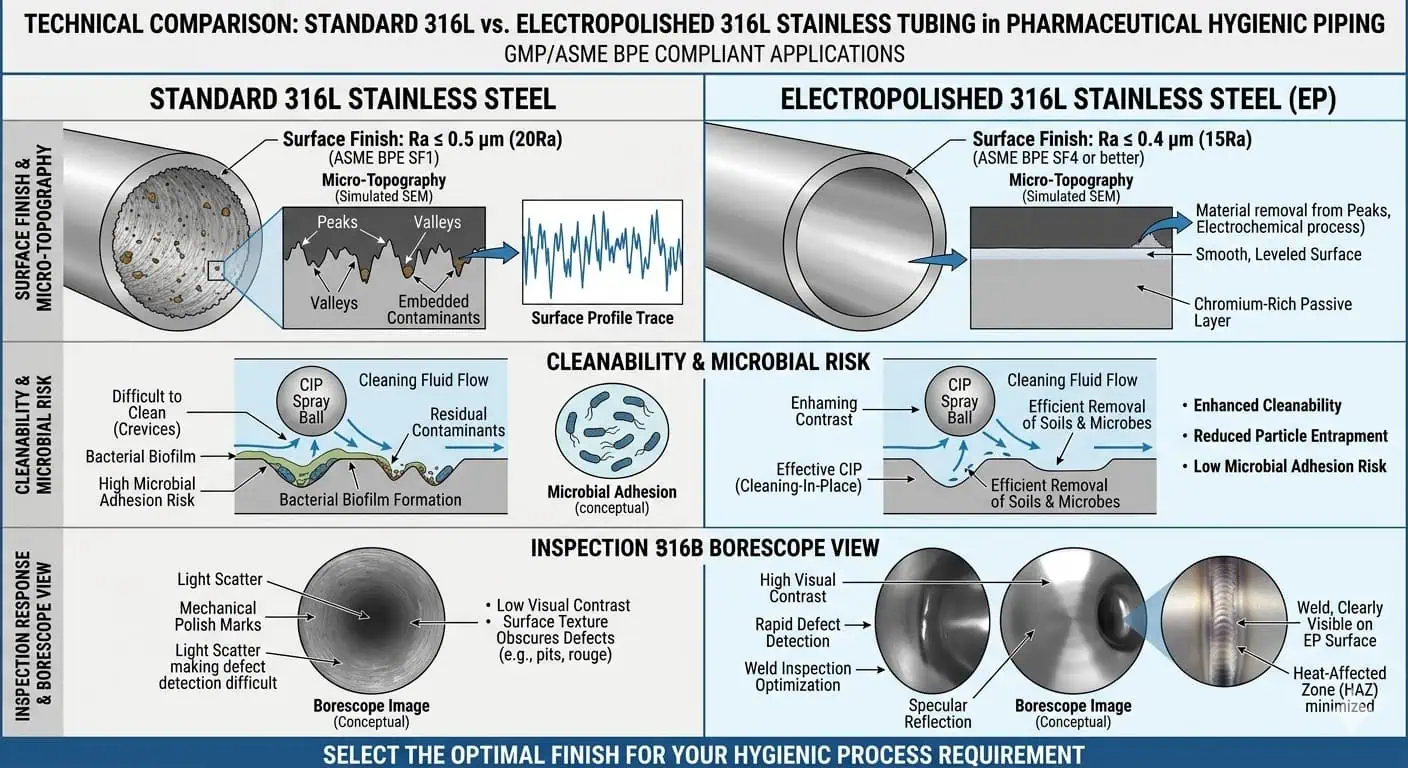
Cuando el acabado superficial cambia el rendimiento higiénico real
El acabado superficial no es una mejora cosmética en servicio farmacéutico. Cambia la limpiabilidad, la respuesta a la inspección y el comportamiento de retención de residuos. Un requisito de acabado importa más donde el proceso es sensible a los residuos, donde la repetibilidad de SIP/CIP es crítica, donde la inspección de contacto con el producto es estricta, o donde la geometría local hace que cualquier defecto superficial sea más consecuencial.
En entornos de alta pureza y biofarmacéuticos, los ingenieros no separan la selección de aleación de la selección de acabado porque el resultado higiénico se crea por ambas juntas. Una lección repetida de las investigaciones de campo es que un sistema puede usar la aleación correcta y aún tener un rendimiento inferior si la condición de acabado local varía más de lo que el modelo de riesgo permitió.
Cuando una revisión de aleación superior o material especial está justificada
A veces 316L aún no es suficiente, pero esa decisión debe provenir de la química y el mecanismo de falla, no del hábito. La exposición más agresiva a haluros, sistemas de solventes inusuales, química de proceso fuerte o historial de fallas repetidas pueden justificar una revisión de aleación superior. Ese paso debe basarse en datos reales de servicio, revisión del mecanismo de corrosión y química de proceso, no en una suposición genérica de que “la farmacéutica siempre usa el grado más alto disponible”.”
El consejo experto aquí es directo: no escale la aleación porque el sistema es “importante”. Escálela solo cuando pueda definir el modo de falla que está tratando de prevenir y la razón por la cual la opción de referencia no proporciona suficiente margen.
Selección de material por área de proceso en instalaciones farmacéuticas
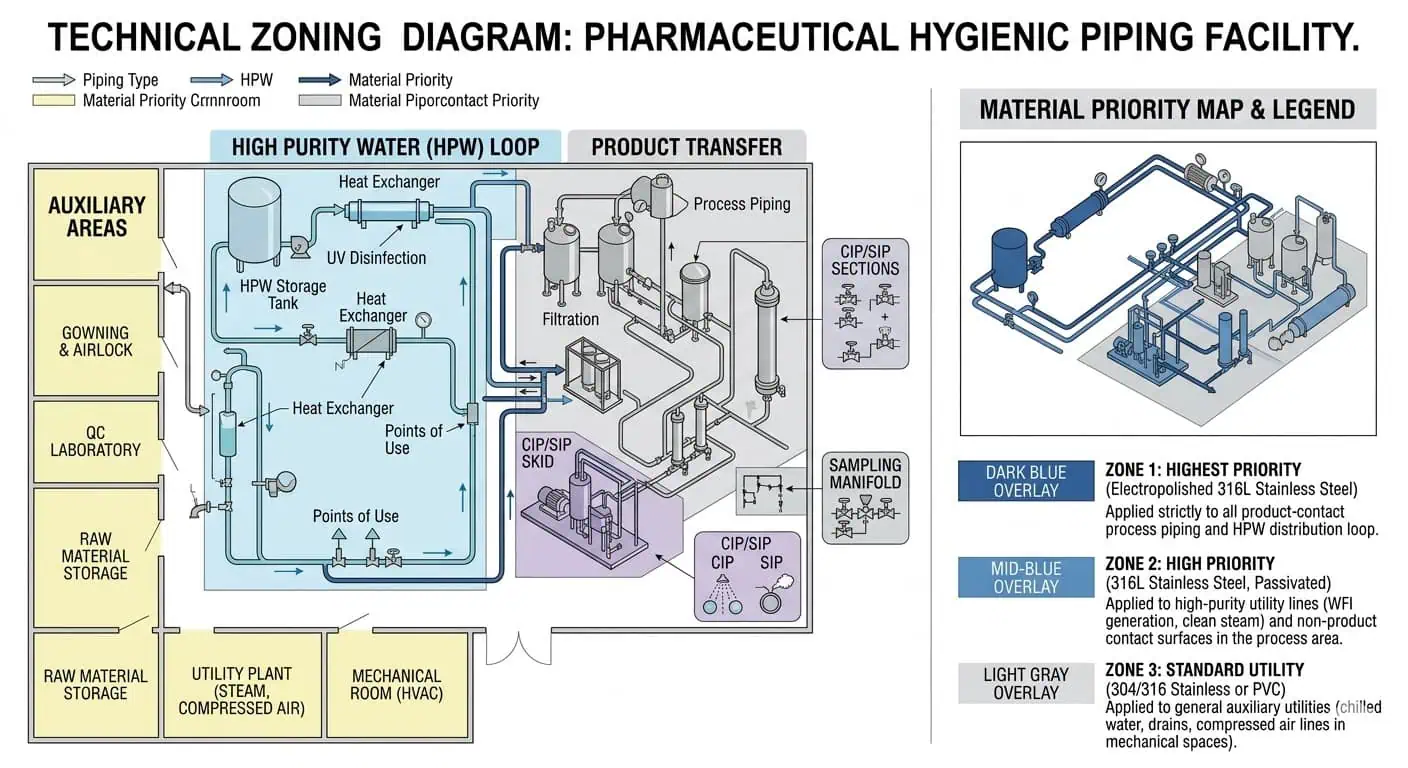
Sistemas relacionados con agua de alta pureza y utilidades limpias
Los circuitos de agua de alta pureza y los circuitos de servicios limpios relacionados ejercen presión sobre la consistencia del material, la calidad de la soldadura y la estabilidad superficial a largo plazo. En estos sistemas, la decisión del material está estrechamente ligada a la tendencia a la oxidación roja, la consistencia del acabado, la aceptación de la soldadura y la compatibilidad con la sanitización. Las especificaciones más sólidas suelen centrarse menos en el nombre de la aleación por sí solo y más en si el paquete completo de tubería y soldadura puede soportar un rendimiento higiénico estable y repetible a lo largo del tiempo.
Nota de ingeniería típica: En los circuitos de agua de alta pureza, la primera preocupación a menudo no es la corrosión masiva de la pared. Es la inconsistencia local del acabado, el estado de la soldadura o la restauración incompleta de la superficie en contacto con el producto después de la fabricación y el reprocesamiento. Por eso, los ingenieros que han visto investigaciones repetidas de circuitos tienden a centrarse tempranamente en la ejecución de la soldadura y la evidencia del acabado, no solo en la designación de la aleación.
Líneas de Proceso en Contacto con el Producto y Ensambles de Transferencia
Las líneas de proceso en contacto con el producto suelen justificar el pensamiento de material más conservador. Aquí es donde la corrosión, el cambio superficial, la preocupación por los extractables o la inconsistencia en la fabricación pueden tener el efecto más directo en la calidad del producto y la confianza del lote. El grado del material, el acabado, las interfaces de los accesorios y el paquete de documentación deben definirse todos antes de la solicitud de cotización, no aclararse después de la fabricación.
En términos de proyecto, aquí es donde “aceptable para uso higiénico general” y “aceptable para uso validado en contacto con el producto” se separan más claramente. La penalización por una aclaración tardía a menudo no es solo el reprocesamiento técnico, sino la demora en la prueba de aceptación en fábrica, la prueba de aceptación en sitio o el cierre de control de calidad.
Secciones Expuestas a CIP/SIP
Las secciones expuestas a CIP/SIP a menudo revelan la debilidad del material más rápido que el proceso en sí. Los ciclos repetidos de agua caliente, vapor limpio, sosa cáustica, ácido, desinfectante y enfriamiento cambian significativamente el entorno de servicio. En la práctica, muchos problemas relacionados con los materiales en tuberías farmacéuticas no se revelan primero por el producto; se revelan por los ciclos repetidos de limpieza y esterilización.
Esta es una razón por la que un ingeniero debe revisar los materiales mojados metálicos y no metálicos juntos siempre que el sistema experimente un servicio repetido de SIP/CIP. Un patrón común en campo es que la tubería permanece aceptable mientras que un sello local, asiento o ensamblaje de ramal envejece más rápido de lo esperado bajo el ciclo térmico y químico real.
Muestreo, Colectores de Válvulas y Otros Ensamblajes Locales de Alto Riesgo
Las decisiones de materiales más difíciles a menudo están en los ensamblajes locales, no en tramos rectos de tubería. Las válvulas de muestreo, colectores de distribución, conexiones de ramal, válvulas de diafragma y tes de instrumentación combinan una mayor densidad de soldadura, más interfaces, más riesgo de tramos muertos y más sensibilidad de inspección. Aquí es donde el paquete higiénico total importa más.
Es por eso que este artículo debe conectarse directamente con Selección de Conexiones de Grado Alimentario para Instalaciones GMP. En farmacéutica, la aleación correcta en el ensamblaje incorrecto sigue siendo el resultado incorrecto. Los ingenieros que solucionan problemas en estos sistemas regularmente saben que la línea rara vez falla “en todas partes”. Falla primero en el detalle local que se trató como normal cuando en realidad era el punto de mayor riesgo en el circuito.
Soldabilidad, Condición de la Superficie y Tratamiento Post-Fabricación
Por Qué la Densidad de Soldadura Cambia el Riesgo del Material
Cuantas más soldaduras contiene un sistema higiénico, menos útil es hablar sobre la elección del material como si solo importara el tubo base. Las zonas afectadas por el calor de la soldadura, la calidad de la purga, la condición del cordón interno, la consistencia de la soldadura orbital y el historial de retrabajo influyen en si el sistema final se comporta como un activo GMP limpiable o como una fuente recurrente de desviaciones.
Un sistema con una excelente elección de aleación pero una ejecución deficiente de la soldadura sigue siendo un sistema farmacéutico débil. En términos prácticos, cada soldadura añadida aumenta la importancia de la disciplina de fabricación, no solo la importancia del certificado de aleación.
Por qué los defectos superficiales pueden anular una buena elección de material
Una aleación correcta no rescata una superficie de contacto con el producto deficiente. Las irregularidades superficiales, la decoloración de la soldadura, el contorno deficiente, los arañazos, la contaminación por manipulación durante la fabricación o el retrabajo no controlado pueden reducir el valor higiénico de una buena selección de material. Aquí es donde los ingenieros suelen ver la primera brecha entre la intención de la especificación y la realidad instalada.
Caso típico de la industria: El proyecto especificó correctamente 316L para un circuito crítico de contacto con el producto, pero el paquete de entrega aún generó preocupación porque la apariencia local de la soldadura, la consistencia del acabado y la revisión con boroscopio no respaldaban el estándar higiénico declarado. La aleación no era el problema. La condición superficial fabricada sí lo era.
Ese caso es lo suficientemente común como para importar. Es una razón por la que los revisores experimentados no aprueban mentalmente un circuito solo porque el certificado de prueba de material parezca correcto.
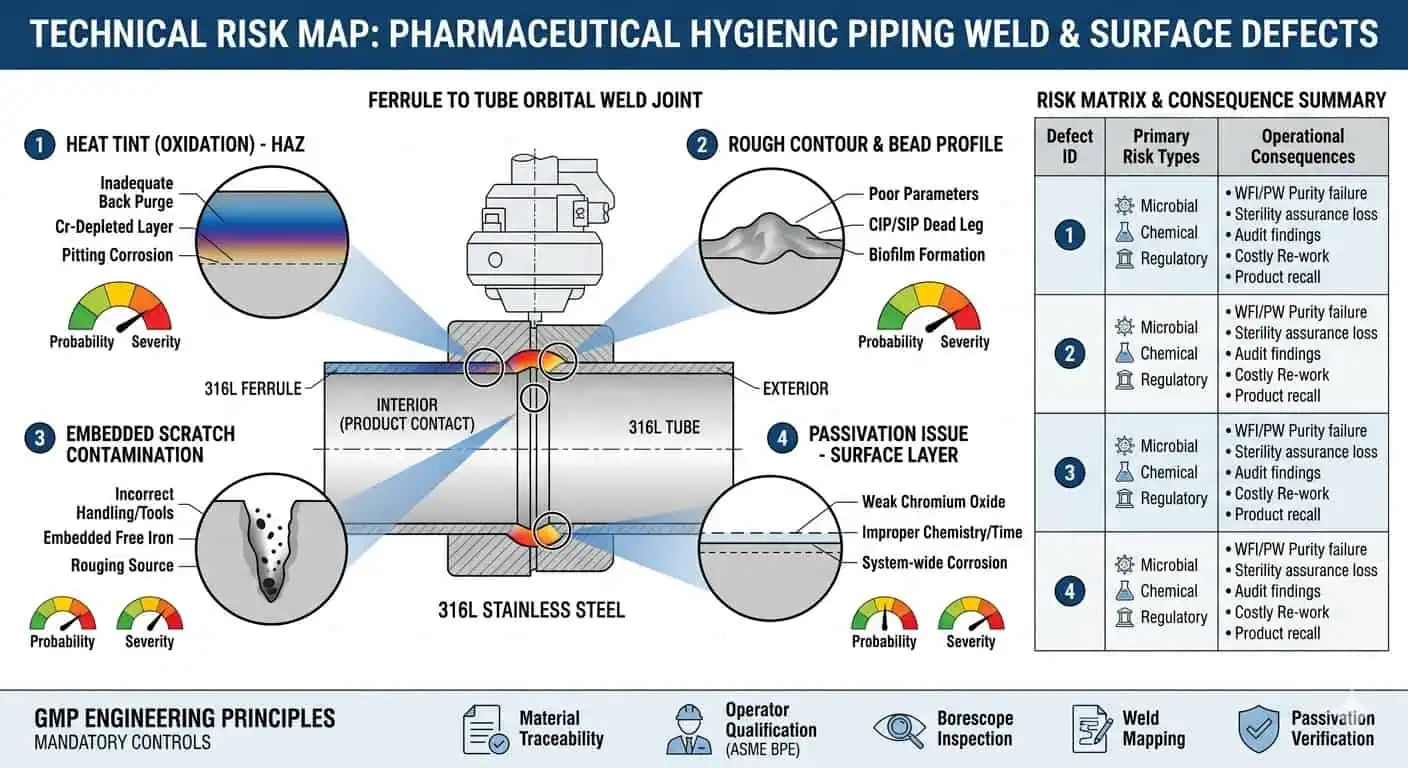
Pasivación, compatibilidad de limpieza y estabilidad a largo plazo
La pasivación y el tratamiento posterior a la fabricación son parte de la estrategia de material, no un acabado opcional. Un material que es correcto en papel pero con un acabado deficiente, mal limpiado después de la fabricación o restaurado inadecuadamente tras trabajos de soldadura no funcionará como se pretendía que lo hiciera el material especificado. Esto importa aún más en sistemas con limpieza repetida, sanitización y escrutinio de validación.
El consejo experto aquí es simple: nunca trates la condición superficial post-fabricación como un elemento de cierre cosmético. En servicio higiénico farmacéutico, es parte del rendimiento técnico de la decisión del material en sí.
Documentación y Trazabilidad: Por Qué la Selección de Materiales También es una Decisión de Control de Calidad
Lo que el Control de Calidad Suele Querer Ver
En proyectos de tuberías GMP, el material correcto es solo la mitad de la respuesta. El Control de Calidad suele necesitar pruebas. Dependiendo del alcance del proyecto, eso puede incluir números de colada, certificados de prueba de materiales, certificados EN 10204 3.1, registros de PMI donde se requiera, registros de acabado superficial, mapas de soldadura, registros de soldadura, registros de inspección y documentación de entrega que vincule el ensamblaje instalado con la especificación aprobada.
El paquete exacto varía según el proyecto, pero el patrón es consistente: si la elección del material no puede rastrearse y verificarse, sigue siendo un riesgo para el proyecto. Aquí es donde muchos paquetes técnicamente capaces pierden tiempo durante la entrega: no porque la metalurgia fuera incorrecta, sino porque la cadena de evidencia era más delgada de lo que requería el entorno GMP.
Por Qué “Material Correcto” Sin Registros Sigue Siendo un Riesgo para el Proyecto
Uno de los fracasos más comunes en proyectos farmacéuticos no es la selección incorrecta de aleación. Es el cierre incompleto de la cadena de evidencia. La tubería puede ser correcta. Los accesorios pueden ser correctos. Las soldaduras pueden incluso ser aceptables. Pero si la trazabilidad, los registros de acabado o la documentación de inspección están incompletos, la liberación del Control de Calidad aún puede estancarse.
Caso típico de la industria: Un paquete de tubería GMP aprobó la revisión de fabricación pero falló en la preparación para entrega porque los registros de trazabilidad térmica y acabado para un grupo de piezas de tubería higiénica estaban incompletos. El problema no fue metalurgia técnica. Fue control de documentación.
Por eso los ingenieros experimentados tratan la documentación como parte de la selección de materiales desde el principio, no como un ejercicio de papeleo para el final del proyecto.
Cómo Definir Requisitos de Materiales Antes de la Solicitud de Cotización
El mejor momento para definir las expectativas de materiales es antes de la Solicitud de Cotización, no durante la revisión de la lista de pendientes. Una Solicitud de Cotización sólida generalmente define el grado de aleación, estándar de tubería, objetivo de acabado, requisitos de soldadura, expectativas de pasivación, entregables de documentación y cualquier requisito de inspección específico para la aceptación.
Para el lado completo de Control de Calidad de ese tema, conecte este artículo con Documentación y Trazabilidad en Proyectos de Tubería Farmacéutica.
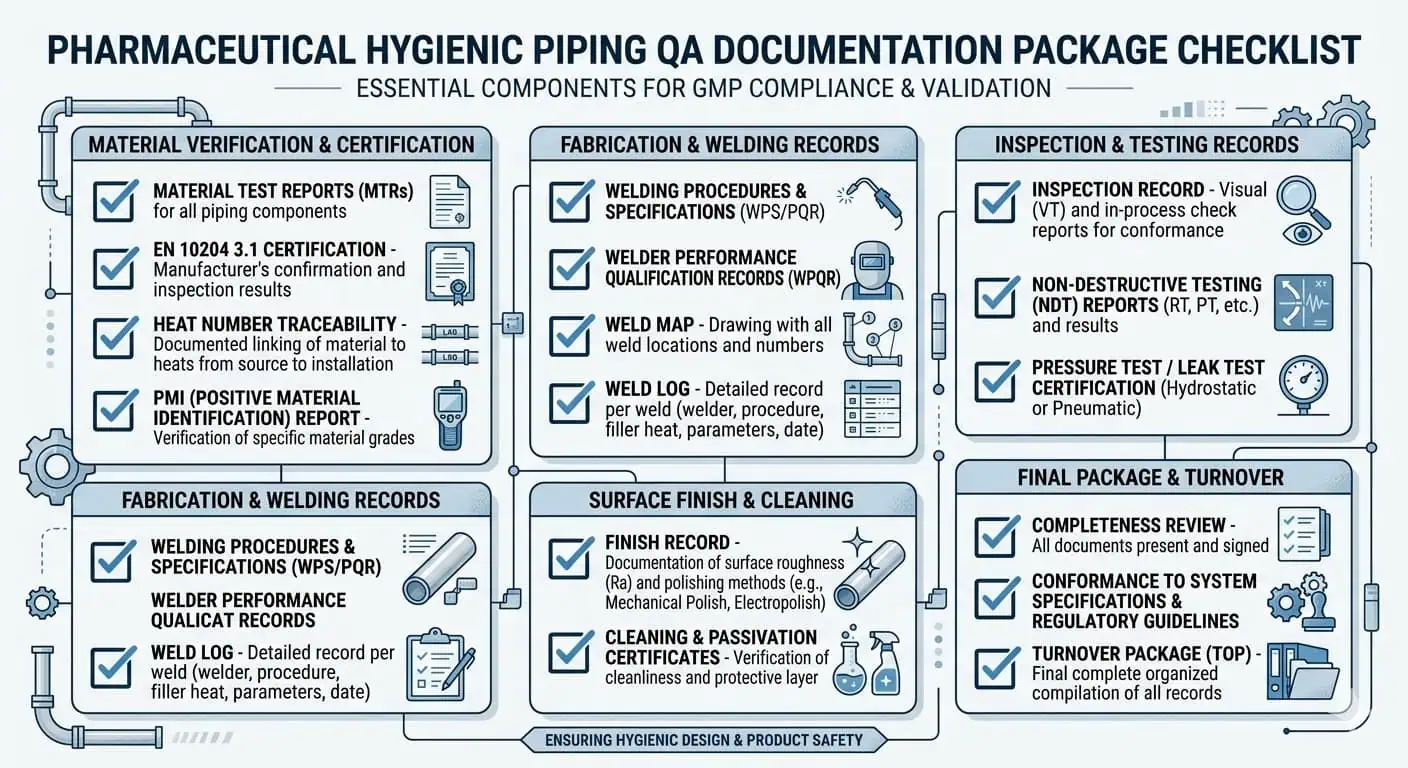
Ejemplos de investigación, casos de la industria y consejos de expertos
Caso de Ingeniería Típico 1: 316L Era Correcto, pero la Zona de Soldadura Falló en la Intención Higiénica
Este es uno de los fallos de tubería farmacéutica más realistas. El equipo de diseño eligió la familia de aleación correcta, pero la zona de soldadura instalada no preservó la intención higiénica de la elección del material. La preocupación resultante puede manifestarse como inconsistencia de acabado, fallo de inspección, respuesta de limpieza difícil o vacilación de Control de Calidad sobre la calidad local de contacto con el producto.
La lección es directa: en la industria farmacéutica, la selección de materiales y la ejecución de la soldadura no pueden separarse. Los sistemas más fuertes no son aquellos con la descripción de material más costosa. Son aquellos donde el material, el acabado, la fabricación y la lógica de inspección apoyan el mismo objetivo higiénico.
Caso de Ingeniería Típico 2: El Problema de QA Fue la Documentación, No la Aleación
Otro modo de falla común aparece durante la entrega. El proyecto utilizó el grado de material correcto, pero el paquete carecía de los registros necesarios para demostrar el cumplimiento. Certificados faltantes, trazabilidad poco clara, registros de acabado incompletos o documentación de soldadura débil pueden retrasar la aprobación incluso cuando el metal instalado es técnicamente correcto.
Por eso los ingenieros experimentados tratan la documentación como parte de la selección de materiales desde el principio. En el trabajo práctico de GMP, una elección correcta no documentada sigue siendo una elección incompleta.
Caso de Ingeniería Típico 3: Se Necesitaba Electropulido por Limpiabilidad, No Porque el 316L Estuviera “Equivocado”
A veces el 316L estándar no se rechaza porque la aleación sea inadecuada, sino porque el requisito de acabado cambió el objetivo higiénico. En esos casos, la mejor respuesta no es decir que el proyecto eligió la familia de metal equivocada. La mejor respuesta es que el proyecto eventualmente reconoció un requisito de limpiabilidad e inspeccionabilidad más estricto que el que la especificación de acabado original apoyaba.
Ese es un refinamiento de ingeniería normal, no una vergüenza. Es exactamente cómo un equipo de proceso fuerte mejora la precisión de la especificación con el tiempo.
Consejo de Experto: Pregunte Qué Falla Está Intentando Prevenir Realmente
La mejor pregunta para la selección de materiales no es “¿Qué grado usa la mayoría de la gente?” Es “¿Qué falla estamos tratando de prevenir en este sistema específico?” La respuesta puede ser corrosión. Puede ser riesgo de oxidación rojiza. Puede ser preocupación por extractables. Puede ser limpieza impulsada por el acabado. Puede ser inconsistencia en la soldadura. Puede ser falla de cierre en el control de calidad. Una vez que ese modo de falla está claro, la decisión sobre el material se vuelve mucho más racional.
Ese es el consejo más consistente de los ingenieros que han trabajado con desviaciones reales en tuberías farmacéuticas: defina primero el modo de falla, y la lógica del material se vuelve más clara, más estrecha y más fácil de defender.
Errores Comunes en la Selección de Materiales para Tuberías Higiénicas Farmacéuticas
Elegir Solo por el Nombre de la Aleación
La familia de aleaciones importa, pero el resultado higiénico instalado depende también del acabado, las soldaduras, la geometría, las interfaces y la documentación.
Separar el Grado del Acabado Superficial
El 316L estándar y el 316L electropulido no son intercambiables si el objetivo higiénico está definido por las expectativas de limpieza e inspección relacionadas con el acabado.
Ignorar la Soldabilidad y la Realidad de la Fabricación
Un material base correcto con una ejecución de soldadura deficiente sigue siendo un paquete de tuberías débil para GMP.
Tratar la documentación como un problema posterior a la adquisición
En proyectos farmacéuticos, la documentación es parte de la aceptación, no una idea tardía para la entrega.
Usar una única regla de material para cada área de proceso
Los circuitos de agua de alta pureza, las transferencias en contacto con el producto, las secciones expuestas a CIP/SIP y las áreas auxiliares no tienen todas la misma consecuencia higiénica o de cumplimiento.
Lista de verificación práctica para la selección de materiales de tuberías higiénicas farmacéuticas
Preguntas para responder antes de la aprobación final del material
- ¿Qué fluido de proceso o producto entra realmente en contacto con la superficie?
- ¿Qué exposición a CIP/SIP verá realmente el sistema?
- ¿Qué nivel de acabado se requiere para la limpieza y la inspección?
- ¿Qué ensamblajes locales conllevan el mayor riesgo de contaminación o retención?
- ¿Qué paquete de documentación se requiere para la liberación de QA?
- ¿Es suficiente el estándar 316L, o los requisitos de acabado y fabricación cambian la respuesta?
Qué Definir en la Solicitud de Cotización
- Grado de aleación
- Estándar de tubería
- Requisito de acabado superficial
- Criterios de aceptación de soldadura
- Expectativas de pasivación / post-fabricación
- Certificados y entregables de trazabilidad
- Requisitos de inspección para liberación
Conclusión: Una Buena Selección de Materiales Farmacéuticos es una Decisión de Sistema, No una Compra de Metal
La selección de materiales de tuberías higiénicas para farmacéuticas es una decisión de sistema, no una compra de metal. Los proyectos más sólidos eligen materiales considerando juntos la resistencia a la corrosión, el acabado, la soldabilidad, el régimen de limpieza, la documentación de control de calidad y el riesgo del proceso. Por eso el 316L es tan común en tuberías higiénicas GMP críticas, pero también por eso el 316L solo nunca es la respuesta completa.
Si desea un grupo de temas farmacéuticos más limpio, conecte este artículo con Acero Inoxidable 316L Electropulido vs 316L Estándar, Selección de Conexiones de Grado Alimentario para Instalaciones GMPy Documentación y Trazabilidad en Proyectos de Tubería Farmacéutica.
PREGUNTAS FRECUENTES
¿Es el acero 316L siempre requerido en tuberías de grado alimentario farmacéutico?
No. El 316L es la línea base práctica para muchos sistemas higiénicos farmacéuticos críticos, pero la elección final aún depende de la química del proceso, el requisito de acabado, la densidad de soldadura, las expectativas de validación y el riesgo del proyecto.
¿Cuál es la diferencia entre el acero 316L electropulido y el 316L estándar en servicio farmacéutico?
La familia de aleación base puede ser la misma, pero la condición de la superficie no lo es. El 316L electropulido se elige donde se necesita una consistencia de acabado más estricta, limpiabilidad e inspeccionabilidad.
¿Se puede seguir utilizando acero 304L en proyectos de tuberías farmacéuticas?
A veces. Puede seguir apareciendo en aplicaciones de menor riesgo o heredadas, pero los sistemas de contacto con productos higiénicos GMP críticos a menudo se mueven hacia el 316L porque la decisión es más amplia que solo el costo de corrosión.
¿Por qué la documentación es parte de la selección de materiales en proyectos de GMP?
Porque la liberación de control de calidad depende de la prueba, no solo de la intención. Un material correcto sin trazabilidad, certificados y registros de inspección relacionados sigue siendo un riesgo para el proyecto.
¿Qué estándares son los más importantes al seleccionar materiales de tuberías higiénicas para la industria farmacéutica?
ASME BPE, FDA 21 CFR 211.65 y 211.67, ASTM A270, y el marco GMP incluyendo el Anexo 1 están entre los puntos de partida más útiles. Definen cómo los ingenieros establecen los materiales, la calidad de fabricación, la limpiabilidad y las expectativas de documentación.
¿Una buena selección de aleación elimina la necesidad de control de soldadura y acabado?
No. Una aleación correcta con una consistencia de acabado deficiente, una calidad de soldadura débil o un tratamiento post-fabricación incompleto aún puede fallar en el propósito higiénico del proyecto.




