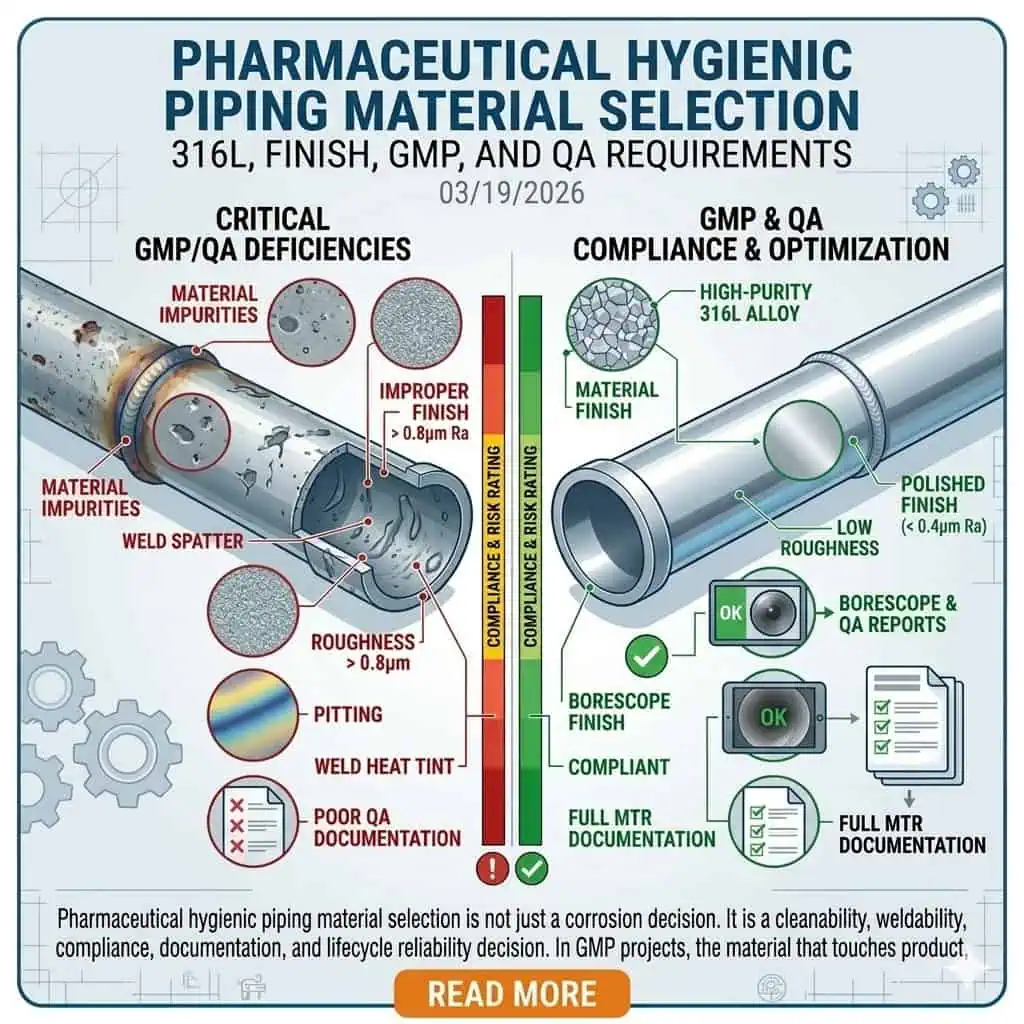
La selezione dei materiali per tubazioni alimentari farmaceutiche non è solo una decisione sulla corrosione. È una decisione sulla pulibilità, saldabilità, conformità, documentazione e affidabilità del ciclo di vita. Nei progetti GMP, il materiale che entra in contatto con il prodotto, i fluidi di processo, l'acqua ad alta purezza o i mezzi di pulizia deve fare più che “resistere alla ruggine”. Deve rimanere non reattivo, non additivo, non assorbente, pulibile, ispezionabile e supportare una fabbricazione ripetibile e il rilascio QA. Ecco perché gli ingegneri esperti non selezionano tubi e raccordi solo in base al nome della lega.
Nella maggior parte dei sistemi di tubazioni alimentari farmaceutiche, l'acciaio inossidabile 316L è la linea di base pratica per il servizio critico di contatto con il prodotto metallico perché bilancia il margine di corrosione, la saldabilità, l'accettazione del settore e la compatibilità con le pratiche di fabbricazione ad alta purezza. Ciò non significa che ogni linea, ogni raccordo o ogni assemblaggio debba essere gestito allo stesso modo. La decisione corretta dipende dalla chimica effettiva del processo, dal regime CIP/SIP, dal requisito di finitura superficiale, dalla densità di saldatura, dalla sensibilità alla contaminazione e dal pacchetto di documentazione richiesto per il passaggio e la convalida.
Questa guida spiega come gli ingegneri selezionano i materiali per le tubazioni alimentari farmaceutiche, dove il 316L ha chiaramente senso, dove lo standard 316L potrebbe non essere sufficiente senza la giusta finitura e qualità di saldatura, e dove la documentazione e la tracciabilità diventano altrettanto importanti del metallo stesso. Nelle revisioni effettive del progetto, la decisione finale sul materiale viene raramente modificata da un grande fallimento. Di solito viene modificata da un modello di problemi minori: una saldatura più difficile da ispezionare del previsto, un record di finitura che non si chiude in modo pulito con la QA, un ramo campione che subisce cicli SIP più severi rispetto al resto del circuito o un assemblaggio locale che si comporta come una zona a rischio più elevato di quanto suggerito dal P&ID.
Cosa significa realmente la selezione dei materiali per tubazioni alimentari farmaceutiche
La scelta del materiale è una decisione GMP e di controllo della contaminazione
Nei sistemi farmaceutici, la selezione dei materiali fa parte del controllo della contaminazione. Un tubo, un corpo valvola, una fascetta o un raccordo non viene accettato perché sembra alimentare. Viene accettato perché la superficie a contatto con il prodotto può supportare il processo previsto senza alterare sicurezza, identità, resistenza, qualità o purezza. Questo principio si allinea con FDA 21 CFR 211.65, che richiede che le superfici a contatto con il prodotto siano non reattive, non additive e non assorbenti.
In pratica, ciò significa che gli ingegneri esaminano la scelta del materiale insieme alla finitura superficiale, alle condizioni di saldatura, alla drenabilità, alla passivazione, alla chimica di pulizia e all'accessibilità per l'ispezione. Una lega corretta con una scarsa purga della saldatura, una condizione superficiale non controllata o una documentazione debole può comunque diventare un problema GMP. Una lezione comune sul campo è che un pacchetto di tubazioni può apparire tecnicamente accettabile al rilascio della fabbricazione e comunque diventare difficile durante la qualifica perché la decisione sul materiale è stata trattata come un articolo di acquisto piuttosto che come una decisione di controllo della contaminazione.
Nota ingegneristica: nel lavoro GMP, la domanda non è solo “Questa lega sopravviverà?” ma anche “Questa superficie finita, saldata e documentata si comporterà in modo prevedibile nell'ispezione, nella pulizia e nel rilascio QA?”
Perché la selezione delle tubazioni farmaceutiche è diversa dal servizio sanitario generale
Le tubazioni igieniche farmaceutiche sono generalmente soggette a standard più rigorosi rispetto al servizio sanitario generale per alimenti o utilità. La ragione non è solo il valore del prodotto. È la conseguenza di contaminazione, ritenzione di residui, sostituzioni non documentate, fabbricazione incoerente e rilascio QA ritardato in ambienti validati. Lo stesso grado di acciaio inossidabile può essere accettabile in un'applicazione alimentare generale ma comunque risultare insufficiente in un sistema GMP se la consistenza della finitura, i registri di saldatura o la tracciabilità non sono controllati al livello richiesto dal progetto.
Ecco perché la revisione dei materiali nei progetti farmaceutici dovrebbe affiancarsi alla selezione delle connessioni, al controllo dei rami morti, all'accettazione delle saldature e alla pianificazione del passaggio QA. Una lega corretta in un assemblaggio sbagliato rimane comunque un risultato ingegneristico errato.
Quali Standard Guidano Effettivamente la Decisione
Gli standard più utili sono quelli che cambiano ciò che si specifica, si ispeziona e si accetta. Nelle tubazioni alimentari farmaceutiche, i riferimenti più rilevanti di solito includono:
- ASME BPE per la logica di materiali, progettazione, fabbricazione, ispezione, test e certificazione nelle apparecchiature di bioprocessing e farmaceutiche.
- FDA 21 CFR 211.65 per la costruzione delle apparecchiature e l'idoneità delle superfici a contatto con il prodotto.
- FDA 21 CFR 211.67 per le aspettative di pulizia e manutenzione.
- ASTM A270/A270M per tubazioni alimentari, inclusa l'opzione di specificare la qualità farmaceutica come requisito supplementare.
- EU GMP Allegato 1 per il controllo della contaminazione, la gestione del rischio di qualità e le aspettative di produzione sterile.
Il compito dell'ingegnere è trasformare quei requisiti in decisioni effettive su materiali, finitura, saldatura e documentazione che possano sopravvivere a approvvigionamento, fabbricazione, ispezione, avvio e revisione QA. Nei progetti solidi, gli standard non sono citati alla fine per giustificare una scelta finita. Sono tradotti all'inizio nel linguaggio RFQ, nei criteri di ispezione, nei requisiti di consegna e nei limiti di controllo delle modifiche.
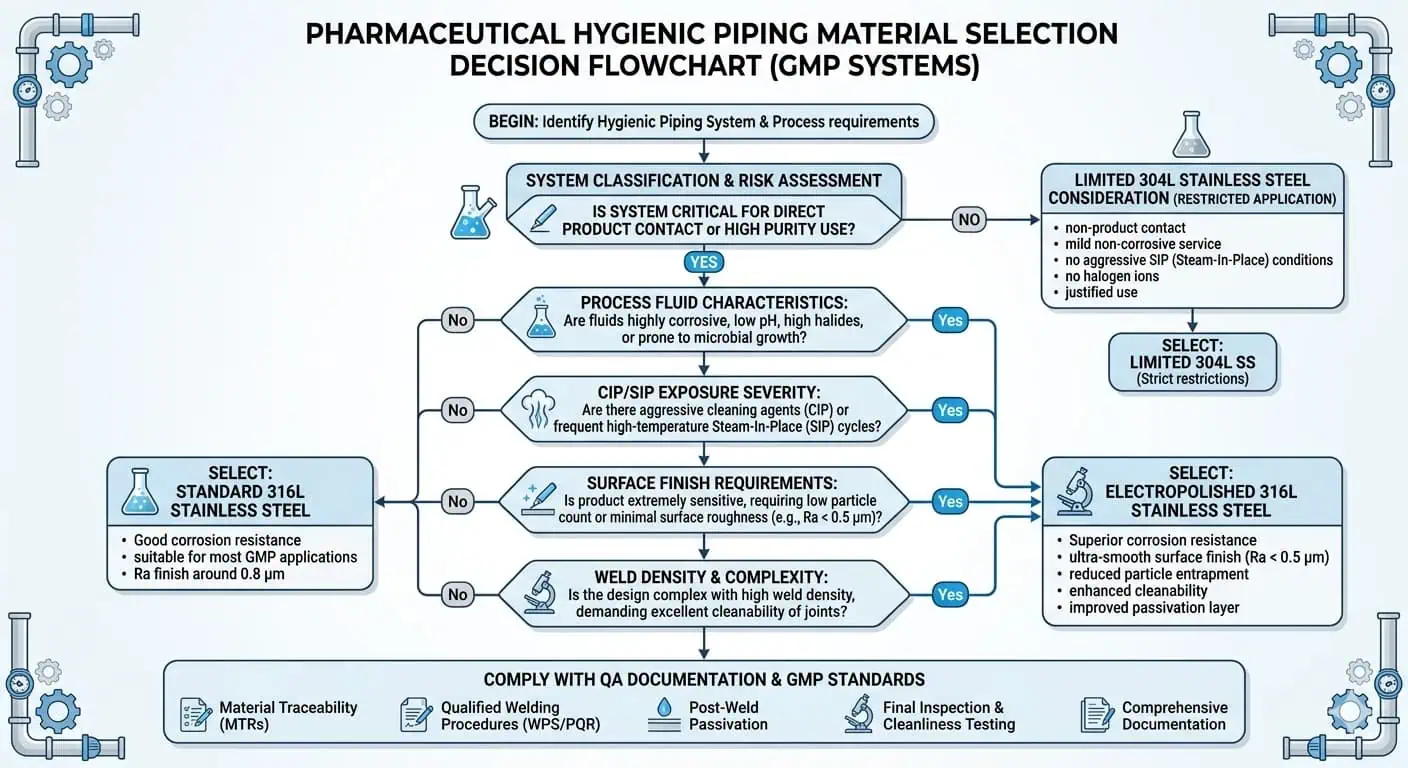
Le Famiglie di Materiali Principali Utilizzate nelle Tubazioni Igieniche Farmaceutiche
Perché il 316L È la Base Pratica per Molti Sistemi Igienici GMP
L'acciaio 316L è comunemente considerato il materiale metallico di base per le tubazioni alimentari critiche farmaceutiche perché offre una combinazione pratica di resistenza alla corrosione, saldabilità e ampia accettazione nel settore. La qualità a basso tenore di carbonio supporta la fabbricazione saldata alimentare in modo più affidabile rispetto all'acciaio 316 standard in molte condizioni di processo, e la composizione contenente molibdeno migliora la resistenza alla corrosione localizzata rispetto agli acciai 304/304L in ambienti di pulizia e servizio più impegnativi.
Ciò non rende l'acciaio 316L una soluzione magica. Significa che l'acciaio 316L è spesso il punto di partenza più difendibile per le tubazioni metalliche a contatto con il prodotto quando il sistema deve anche supportare aspettative di fabbricazione ad alta purezza e documentazione. Nei progetti reali, gli ingegneri spesso scelgono l'acciaio 316L non perché ogni sezione del sistema sia chimicamente severa, ma perché il rischio totale del progetto è sostenuto dagli assemblaggi saldati, dalla pulibilità locale, dall'esposizione a SIP/CIP e dalle aspettative di validazione insieme.
Quando l'acciaio 304/304L può ancora apparire—e perché è spesso limitato
L'acciaio 304 o 304L può ancora apparire in alcuni progetti farmaceutici, ma solitamente in ruoli più limitati. Servizi ausiliari a basso rischio, sistemi legacy, aree di supporto non critiche o progetti storici guidati dai costi possono ancora utilizzare materiali della famiglia 304. Ma nelle tubazioni alimentari critiche a contatto con il prodotto, il settore di solito si orienta verso l'acciaio 316L perché il rischio totale è più ampio della sola corrosione di massa.
Questo è uno degli errori di specifica più comuni nei progetti in fase iniziale: trattare la scelta tra acciaio 304 e 316L come una semplice scelta di prezzo invece che una scelta di pulibilità, fabbricazione e rischio QA. In pratica, quando un team chiede se l'acciaio 304L può ancora essere utilizzato, la migliore domanda di follow-up è solitamente: utilizzato dove, sotto quale regime di pulizia, con quale requisito di finitura e sotto quale standard di documentazione?
Dove i materiali non metallici contano ancora
La selezione dei materiali per le tubazioni farmaceutiche non si ferma alla parete del tubo. Diaframmi, sedi di valvola, guarnizioni, tubi flessibili e altre parti bagnate non metalliche spesso determinano se l'assemblaggio finale funziona come previsto. PTFE, PTFE modificato, EPDM, FKM, silicone o composti specifici per l'applicazione possono essere coinvolti a seconda della chimica, della temperatura, dell'esposizione SIP e dei requisiti di validazione.
In molte deviazioni GMP, il punto debole non è il tubo in acciaio inossidabile. È il materiale di interfaccia che è stato trattato come un consumabile minore invece che come un componente bagnato controllato. Un esempio comune è un sistema metallico chimicamente compatibile abbinato a un materiale di tenuta che invecchia più rapidamente sotto ripetuti SIP di quanto ipotizzato nella revisione del rischio originale. La lezione non è che la selezione del metallo fosse sbagliata in isolamento; è che il sistema bagnato non è stato rivisto nel suo insieme.
Come gli ingegneri decidono tra 316L standard, 316L elettrolucidato e opzioni di specifica superiore
316L standard vs 316L elettrolucidato
316L standard e 316L elettrolucidato non sono famiglie di leghe in competizione. Sono decisioni diverse sulla condizione superficiale basate sulla stessa famiglia di materiale di base. 316L standard può essere pienamente accettabile dove la finitura richiesta, la pulibilità e le aspettative di ispezione sono moderate. 316L elettrolucidato diventa più attraente dove i requisiti di consistenza superficiale, comportamento di rilascio dei residui, ispezionabilità e pulibilità ad alta purezza sono più stringenti.
La domanda migliore non è “L'elettrolucidatura è migliore?” ma “Questo processo ha bisogno dei vantaggi legati alla finitura abbastanza fortemente da giustificare il requisito più stringente?” Nella revisione ingegneristica reale, l'elettrolucidatura è spesso selezionata non perché il 316L standard fallisca ovunque, ma perché il processo richiedeva una superficie più controllata per la fiducia nell'ispezione, la risposta ai residui o la disciplina operativa ad alta purezza. Per la discussione dettagliata sulla finitura, collega questo articolo con Acciaio inossidabile 316L elettrolucidato vs 316L standard.
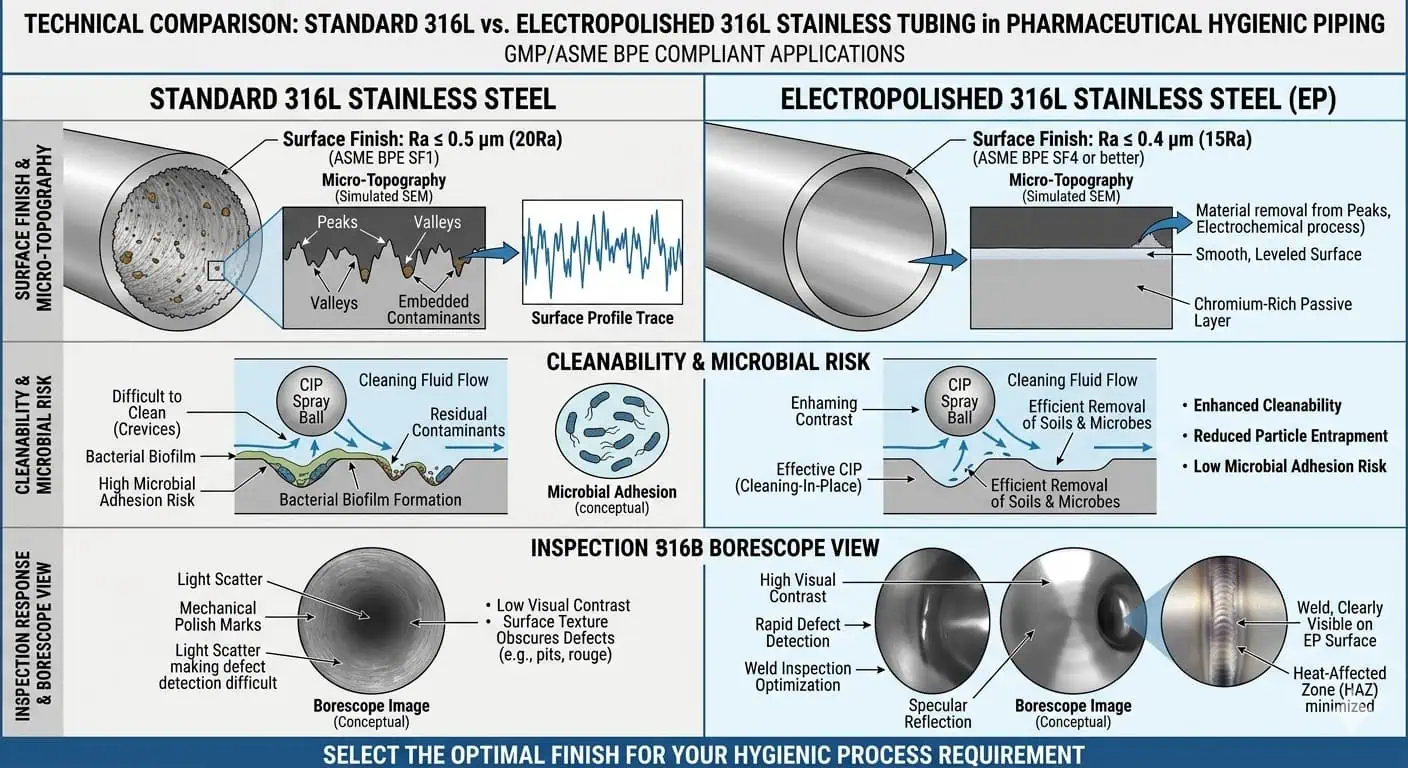
Quando la finitura superficiale cambia la reale prestazione igienica
La finitura superficiale non è un aggiornamento cosmetico nel servizio farmaceutico. Cambia la pulibilità, la risposta all'ispezione e il comportamento di ritenzione dei residui. La finitura è fondamentale dove il processo è sensibile ai residui, dove la ripetibilità SIP/CIP è critica, dove l'ispezione a contatto con il prodotto è rigorosa o dove la geometria locale rende qualsiasi difetto superficiale più rilevante.
Negli ambienti ad alta purezza e biofarmaceutici, gli ingegneri non separano la scelta della lega dalla scelta della finitura perché il risultato igienico è creato da entrambe insieme. Una lezione ripetuta dalle indagini sul campo è che un sistema può utilizzare la lega corretta e comunque sottoperformare se la condizione della finitura locale varia più di quanto consentito dal modello di rischio.
Quando è giustificata una revisione di lega superiore o materiale speciale
A volte l'acciaio 316L non è ancora sufficiente, ma tale decisione dovrebbe derivare dalla chimica e dal meccanismo di guasto, non dall'abitudine. L'esposizione più aggressiva agli alogenuri, sistemi di solventi insoliti, chimica di processo forte o una storia ripetuta di guasti possono giustificare una revisione di lega superiore. Tale passo dovrebbe basarsi su dati reali di servizio, revisione del meccanismo di corrosione e chimica di processo, non su un'ipotesi generica che “il farmaceutico utilizza sempre il grado più alto disponibile”.”
Il consiglio esperto qui è semplice: non aumentare la lega perché il sistema è “importante”. Aumentarla solo quando si può definire la modalità di guasto che si sta cercando di prevenire e il motivo per cui l'opzione di base non fornisce un margine sufficiente.
Selezione del materiale per area di processo negli impianti farmaceutici
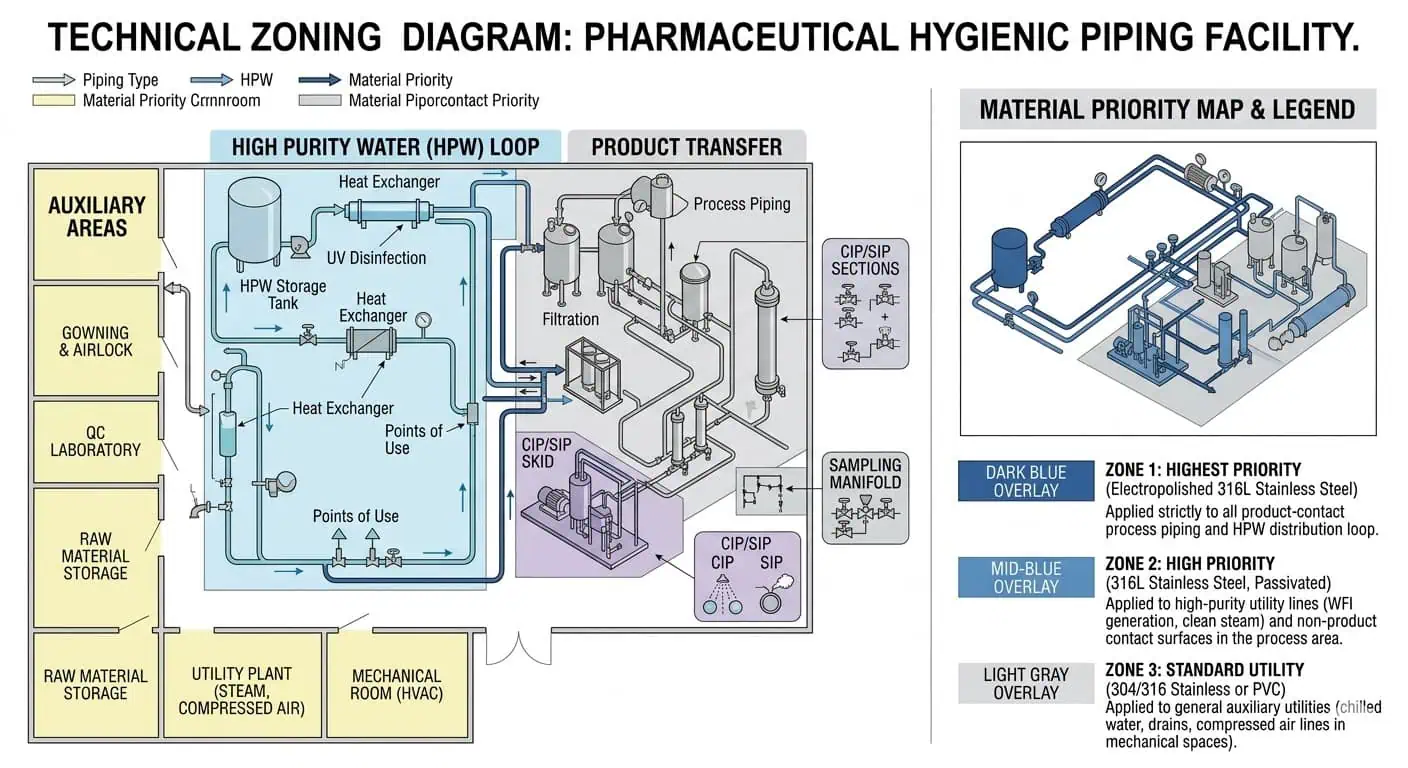
Sistemi relativi ad acqua ad alta purezza e utility pulite
I circuiti di acqua ad alta purezza e utility pulite correlate esercitano pressione sulla consistenza del materiale, la qualità della saldatura e la stabilità superficiale a lungo termine. In questi sistemi, la scelta del materiale è strettamente legata alla tendenza all'arrugginimento, alla coerenza della finitura, all'accettabilità della saldatura e alla compatibilità con la sanificazione. Le specifiche più rigorose di solito si concentrano meno sul solo nome della lega e più sulla capacità del pacchetto completo tubazione-e-saldatura di supportare prestazioni igieniche stabili e ripetibili nel tempo.
Nota tecnica tipica: nei circuiti ad acqua ad alta purezza, la prima preoccupazione spesso non è la corrosione di massa della parete. È l'incoerenza locale della finitura, lo stato della saldatura o il ripristino incompleto della superficie a contatto con il prodotto dopo la fabbricazione e la rielaborazione. Ecco perché gli ingegneri che hanno visto ripetute indagini sui circuiti tendono a concentrarsi precocemente sull'esecuzione della saldatura e sulle prove di finitura, non solo sulla designazione della lega.
Linee di processo a contatto con il prodotto e assemblaggi di trasferimento
Le linee di processo a contatto con il prodotto di solito giustificano il pensiero più conservativo sui materiali. Qui è dove la corrosione, il cambiamento superficiale, la preoccupazione per gli estraibili o l'incoerenza di fabbricazione possono avere l'effetto più diretto sulla qualità del prodotto e sulla fiducia nel lotto. Il grado del materiale, la finitura, le interfacce dei raccordi e il pacchetto di documentazione dovrebbero essere tutti definiti prima della RFQ, non chiariti dopo la fabbricazione.
In termini di progetto, è qui che “accettabile per uso sanitario generale” e “accettabile per uso validato a contatto con il prodotto” si separano più chiaramente. La penalità per una chiarificazione tardiva è spesso non solo la rielaborazione tecnica, ma il ritardo nella FAT, SAT o nella chiusura QA.
Sezioni esposte a CIP/SIP
Le sezioni esposte a CIP/SIP spesso rivelano la debolezza del materiale più rapidamente del processo stesso. I ripetuti cicli di acqua calda, vapore pulito, caustico, acido, sanificante e raffreddamento cambiano significativamente l'ambiente di servizio. In pratica, molti problemi legati ai materiali nelle tubazioni farmaceutiche non sono rivelati prima dal prodotto; sono rivelati dai ripetuti cicli di pulizia e sterilizzazione.
Questa è una delle ragioni per cui un ingegnere dovrebbe esaminare insieme i materiali a contatto con il fluido, sia metallici che non metallici, ogni volta che il sistema è sottoposto a cicli ripetuti di SIP/CIP. Un modello comune sul campo è che la tubazione rimanga accettabile mentre una guarnizione locale, una sede o un'assemblaggio di diramazione invecchia più rapidamente del previsto sotto il ciclo termico e chimico reale.
Valvole di Campionamento, Collettori di Valvole e Altri Assemblaggi Locali ad Alto Rischio
Le decisioni più difficili sui materiali riguardano spesso gli assemblaggi locali, non i tratti rettilinei di tubazione. Le valvole di campionamento, i collettori di distribuzione, le connessioni di diramazione, le valvole a diaframma e i tee per strumentazione combinano una maggiore densità di saldature, più interfacce, più rischio di zone morte e una maggiore sensibilità all'ispezione. È qui che il pacchetto igienico complessivo è più importante.
Ecco perché questo articolo dovrebbe collegarsi direttamente con Selezione di raccordi alimentari per strutture GMP. Nel settore farmaceutico, la lega corretta nell'assemblaggio sbagliato è comunque un risultato errato. Gli ingegneri che risolvono regolarmente i problemi di questi sistemi sanno che la linea raramente fallisce “ovunque”. Fallisce prima nel dettaglio locale che è stato trattato come normale quando in realtà era il punto a più alto rischio nel circuito.
Saldabilità, Condizione della Superficie e Trattamento Post-Fabbricazione
Perché la Densità di Saldatura Cambia il Rischio del Materiale
Più saldature contiene un sistema igienico, meno utile è parlare di scelta del materiale come se contasse solo il tubo base. Le zone termicamente alterate dalla saldatura, la qualità della purga, la condizione del cordone interno, la coerenza della saldatura orbitale e la storia delle riparazioni influenzano tutti se il sistema finale si comporta come un asset GMP pulibile o come una fonte ricorrente di deviazioni.
Un sistema con eccellente scelta di lega ma scarsa esecuzione delle saldature rimane comunque un sistema farmaceutico debole. In termini pratici, ogni saldatura aggiunta aumenta l'importanza della disciplina di fabbricazione, non solo l'importanza del certificato della lega.
Perché i difetti superficiali possono compromettere una buona scelta del materiale
Una lega corretta non salva una superficie di contatto con il prodotto scadente. Irregolarità superficiali, scolorimento delle saldature, contorno irregolare, graffi, contaminazione dalla manipolazione in fabbricazione o riparazioni non controllate possono tutti ridurre il valore igienico di una buona selezione del materiale. Questo è dove gli ingegneri spesso vedono il primo divario tra l'intento della specifica e la realtà installata.
Caso tipico del settore: Il progetto ha specificato correttamente 316L per un circuito critico di contatto con il prodotto, ma il pacchetto di consegna ha comunque sollevato preoccupazione perché l'aspetto locale delle saldature, la coerenza della finitura e la revisione con boroscopio non supportavano lo standard igienico dichiarato. La lega non era il problema. La condizione superficiale fabbricata lo era.
Quel caso è abbastanza comune da essere significativo. È una ragione per cui i revisori esperti non approvano mentalmente un circuito solo perché il certificato di prova del materiale sembra corretto.
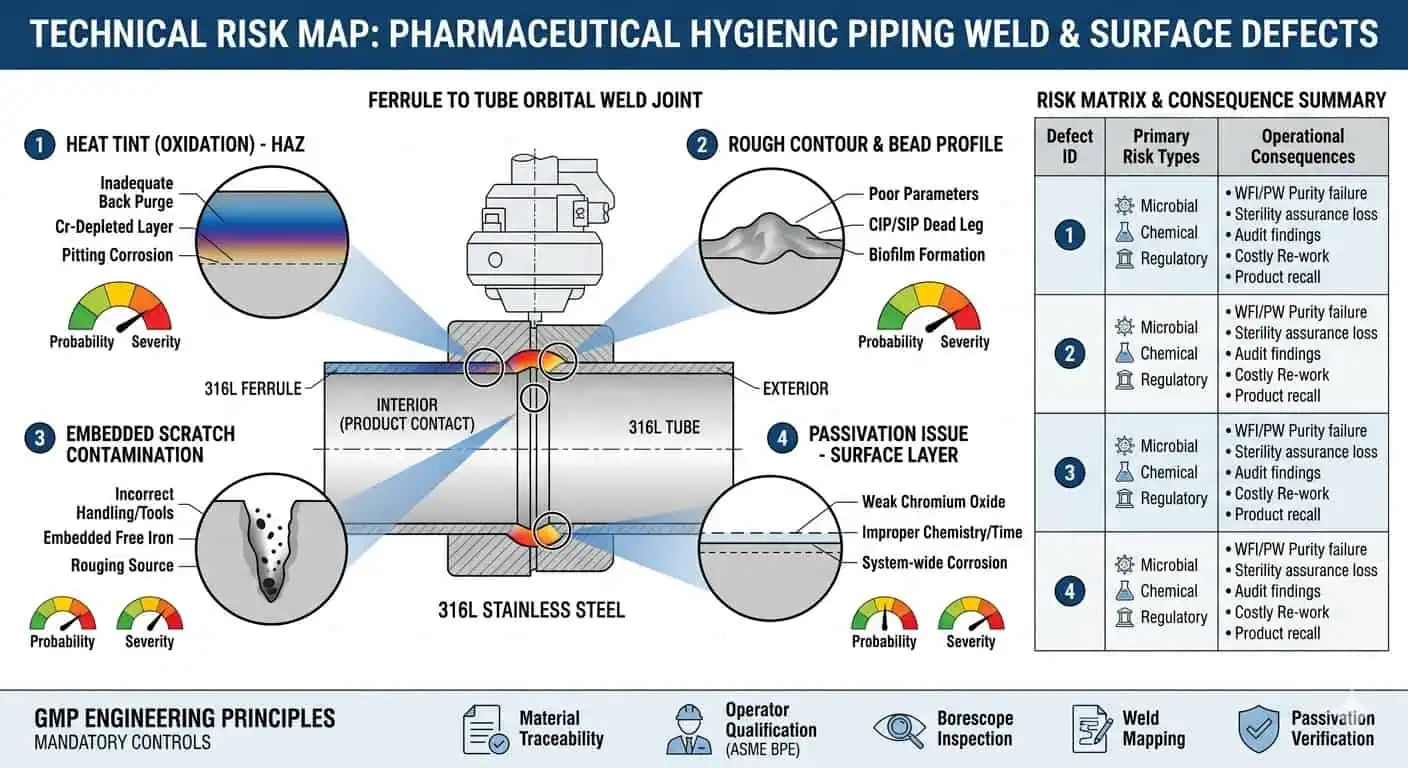
Passivazione, Compatibilità di Pulizia e Stabilità a Lungo Termine
La passivazione e il trattamento post-fabbricazione fanno parte della strategia del materiale, non sono un tocco finale opzionale. Un materiale che è corretto sulla carta ma mal rifinito, mal pulito dopo la fabbricazione o inadeguatamente ripristinato dopo il lavoro di saldatura non si comporterà come il materiale specificato era inteso comportarsi. Questo conta ancora di più nei sistemi con ripetute pulizie, sanificazioni e controlli di validazione.
Il consiglio esperto qui è semplice: non trattare mai la condizione superficiale post-produzione come un elemento di finitura estetica. Nel servizio farmaceutico igienico, è parte integrante della prestazione tecnica della decisione sul materiale stesso.
Documentazione e Tracciabilità: Perché la Selezione del Materiale è anche una Decisione di Controllo Qualità
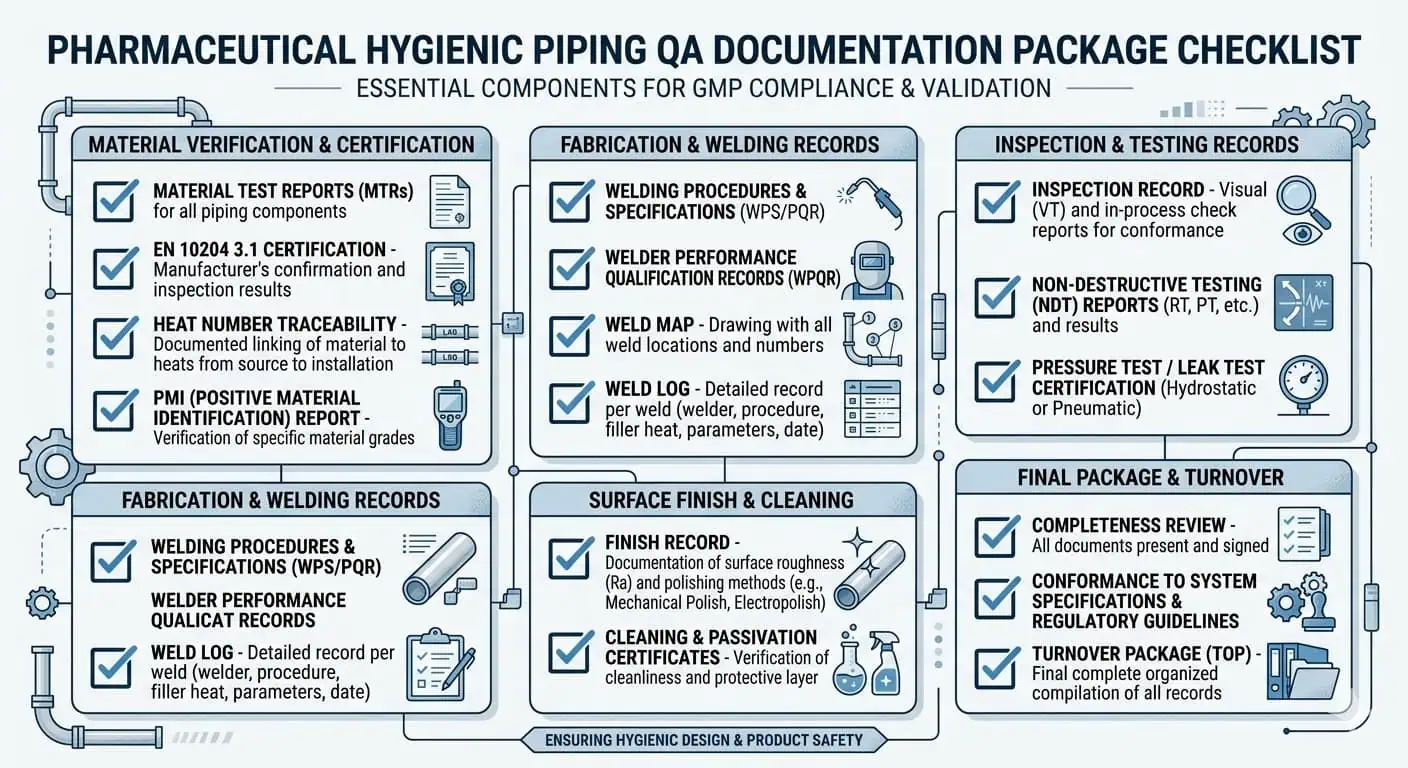
Cosa il Controllo Qualità di solito vuole vedere
Nei progetti di tubazioni GMP, il materiale corretto è solo metà della risposta. Il Controllo Qualità di solito ha bisogno di prove. A seconda dell'ambito del progetto, ciò può includere numeri di colata, certificati di prova materiale, certificati EN 10204 3.1, registri PMI dove richiesti, registri di finitura superficiale, mappe di saldatura, registri di saldatura, registri di ispezione e documentazione di consegna che collega l'assemblaggio installato alla specifica approvata.
Il pacchetto esatto varia per progetto, ma lo schema è coerente: se la scelta del materiale non può essere tracciata e verificata, rimane un rischio di progetto. È qui che molti pacchetti tecnicamente capaci perdono tempo durante la consegna: non perché la metallurgia fosse sbagliata, ma perché la catena di prove era più sottile di quanto richiesto dall'ambiente GMP.
Perché “Materiale Corretto” Senza Registri è Ancora un Rischio di Progetto
Uno dei fallimenti più comuni nei progetti farmaceutici non è la selezione errata della lega. È la chiusura incompleta della catena di prove. Il tubo può essere corretto. I raccordi possono essere corretti. Le saldature possono anche essere accettabili. Ma se la tracciabilità, i registri di finitura o la documentazione di ispezione sono incompleti, il rilascio del Controllo Qualità può ancora bloccarsi.
Caso tipico del settore: Un pacchetto di tubazioni GMP ha superato la revisione di fabbricazione ma ha fallito la prontezza di consegna perché la tracciabilità della colata e i registri di finitura per un gruppo di pezzi di tubazione alimentare erano incompleti. Il problema non era la metallurgia tecnica. Era il controllo della documentazione.
Questo è il motivo per cui gli ingegneri esperti considerano la documentazione parte della selezione dei materiali fin dall'inizio, non come un esercizio burocratico per la fine del progetto.
Come Definire i Requisiti dei Materiali Prima della RFQ
Il momento migliore per definire le aspettative sui materiali è prima della RFQ, non durante la revisione della punch-list. Una RFQ solida di solito definisce il grado della lega, lo standard dei tubi, l'obiettivo di finitura, i requisiti di saldatura, le aspettative di passivazione, i deliverable documentali e qualsiasi specifico requisito di ispezione per l'accettazione.
Per il lato completo QA di quel argomento, collega questo articolo con Documentazione e tracciabilità nei progetti di tubazioni farmaceutiche.
Esempi di Ricerca, Casi Industriali e Consigli di Esperti
Caso Ingegneristico Tipico 1: Il 316L Era Corretto, ma la Zona di Saldatura Non Ha Preservato l'Intento Alimentare
Questo è uno dei fallimenti più realistici nelle tubazioni farmaceutiche. Il team di progettazione ha scelto la famiglia di leghe giusta, ma la zona di saldatura installata non ha preservato l'intento alimentare della scelta del materiale. La preoccupazione risultante può manifestarsi come incoerenza di finitura, fallimento dell'ispezione, risposta di pulizia difficile o esitazione della QA sulla qualità locale a contatto con il prodotto.
La lezione è chiara: nel settore farmaceutico, la selezione dei materiali e l'esecuzione delle saldature non possono essere separate. I sistemi più robusti non sono quelli con la descrizione del materiale più costosa. Sono quelli in cui il materiale, la finitura, la fabbricazione e la logica di ispezione supportano tutti lo stesso obiettivo igienico.
Caso Ingegneristico Tipico 2: Il Problema QA Era la Documentazione, Non la Lega
Un'altra modalità di guasto comune si manifesta durante la consegna. Il progetto ha utilizzato il grado di materiale corretto, ma il pacchetto mancava dei documenti necessari per dimostrare la conformità. Certificati mancanti, tracciabilità poco chiara, registri di finitura incompleti o documentazione di saldatura debole possono ritardare l'approvazione anche quando il metallo installato è tecnicamente corretto.
Ecco perché gli ingegneri esperti trattano la documentazione come parte della selezione del materiale fin dall'inizio. Nel lavoro pratico GMP, una scelta corretta non documentata rimane una scelta incompleta.
Caso Ingegneristico Tipico 3: L'Elettrolucidatura Era Necessaria per la Pulibilità, Non Perché l'Acciaio 316L Era “Sbagliato”
A volte l'acciaio 316L standard non viene rifiutato perché la lega è inadeguata, ma perché il requisito di finitura ha cambiato l'obiettivo igienico. In questi casi, la risposta migliore non è dire che il progetto ha scelto la famiglia di metalli sbagliata. La risposta migliore è che il progetto ha infine riconosciuto un requisito di pulibilità e ispezionabilità più stringente di quanto supportato dalla specifica di finitura originale.
Questo è un normale perfezionamento ingegneristico, non un imbarazzo. È esattamente come un team di processo forte migliora l'accuratezza delle specifiche nel tempo.
Consiglio dell'Esperto: Chiedi Quale Guasto Stai Effettivamente Cercando di Prevenire
La domanda migliore per la selezione del materiale non è “Quale grado utilizza la maggior parte delle persone?” È “Quale guasto stiamo cercando di prevenire in questo sistema specifico?” La risposta potrebbe essere la corrosione. Potrebbe essere il rischio di arrugginimento. Potrebbe essere la preoccupazione per gli estraibili. Potrebbe essere la pulibilità guidata dalla finitura. Potrebbe essere l'incoerenza della saldatura. Potrebbe essere il fallimento della chiusura QA. Una volta che la modalità di guasto è chiara, la decisione sul materiale diventa molto più razionale.
Questo è il consiglio più coerente degli ingegneri che hanno affrontato deviazioni reali nelle tubazioni farmaceutiche: definire prima la modalità di guasto, e la logica del materiale diventa più chiara, più ristretta e più facile da difendere.
Errori Comuni nella Selezione dei Materiali per Tubazioni Alimentari Farmaceutiche
Scegliere Solo in Base al Nome della Lega
La famiglia della lega è importante, ma il risultato alimentare installato dipende anche dalla finitura, dalle saldature, dalla geometria, dalle interfacce e dalla documentazione.
Separare il Grado dalla Finitura Superficiale
316L standard e 316L elettrolucidato non sono intercambiabili se l'obiettivo alimentare è definito dalle aspettative di pulibilità e ispezione legate alla finitura.
Ignorare la Saldabilità e la Realtà della Fabbricazione
Un materiale di base corretto con una scarsa esecuzione della saldatura rimane un pacchetto di tubazioni GMP debole.
Trattare la documentazione come un problema post-acquisto
Nei progetti farmaceutici, la documentazione fa parte dell'accettazione, non è un ripensamento per il passaggio di consegna.
Utilizzare una regola unica dei materiali per ogni area di processo
I circuiti ad acqua ad alta purezza, i trasferimenti a contatto con il prodotto, le sezioni esposte a CIP/SIP e le aree ausiliarie non hanno tutte le stesse conseguenze igieniche o di conformità.
Lista di controllo pratica per la selezione dei materiali per tubazioni igieniche farmaceutiche
Domande da Rispondere Prima dell'Approvazione Finale del Materiale
- Quale fluido di processo o prodotto entra effettivamente in contatto con la superficie?
- Quale esposizione CIP/SIP subirà effettivamente il sistema?
- Quale livello di finitura è richiesto per la pulibilità e l'ispezione?
- Quali assemblaggi locali presentano il rischio più elevato di contaminazione o ritenzione?
- Quale pacchetto documentale è richiesto per il rilascio QA?
- Lo standard 316L è sufficiente, o la finitura e i requisiti di fabbricazione cambiano la risposta?
Cosa Definire nella Richiesta di Offerta
- Grado di lega
- Standard del tubo
- Requisito di finitura superficiale
- Criteri di accettazione della saldatura
- Aspettative di passivazione / post-fabbricazione
- Certificati e documenti di tracciabilità
- Requisiti di ispezione per il rilascio
Conclusione: Una Buona Selezione dei Materiali Farmaceutici è una Decisione di Sistema, Non un Acquisto di Metallo
La selezione del materiale per tubazioni alimentari farmaceutiche è una decisione di sistema, non un acquisto di metallo. I progetti più solidi scelgono i materiali considerando insieme resistenza alla corrosione, finitura, saldabilità, regime di pulizia, documentazione QA e rischio di processo. Ecco perché l'acciaio 316L è così comune nelle tubazioni alimentari critiche GMP, ma anche perché l'acciaio 316L da solo non è mai la risposta completa.
Se desideri un cluster di argomenti farmaceutici più pulito, collega questo articolo con Acciaio inossidabile 316L elettrolucidato vs 316L standard, Selezione di raccordi alimentari per strutture GMP, e Documentazione e tracciabilità nei progetti di tubazioni farmaceutiche.
FAQ
La 316L è sempre necessaria nelle tubazioni alimentari farmaceutiche?
No. L'acciaio 316L è la base pratica per molti sistemi alimentari farmaceutici critici, ma la scelta finale dipende ancora dalla chimica del processo, dal requisito di finitura, dalla densità di saldatura, dalle aspettative di validazione e dal rischio del progetto.
Qual è la differenza tra l'acciaio 316L elettrolucidato e l'acciaio 316L standard per applicazioni farmaceutiche?
La famiglia di lega di base può essere la stessa, ma la condizione superficiale no. L'acciaio 316L elettrolucidato è scelto dove sono necessarie una maggiore coerenza di finitura, pulibilità e ispezionabilità.
Il 304L può ancora essere utilizzato in progetti di tubazioni farmaceutiche?
A volte. Può ancora apparire in applicazioni a basso rischio o legacy, ma i sistemi a contatto con prodotti alimentari critici GMP si spostano più spesso verso l'acciaio 316L perché la decisione è più ampia del solo costo della corrosione.
Perché la documentazione fa parte della selezione dei materiali nei progetti GMP?
Perché il rilascio QA dipende dalla prova, non solo dall'intento. Un materiale corretto senza tracciabilità, certificati e relativi registri di ispezione è ancora un rischio per il progetto.
Quali standard sono più importanti nella scelta dei materiali per tubazioni alimentari farmaceutiche?
ASME BPE, FDA 21 CFR 211.65 e 211.67, ASTM A270 e il quadro GMP incluso l'Allegato 1 sono tra i punti di partenza più utili. Definiscono come gli ingegneri definiscono i materiali, la qualità di fabbricazione, la pulibilità e le aspettative di documentazione.
Una buona selezione della lega elimina la necessità di controllo della saldatura e della finitura?
No. Una lega corretta con scarsa uniformità di finitura, qualità di saldatura debole o trattamento post-fabbricazione incompleto può comunque fallire l'intento igienico del progetto.


