La documentazione e la tracciabilità nei progetti di tubazioni farmaceutiche non sono una pratica burocratica aggiunta dopo l'installazione. Sono la catena di prove che dimostra che il sistema installato corrisponde al materiale approvato, alla finitura, alla saldatura, all'ispezione e all'intento progettuale igienico. Nei progetti GMP, un circuito di tubazioni può essere meccanicamente completo e rimanere comunque non rilasciabile perché la documentazione non dimostra chiaramente cosa è stato installato, come è stato fabbricato, cosa è cambiato in campo e se l'assemblaggio finale soddisfa ancora lo standard di progetto approvato.
Ecco perché gli ingegneri esperti non trattano i documenti di consegna come un passaggio amministrativo. Li trattano come parte del controllo di progetto fin dall'inizio. Se la tracciabilità dei materiali, i registri di saldatura, i registri di finitura, le prove di ispezione, le modifiche in rosso e le consegne di turnover non sono definiti prima della RFQ, il progetto spesso cerca di ricostruire la catena di prove in seguito a costi molto più elevati e con minore affidabilità. Questa guida spiega cosa significano realmente documentazione e tracciabilità nei progetti di tubazioni farmaceutiche, quali registri sono più importanti, dove la catena di prove di solito si interrompe e come i team GMP possono definire il pacchetto documentale corretto prima che inizi la fabbricazione.
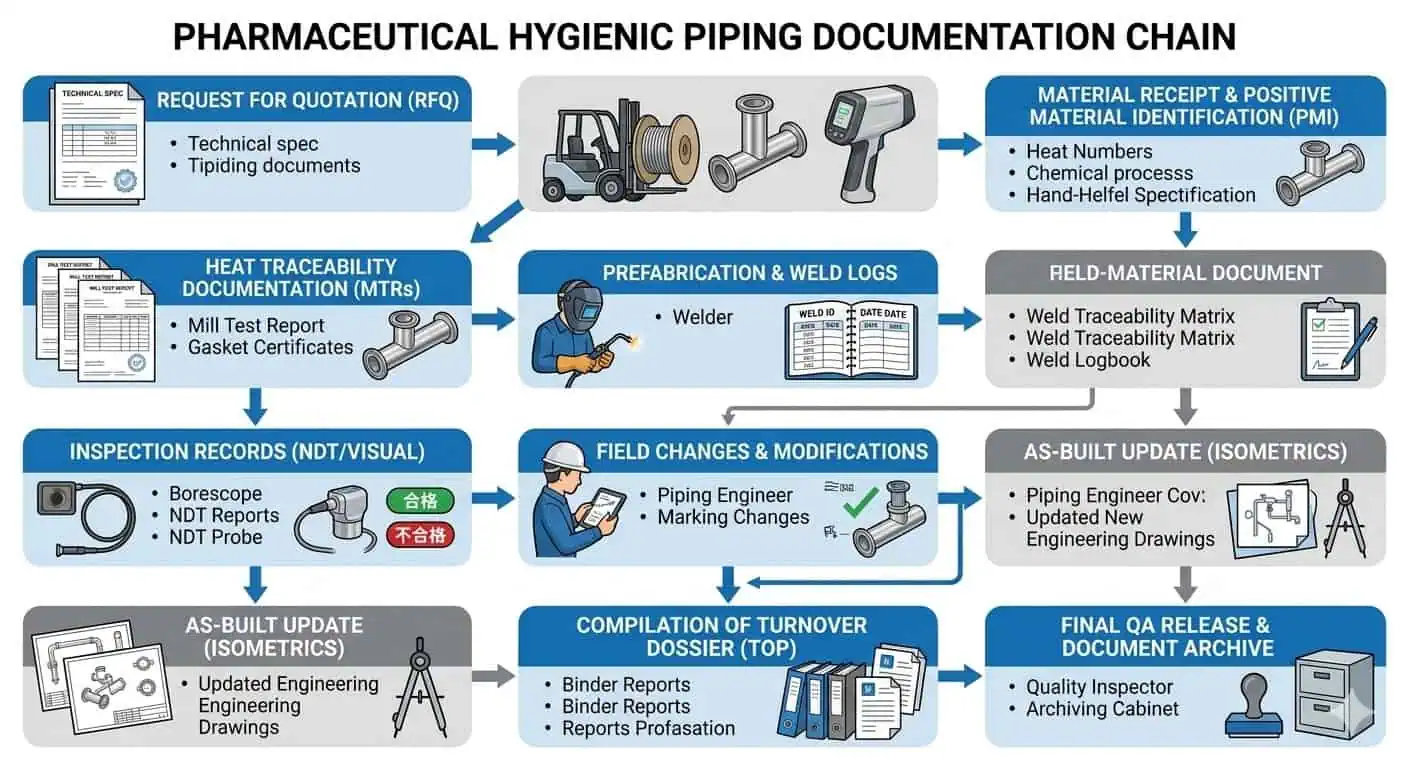
Nel lavoro farmaceutico reale, i problemi di documentazione raramente si manifestano come guasti meccanici drammatici. Si presentano come chiusura QA più lenta, commenti di turnover irrisolti, lignaggio di saldatura poco chiaro, storie di spezzoni non corrispondenti o incertezza sul fatto che il circuito installato finale rifletta ancora l'intento igienico approvato. Ecco perché una documentazione solida non è una preferenza burocratica. È un controllo ingegneristico.
Perché Documentazione e Tracciabilità Sono Importanti nei Progetti di Tubazioni Farmaceutiche
Questo è un Argomento di QA e Rilascio, Non Solo di Archiviazione Ingegneristica
Nelle tubazioni farmaceutiche, la documentazione è parte del controllo di rilascio, non solo dell'amministrazione del progetto. Il Capitolo 4 dell'EU GMP non descrive la documentazione come una comodità di archiviazione. Descrive una buona documentazione come una parte essenziale del sistema di garanzia della qualità e il meccanismo utilizzato per stabilire, controllare, monitorare e registrare le attività che influenzano la qualità del prodotto. La logica FDA punta nella stessa direzione: le apparecchiature a contatto con il prodotto devono essere idonee all'uso, e la pulizia, la manutenzione e la storia delle apparecchiature devono essere controllate e registrate. In altre parole, il circuito installato deve essere tecnicamente corretto e dimostrabilmente corretto allo stesso tempo.
Caso tipico del settore: Un circuito di trasferimento a contatto con il prodotto è completamente installato, testato in pressione e visivamente accettabile. Le operazioni vedono un sistema di tubazioni finito. La QA vede una catena di prove incompleta perché il dossier finale non può ancora collegare chiaramente l'identità del materiale approvato, la storia di saldatura e la configurazione as-built finale. La tubazione è fisicamente presente, ma la logica di rilascio è ancora irrisolta.
Consiglio esperto: Se il team di progetto considera la documentazione come qualcosa che inizia alla consegna, è già troppo tardi. Nelle tubazioni GMP, la storia del rilascio deve essere costruita mentre il circuito viene progettato, fabbricato, ispezionato e modificato—non dopo che l'ultimo morsetto è stato serrato.
Nota ingegneristica: nelle tubazioni GMP, il circuito installato è rilasciabile solo quanto la catena di prove che dimostra la sua condizione finale a contatto con il fluido.
Perché i progetti di tubazioni farmaceutiche spesso falliscono alla consegna, non alla fabbricazione
Molti progetti di tubazioni farmaceutiche non falliscono perché il circuito è stato costruito male. Falliscono perché il progetto non può dimostrare, in forma pronta per il rilascio, che il circuito installato finale corrisponde ancora all'intento igienico approvato. Questo è un tipo diverso di fallimento, ma nel lavoro GMP è spesso quello più pericoloso perché appare tardi, dopo che il sistema sembra già meccanicamente completo. La logica della documentazione del Capitolo 4 EU GMP e della FDA supporta entrambe la stessa conclusione pratica: se la storia di pulizia, l'identità dei componenti, lo stato delle saldature e la configurazione installata non possono essere ricostruiti in modo affidabile, il sistema diventa più difficile da difendere al rilascio e successivamente durante l'operazione.
Caso tipico del settore: Il team di installazione in campo termina un circuito alimentare e presume che il lavoro difficile sia finito. Una revisione successiva mostra che diversi spezzoni sono stati modificati in campo per migliorare il percorso e la pendenza, ma la mappa finale delle saldature, la matrice materiale-posizione e il pacchetto as-built non sono mai stati completamente riconciliati. Nessuno sostiene che il metallo sia sbagliato. Il problema è che il progetto non può più dimostrare chiaramente quali materiali certificati, registri di saldatura e risultati di ispezione appartengono alla disposizione installata finale. A quel punto, il circuito non sta combattendo un difetto di fabbricazione. Sta combattendo un difetto di prova di rilascio.
Gli ingegneri di progetto esperti definiscono quindi la catena di documentazione prima della RFQ, non dopo il completamento meccanico. Una volta che inizia la fabbricazione, ogni taglio in campo non controllato, scambio di spezzoni o ripercorso di diramazione diventa più difficile da chiudere retroattivamente. La lezione ingegneristica è semplice: nelle tubazioni GMP, se si aspetta fino alla consegna per decidere cosa deve essere tracciabile, il progetto di solito finisce per ricostruire la catena di prove a costi più elevati e con minore fiducia.
Cosa richiede effettivamente il quadro normativo GMP e regolatorio
Le normative più utili sono quelle che cambiano ciò che il team di progetto definisce e registra prima della consegna. In questo argomento, il quadro di riferimento principale di solito include:
- ASME BPE, che copre materiali, progettazione, fabbricazione, ispezioni, test e logica di certificazione per attrezzature di bioprocessing e farmaceutiche.
- FDA 21 CFR 211.65, che richiede che le superfici a contatto con il prodotto siano non reattive, non additive e non assorbenti.
- FDA 21 CFR 211.67, che collega la pulizia e la manutenzione delle attrezzature a procedure scritte e registrazioni.
- FDA 21 CFR 211.182, che affronta i registri di pulizia, manutenzione e utilizzo per le attrezzature principali.
- FDA 21 CFR 211.184, che copre i registri di componenti, contenitori, chiusure ed etichettatura.
- EU GMP Capitolo 4, che definisce la documentazione come una parte essenziale del sistema di assicurazione della qualità e richiede che i registri siano controllati, accurati, tracciabili e conservati in modo appropriato.
Risultato della ricerca: queste fonti non trattano la documentazione come supporto di sfondo. La trattano come una parte controllata dell'esecuzione GMP. Per i team di tubazioni, ciò significa che la domanda non è mai solo “quali registri abbiamo?” ma “questi registri dimostrano ancora chiaramente il sistema bagnato finale per il rilascio QA?”
Cosa Deve Essere Tracciabile in un Progetto di Tubazioni GMP
Tubazioni, Raccordi, Valvole e Altri Componenti Bagnati
La tracciabilità dovrebbe seguire il percorso bagnato, non solo i componenti più grandi o più facili. Molti team gestiscono bene le tubazioni ma trattano troppo casualmente raccordi più piccoli, diaframmi, valvole di campionamento, ferrule, guarnizioni e componenti di diramazione. Nei progetti GMP, questo è un errore. Le parti bagnate più piccole sono spesso le più facili da sostituire, le più difficili da tracciare in seguito e le prime a creare domande QA durante il passaggio.
Caso tipico del settore: la tracciabilità delle tubazioni è completa, ma il pacchetto di passaggio diventa debole nelle assemblaggi locali perché raccordi, guarnizioni o interni di valvole di campionamento sono stati gestiti al di fuori del flusso di controllo principale. La linea sembra a posto durante l'ispezione, eppure l'anello di tracciabilità più debole si trova esattamente dove l'assemblaggio alimentare è più complesso.
Consiglio esperto: se un componente è abbastanza importante da essere specificato come parte del progetto alimentare, è abbastanza importante da essere tracciabile come parte della logica di passaggio. In pratica, i team ottengono una migliore chiusura QA quando definiscono la tracciabilità attorno all'intero percorso bagnato invece che solo attorno alle tubazioni.
Certificati di Materiale, Numeri di Colata e Identità di Lotto
La tracciabilità del materiale è utile solo quando la posizione installata può essere collegata chiaramente al set di registri originale. Rapporti di prova del materiale, certificati EN 10204 3.1, numeri di colata e registri di ricevimento sono tutti importanti, ma solo se il progetto preserva il collegamento tra l'identità del fornitore e la posizione installata del tratto, raccordo o assemblaggio. Un mucchio di certificati senza una matrice di posizione chiara non è un pacchetto di tracciabilità forte.
Caso tipico del settore: il progetto dispone dei certificati di materiale corretti, ma dopo il taglio in campo, il riavvolgimento e il reindirizzamento locale, il team di consegna non può dimostrare rapidamente quali numeri di fusione sono finiti in quali sezioni di ramo installate. Il problema non è la mancanza di carta. Il problema è che la carta non corrisponde più chiaramente alla realtà installata.
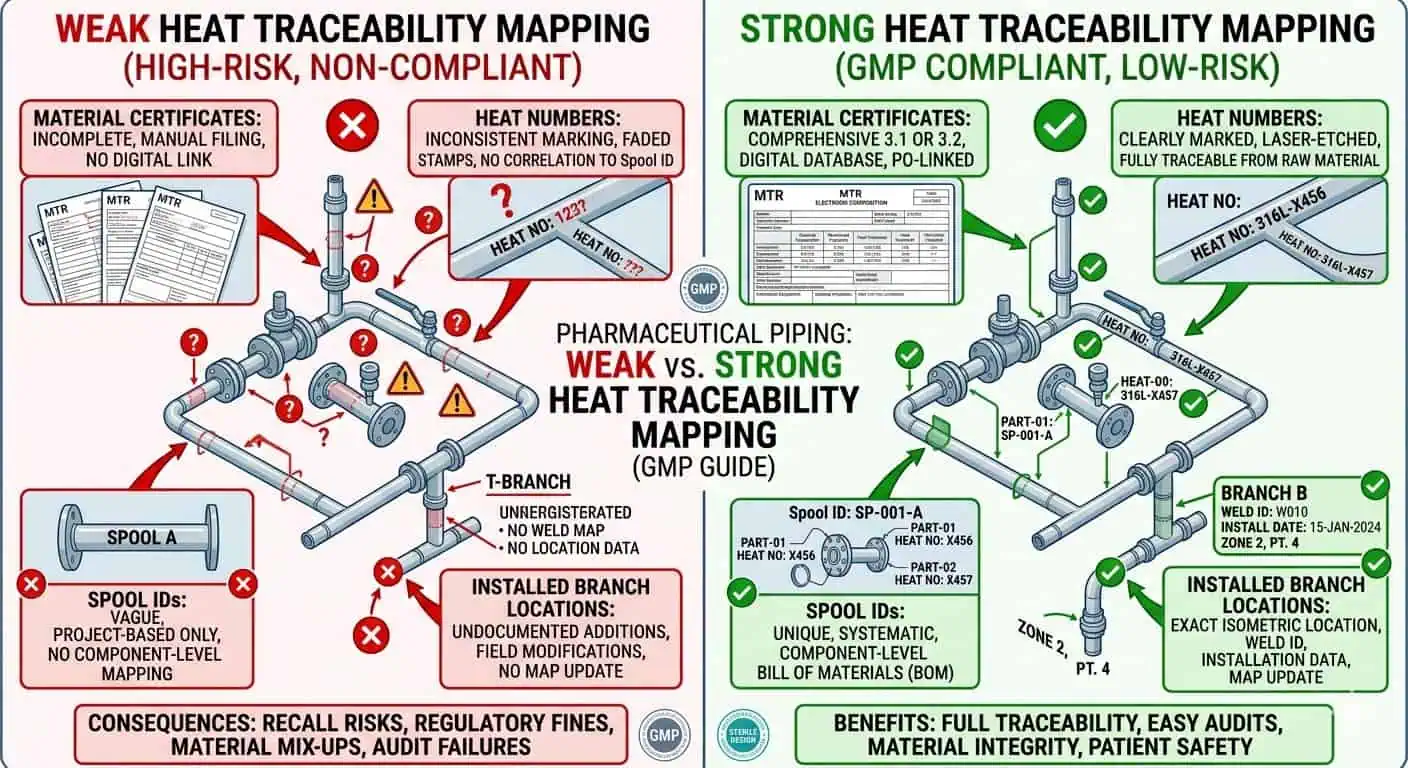
Consiglio esperto: nei sistemi a contatto con prodotti ad alta conseguenza, definire la matrice di tracciabilità in anticipo invece di consentire ai record di materiale e ai record dei tubi di evolversi separatamente. Una volta iniziate le modifiche in campo, ricostruire quel collegamento diventa più lento e meno affidabile.
Mappe di saldatura, registri di saldatura orbitale e stato di ispezione
La documentazione di saldatura è spesso la parte operativamente più importante della catena di prove di tubazione. Nei sistemi farmaceutici alimentari, i numeri di saldatura, le impostazioni della macchina, l'identità dell'operatore, le date, lo stato di ispezione, la cronologia delle riparazioni e lo stato di accettazione sono spesso più decisivi di quanto i team si aspettino. Questo perché la saldatura è dove convergono l'identità del materiale, la qualità della fabbricazione, le prove di ispezione e le prestazioni alimentari finali. ASME BPE è utile qui non perché crea documentazione per se stessa, ma perché tratta fabbricazione, esame, test e certificazione come un quadro di controllo connesso. Nei progetti farmaceutici, i registri di saldatura non sono quindi solo record di officina. Sono record di rilascio.
Caso ingegneristico tipico: un circuito sembra accettabile durante l'ispezione, ma il QA lo segnala comunque perché la mappa di saldatura e la revisione finale del tubo non sono più allineate dopo le modifiche in campo. Le saldature installate possono essere fisicamente accettabili, ma il set di documentazione non dimostra più quali record appartengono a quali posizioni di saldatura finali.
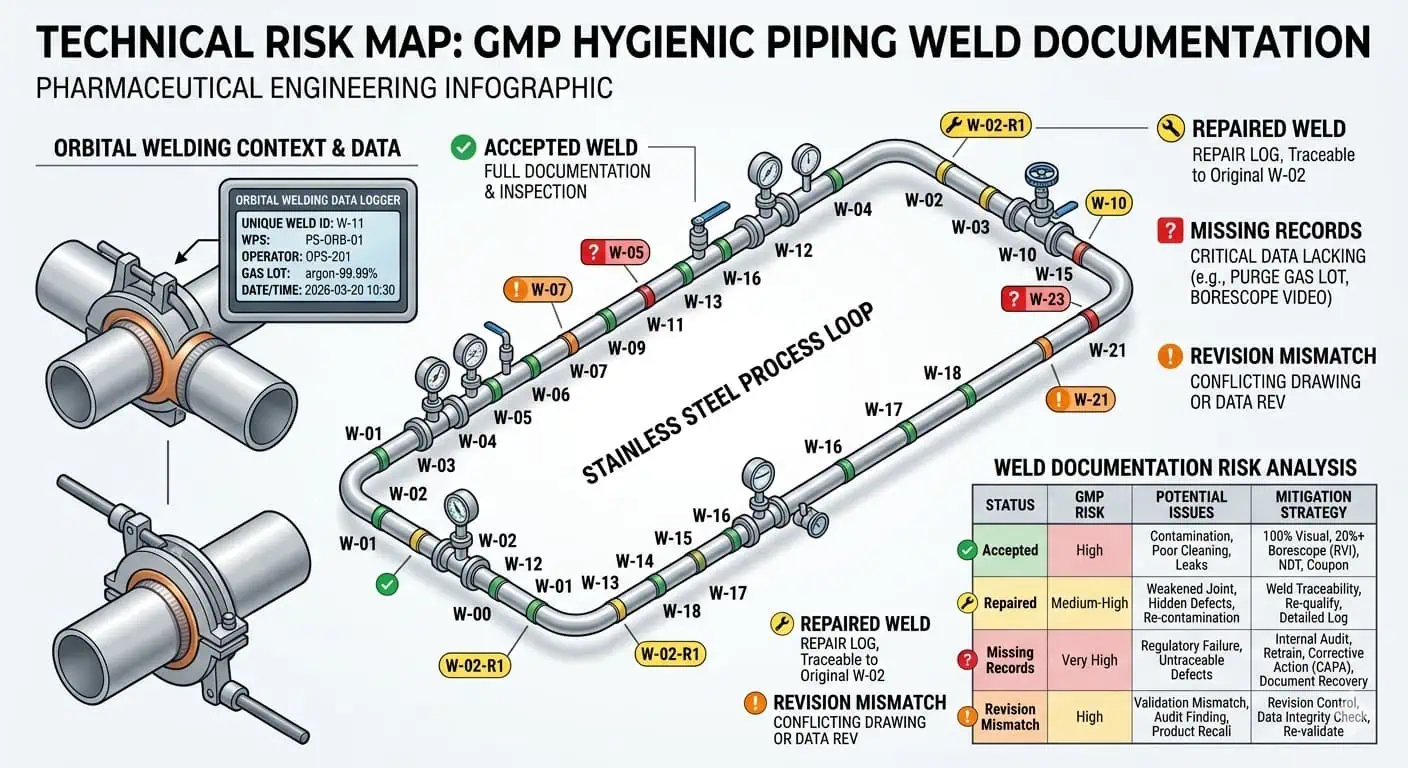
Consiglio esperto: non gestire i record di saldatura come un set di dati solo di fabbricazione. Gestirli come un set di dati di rilascio che deve ancora avere senso dopo le modifiche in campo, la sostituzione dei tubi e la chiusura finale come costruito.
Finitura Superficiale, Elettrolucidatura, Passivazione e Documenti Correlati
I requisiti di finitura contano solo quando il progetto può dimostrare quale finitura era richiesta, quale è stata fornita e come è stata preservata la condizione finale a contatto con il fluido. Nei sistemi GMP più esigenti, la decisione sulla finitura non è separata dalla documentazione. Se il progetto distingue tra 316L standard e 316L elettrolucidato, o richiede prove di passivazione e trattamento post-fabbricazione, tali requisiti necessitano di un percorso di registrazione proprio nel dossier di consegna.
Caso tipico del settore: Il grado del tubo era accettabile, ma la discussione sul rilascio si è spostata sul fatto che la condizione superficiale finale di diversi pezzi di tubazione a contatto con il prodotto corrispondesse ancora alle aspettative igieniche specificate dopo la fabbricazione e la rielaborazione. La lega non era il punto debole. Lo era la condizione di finitura documentata.
Consiglio esperto: Definire la documentazione relativa alla finitura prima dell'inizio della fabbricazione. Se un progetto decide tardivamente che la condizione superficiale è più importante del previsto, i documenti mancanti sono spesso molto più difficili da ricostruire dopo la fabbricazione rispetto ai certificati del materiale.
Modifiche in Rosso, Come Costruiti e Cambiamenti in Campo
I cambiamenti in campo sono dove le catene di tracciabilità si interrompono più spesso. Un ramo viene spostato per l'accesso. Un pezzo di tubazione viene rifatto per adattarsi all'assemblaggio effettivo. Un punto strumentale viene rivisto. L'orientamento di una valvola cambia. Nessuna di queste azioni è automaticamente fatale, ma ognuna crea un rischio documentale se il processo da modifiche in rosso a come costruiti è debole. Uno dei principi documentali più importanti nella pratica GMP è che i documenti dovrebbero essere creati al momento in cui il lavoro avviene. Questo è importante perché i documenti ricostruiti sono quasi sempre più deboli di quelli contemporanei.
Caso industriale: un collegamento di uno skid GMP è stato modificato in campo per migliorare il percorso e l'accesso alla manutenzione. Il cambiamento in sé era ragionevole. Il problema era che i riferimenti di saldatura aggiornati, i riferimenti dei pezzi di tubazione e i disegni come costruiti erano in ritardo rispetto all'installazione. Al momento della consegna, il team stava cercando di riconciliare due versioni tecnicamente simili ma documentalmente inconsistenti dello stesso circuito.
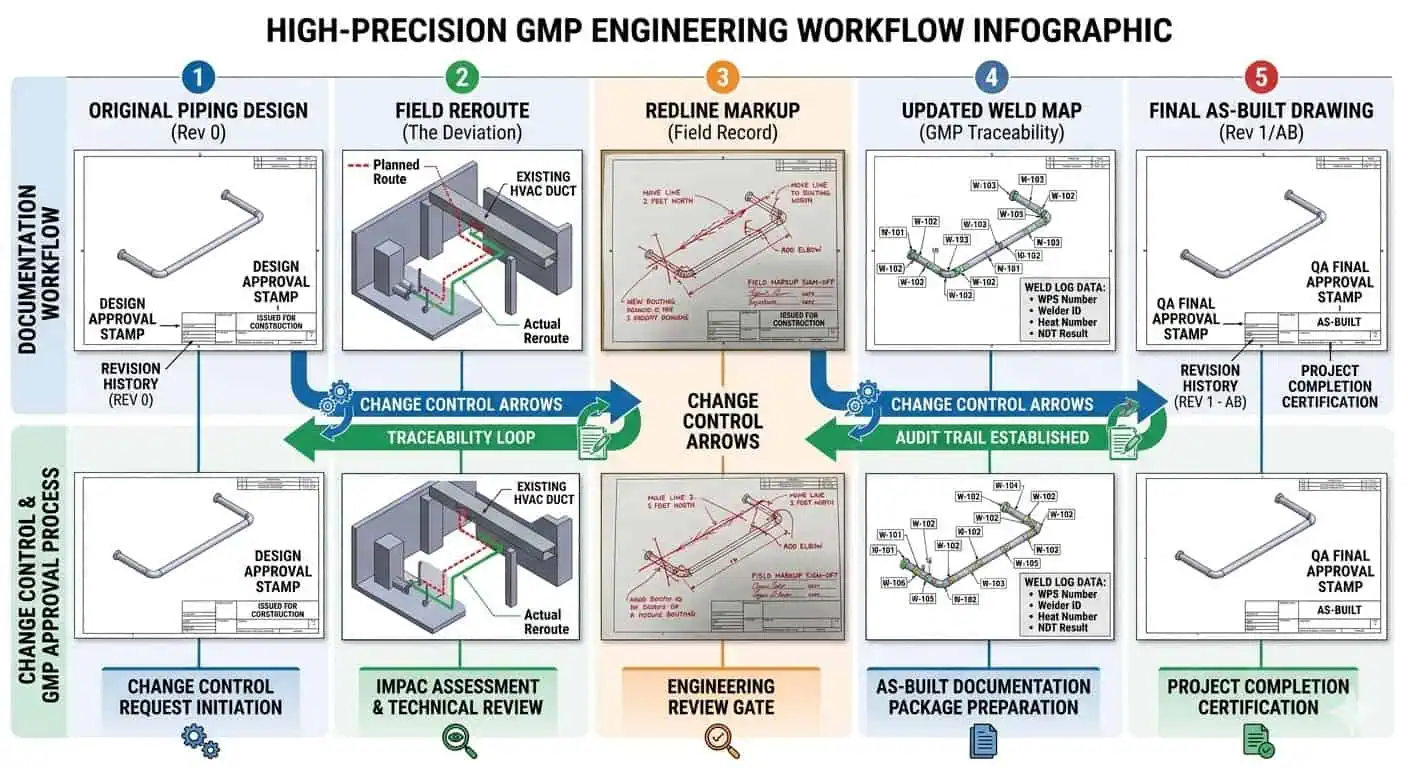
Consiglio esperto: Le deviazioni in campo non sono il vero problema. Le prove non chiuse derivanti dalle deviazioni in campo sono il vero problema. Il progetto dovrebbe trattare le redlines e gli as-builts come strumenti di controllo attivi, non come attività di disegno in fase finale.
Il Pacchetto di Documentazione di Base che i Team GMP Solitamente Si Aspettano
Documentazione dei Materiali
La documentazione dei materiali dimostra che i materiali bagnati approvati sono effettivamente entrati nel sistema. Al minimo, questo di solito significa certificati dei materiali, tracciabilità del calore, controllo di ricevimento e una qualche forma di mappatura della posizione che collega i componenti installati al set di record dei materiali approvati. Più forte è la conseguenza igienica o di contatto con il prodotto, meno accettabile diventa lasciare vaga questa relazione.
Documentazione di Fabbricazione e Saldatura
La documentazione di fabbricazione dimostra come il sistema è diventato ciò che è. Qui di solito si trovano mappe di saldatura, registri di saldatura orbitale, risultati di ispezione delle saldature, storie di riparazione, registri di boroscopia dove richiesti e tracciamento dello stato di fabbricazione. Il punto non è creare un dossier spesso per il suo stesso scopo. Il punto è mantenere il circuito installato verificabile e tecnicamente difendibile.
Documentazione di Superficie e Trattamento
I registri di superficie sono importanti quando la finitura o il trattamento post-fabbricazione fa parte del requisito igienico. Se il progetto specifica elettrolucidatura, passivazione o un obiettivo di finitura definito, il pacchetto di consegna dovrebbe mostrare come tale requisito è stato applicato e come le parti rilevanti sono state identificate. Altrimenti, il progetto rischia di avere un requisito di finitura sulla carta ma nessuna prova solida che la superficie installata corrisponda ancora ad esso.
Documentazione di Collaudo e Consegna
I registri di collaudo e consegna trasformano la storia di fabbricazione in prove di rilascio. Le prove di pressione, le prove di tenuta, la chiusura delle ispezioni, la chiusura della lista di difetti e l'assemblaggio del dossier finale sono dove il progetto dimostra che il circuito fabbricato non è stato solo costruito, ma anche verificato e chiuso in modo da supportare l'operazione GMP.
Caso tipico del settore: il progetto ha tutti i registri individuali da qualche parte, ma la consegna si blocca ancora perché il pacchetto non è strutturato nel modo in cui l'assicurazione qualità ha bisogno di rivedere e approvare il circuito. Questo non è solo un problema di documenti mancanti. È un problema di logica del dossier.

Consiglio esperto: se i documenti di consegna vengono assemblati per la prima volta solo dopo il completamento meccanico, il progetto è già in ritardo dal punto di vista del controllo della documentazione.
Registri di Controllo delle Modifiche e Deviazioni
La documentazione delle modifiche è ciò che mantiene credibile la catena di prove finale. Il progetto deve essere in grado di mostrare cosa è cambiato, chi lo ha approvato, quale ispezione o rielaborazione è seguita e come la condizione finale come costruita ha assorbito tale modifica. Senza questo, anche le modifiche tecnicamente ragionevoli sul campo possono creare inutili esitazioni nel controllo qualità.
| Set di Documentazione | Cosa Dimostra | Dove Fallisce Comune |
|---|---|---|
| Certificati dei materiali e matrice di tracciabilità | I materiali a contatto approvati sono stati effettivamente installati | La mappatura della posizione diventa poco chiara dopo il taglio o il reindirizzamento sul campo |
| Mappe di saldatura e registri di saldatura | Le saldature finali sono state completate e ispezionate sotto controllo | I numeri di saldatura smettono di corrispondere alle revisioni finali dei tratti |
| Registri di finitura / EP / passivazione | La condizione superficiale specificata è stata raggiunta e preservata | Le modifiche di rifacimento o di finitura tardiva non sono completamente documentate |
| Redlines e as-built | Il circuito installato corrisponde alla configurazione finale approvata | Le modifiche in campo avvengono più velocemente della chiusura dei disegni |
| Dossier di consegna | La catena di prove completa è pronta per la revisione QA | I registri esistono, ma non in una struttura pronta per il rilascio |
Dove le catene di documentazione solitamente si interrompono
Il materiale era corretto, ma la matrice di tracciabilità era debole.
Uno dei fallimenti più comuni non è la mancanza di materiale, ma una mappatura debole tra materiale e posizione. I team a volte assumono che avere i certificati sia sufficiente. Non è sufficiente se il progetto non può dimostrare rapidamente dove è finito il materiale certificato dopo il taglio, la fabbricazione, l'avvolgimento e le modifiche in campo.
Le saldature erano accettabili, ma il set di registri di saldatura era incompleto.
Un circuito può essere tecnicamente valido e comunque fallire la chiusura della documentazione perché il set di registri di saldatura è incompleto. La mancanza dello stato di saldatura, una storia di riparazione poco chiara o una numerazione delle saldature disallineata di solito creano più ritardi di quanto i team si aspettino. Nelle tubazioni GMP, l'evidenza della saldatura non è solo uno strumento di fabbricazione. Fa parte della prontezza al rilascio.
Le modifiche in campo sono avvenute più velocemente dell'aggiornamento della documentazione.
La documentazione spesso rimane indietro rispetto al progetto proprio nel momento in cui il progetto diventa più dinamico. Le modifiche al percorso in fase avanzata, le revisioni dei collegamenti, le regolazioni di montaggio in campo e i rami aggiunti spesso si verificano sotto pressione di programma. Se il set di documenti non tiene il passo, il pacchetto di consegna finale diventa un esercizio di ricostruzione invece di una consegna controllata.
I componenti più piccoli hanno creato il problema di controllo qualità più grande.
Le piccole parti a contatto con il fluido creano un rischio documentale sproporzionato. I raccordi, i componenti di campionamento, i diaframmi, le guarnizioni e le parti a contatto con il fluido correlate agli strumenti sono spesso dove la catena di evidenza più pulita si interrompe per prima. I team tendono a pensare in termini di tratti di tubazione, ma il controllo qualità spesso sperimenta il progetto in termini di assemblaggi locali irrisolti.
Lezione esperta dal lavoro di chiusura in campo: più l'assemblaggio è locale e sostituibile, meno è sicuro presumere che i suoi registri si prenderanno cura di sé stessi.
Come gli ingegneri dovrebbero costruire i requisiti di documentazione prima della RFQ
Definire cosa deve essere tracciabile
Prima della RFQ, definire quali componenti a contatto con il fluido devono rimanere tracciabili attraverso l'installazione e la consegna. Se solo la tubazione è controllata e le parti a contatto con il fluido più piccole sono lasciate vaghe, la catena di evidenza sarà solitamente più debole dove l'assemblaggio alimentare è più complesso.
Definire cosa deve essere registrato durante la fabbricazione
I progetti dovrebbero definire cosa deve essere registrato mentre il lavoro è in corso, non solo cosa deve esistere alla fine. I registri di saldatura, i punti di ispezione, i documenti relativi alla finitura, le prove di passivazione ove pertinenti e gli aggiornamenti delle modifiche in campo dovrebbero far parte del flusso di progetto definito.
Definire Cosa il Controllo Qualità Deve Ricevere alla Consegna
Il pacchetto di consegna dovrebbe essere definito come una consegna di rilascio, non una raccolta vaga di qualsiasi cosa l'appaltatore possa assemblare in seguito. Se il Controllo Qualità si aspetta una struttura specifica del dossier, una matrice di tracciabilità o un formato di registrazione, il progetto dovrebbe definirli mentre ha ancora tempo per generare tali documenti correttamente.
Definire Cosa Deve Essere Mantenuto Dopo l'Avvio
La catena documentale dovrebbe sopravvivere nell'operatività, non fermarsi alla consegna. I registri delle apparecchiature, i documenti di manutenzione, la tracciabilità dei pezzi di ricambio e gli aggiornamenti controllati del sistema installato fanno tutti parte del mantenimento della catena di prove originale. Un sistema pronto per il rilascio può diventare molto più difficile da difendere in seguito se i documenti del ciclo di vita sono deboli.
Il consiglio di progetto più forte è semplice: definire la catena di prove prima dell'approvvigionamento. Non aspettare che la fabbricazione sia in corso per decidere se la tracciabilità termica, i registri di finitura, lo stato di saldatura o la documentazione delle modifiche in campo saranno importanti. A quel punto, il progetto di solito finisce per raccogliere documenti in modo reattivo invece di controllarli deliberatamente. Questa è una delle lezioni pratiche più chiare del lavoro di consegna GMP: i progetti che definiscono il set di documenti prima della RFQ di solito si chiudono più velocemente e con meno sorprese di Controllo Qualità rispetto ai progetti che cercano di ricostruirlo in seguito.
Come Questo Si Collega alla Progettazione, ai Materiali e alla Selezione dei Raccordi
Selezione del Materiale Senza Controllo Documentale Non È Rischio Chiuso
Una buona decisione sui materiali diventa una decisione di progetto sicura solo quando è documentata in modo chiaro. Per la logica più ampia relativa ai materiali, collegare questa pagina con Selezione Materiali Tubazioni Alimentari Farmaceutiche.
I Requisiti di Finitura Contano Solo Se Sono Dimostrati
L'elettrolucidatura, gli obiettivi di finitura e le aspettative di post-trattamento non chiudono il rischio a meno che i registri non li dimostrino. Collegare questo argomento con Acciaio inossidabile 316L elettrolucidato vs 316L standard.
I Raccordi e i Gruppi Campione Hanno Bisogno della Loro Propria Catena di Prove
Più piccolo e locale diventa il gruppo, più è probabile che la sua documentazione diventi la parte più debole del pacchetto di consegna. Collegare questo argomento con Selezione di raccordi alimentari per strutture GMP.
La Documentazione Come Costruita Deve Riflettere il Reale Rischio di Pulibilità
La documentazione non dovrebbe solo dimostrare ciò che è stato installato. Dovrebbe anche riflettere la realtà igienica finale locale del sistema. Per quella logica, collegare questa pagina con Considerazioni di Progettazione CIP per Tubazioni Alimentari.
Errori Comuni nella Documentazione e Tracciabilità per Progetti di Tubazioni Farmaceutiche
Trattare la Documentazione come un'Attività di Consegna invece che come un Input di Progettazione
I progetti che definiscono il pacchetto documentale in ritardo spesso finiscono per ricostruire i registri sotto pressione di programma.
Tracciare i Tubi ma non Tracciare i Piccoli Componenti a Contatto con il Fluido
Il collegamento di tracciabilità più debole spesso appare in raccordi, guarnizioni, diaframmi o assemblaggi locali di campioni.
Mantenere i Dati di Saldatura Separati dalla Logica di Rilascio a Livello di Linea
I registri di saldatura sono molto meno utili se non si mappano chiaramente al circuito finale installato e al suo stato di rilascio.
Permettere che le Modifiche in Campo si Allontanino dalla Realtà Installata
Quando le modifiche in campo procedono più velocemente degli aggiornamenti controllati, il pacchetto di consegna diventa più difficile da fidarsi.
Supponendo che il Controllo Qualità lo accetti successivamente
Nelle tubazioni GMP, la mancanza di prove è raramente più facile da correggere alla fine del progetto rispetto all'esecuzione controllata.
Raccolta eccessiva di documenti ma definizione insufficiente di ciò che conta realmente
I grandi volumi di documenti non creano automaticamente un pacchetto di consegna solido. Ciò che conta è se il set di registri dimostra il sistema alimentare installato in modo sufficientemente chiaro per il rilascio e il successivo controllo del ciclo di vita.
Lista di controllo pratica: cosa chiedere prima di rilasciare un sistema di tubazioni farmaceutiche
Prima dell'inizio della fabbricazione
- Quali componenti a contatto con il fluido devono essere tracciabili?
- Quali registri devono essere creati durante la fabbricazione?
- Quali prove di saldatura, finitura e ispezione richiederà il Controllo Qualità successivamente?
- Come verranno incorporate le modifiche in campo nei registri controllati?
Prima del Completamento Meccanico
- Le modifiche in rosso sono aggiornate?
- I componenti installati corrispondono chiaramente ai registri materiali approvati?
- Lo stato delle saldature e la cronologia delle riparazioni sono chiusi?
- I registri di finitura e trattamento sono completi dove richiesto?
Prima del Rilascio QA
- Il pacchetto di consegna corrisponde al circuito effettivamente installato?
- Ci sono assemblaggi locali ancora irrisolti nei registri di tracciabilità o ispezione?
- Il progetto può dimostrare la condizione finale come-costruita in modo sufficientemente chiaro per il rilascio?
Dopo l'Avvio
- Come continueranno i registri delle attrezzature e i record di manutenzione?
- Come rimarranno tracciabili i pezzi di ricambio?
- Come verranno collegati i futuri cambiamenti alla catena di evidenza originale?
| Fase del Progetto | Domanda Chiave di Documentazione | Come Appare un Buon Controllo |
|---|---|---|
| Prima della RFQ | Cosa deve essere tracciabile e consegnabile? | Il set di record è definito, non assunto |
| Durante la fabbricazione | I record vengono creati in tempo reale? | I record di saldatura, materiale, finitura e modifiche rimangono aggiornati |
| Prima della consegna | Il dossier corrisponde alla realtà installata? | I record as-built, la tracciabilità e la chiusura delle ispezioni sono allineati |
| Dopo l'avvio | La catena delle prove sopravviverà ai cambiamenti del ciclo di vita? | I record di manutenzione e sostituzione continuano sotto controllo |
Conclusione: Nell'impiantistica farmaceutica, la documentazione dimostra che il sistema che pensi di aver costruito è il sistema che hai effettivamente installato
Una buona documentazione e tracciabilità non aggiungono valore dopo il progetto. Proteggono il progetto dal rischio di non poter essere rilasciato proprio nel momento in cui dovrebbe essere pronto per funzionare. Nell'impiantistica farmaceutica, il sistema installato è accettabile solo quanto la catena di prove che dimostra che materiale, fabbricazione, finitura, ispezione e modifiche siano state controllate.
I progetti più solidi non cercano di ricostruire questa catena di prove al momento del passaggio di consegne. La definiscono prima della richiesta di offerta, la mantengono durante la fabbricazione e la chiudono prima del rilascio. Per l'intero cluster di argomenti farmaceutici, collega questo articolo con Selezione Materiali Tubazioni Alimentari Farmaceutiche, Acciaio inossidabile 316L elettrolucidato vs 316L standard, Selezione di raccordi alimentari per strutture GMP, e Considerazioni di Progettazione CIP per Tubazioni Alimentari.
FAQ
Quale documentazione è richiesta per i progetti di tubazioni farmaceutiche?
Il pacchetto esatto dipende dall'ambito del progetto, ma di solito include certificati dei materiali, registri di tracciabilità, documentazione delle saldature, registri di ispezione, prove di finitura o trattamento dove richiesto, modifiche in rosso, as-built e registri di passaggio di consegne che supportano il rilascio QA.
Quale tracciabilità è richiesta nelle tubazioni GMP?
La tracciabilità dovrebbe seguire il percorso a contatto con il fluido. Ciò spesso significa che tubazioni, raccordi, valvole, assemblaggi locali e altri componenti critici a contatto con il prodotto devono essere tracciabili fino a registri approvati in modo che corrispondano ancora alla condizione installata.
Perché i progetti di tubazioni farmaceutiche falliscono alla consegna?
Spesso falliscono perché la catena di prove è incompleta. L'installazione può essere fisicamente accettabile, ma registri mancanti o deboli su materiale, saldatura, finitura o as-built possono comunque ritardare il rilascio QA.
I raccordi e le guarnizioni richiedono tracciabilità nei progetti GMP?
In molte applicazioni igieniche critiche, sì. I componenti più piccoli a contatto con il fluido sono spesso dove appare l'anello di documentazione più debole, quindi non dovrebbero essere trattati come consumabili casuali se influenzano le prestazioni igieniche o il rischio di rilascio.
Sono richiesti registri di saldatura per tubazioni alimentari farmaceutiche?
I progetti si affidano comunemente a mappe di saldatura e documentazione di saldatura perché sono centrali per dimostrare lo stato di fabbricazione e ispezione. Il formato esatto varia in base al progetto, ma la documentazione delle saldature deboli è uno dei problemi più comuni di consegna.
Qual è la differenza tra documentazione as-built e documenti di consegna?
I record as-built mostrano la configurazione finale installata. I documenti di consegna sono il pacchetto di prove più ampio utilizzato per supportare il rilascio, inclusi tracciabilità, ispezione, test e relativi record di progetto.




